Электроды в электрической цепи, к которым подсоединяются выводы источника тока или нагрузки, принято называть анодом и катодом. Эти термины позволяют определить направление электрического тока в цепи и полярность подключения. Правильная полярность важна для работы полупроводниковых приборов - диодов, транзисторов, микросхем. Неправильное подключение может привести к выходу электронных компонентов из строя.
Определение анода и катода по отношению к направлению тока
Анод и катод - это электроды, определяемые по отношению к направлению тока в электрической цепи. Анод - это электрод, в который условно втекает электрический ток, а катод - электрод, из которого ток вытекает. Несмотря на условность направления тока, эти понятия позволяют правильно определить полярность подключения полупроводниковых приборов для их корректной работы.
При определении анода и катода в первую очередь нужно ориентироваться на реальное направление движения носителей заряда, а не на знаки полюсов источника питания. Например, в аккумуляторах при перезарядке происходит смена ролей анода и катода, поскольку меняется направление тока. Электрод, бывший катодом в режиме разрядки, становится анодом при зарядке.
- При электролизе положительные ионы движутся к катоду, а отрицательные - к аноду, в соответствии с направлением электрического поля.
- В вакуумных лампах электроны всегда движутся от катода к аноду, создавая электрический ток.
Таким образом, определяя реальное направление движения носителей заряда, можно правильно идентифицировать анод и катод в любой электрической цепи или электронном приборе. Это важно для обеспечения нужной полярности при подключении.
Маркировка выводов на корпусах радиодеталей
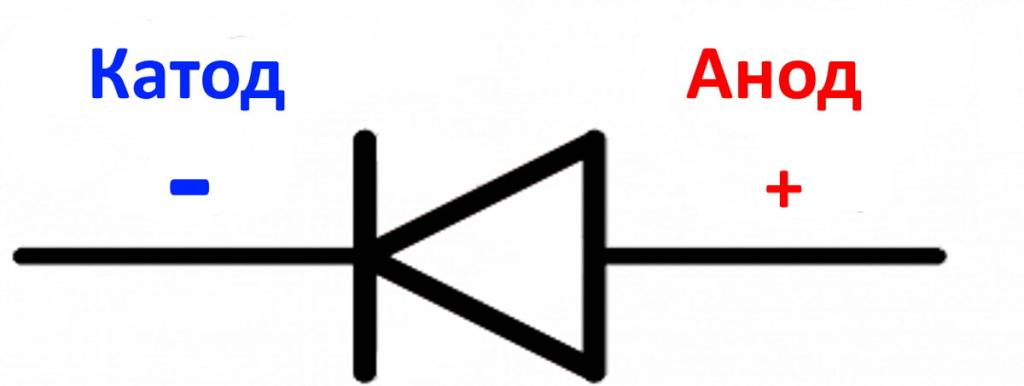
Для правильного определения анода и катода радиодеталей часто используется специальная маркировка выводов на их корпусах. Это могут быть точки, полоски, знаки «плюс» или «минус» либо буквенные обозначения «А» и «К».
Например, у полупроводниковых диодов катод, как правило, маркируется полоской или точкой на корпусе. Анод не имеет специальных обозначений. Таким образом, по маркировке легко определить нужную полярность подключения анода и катода при монтаже.
У электронных ламп выводы анода и катода четко совпадают с контактами соответствующего гнезда, что исключает ошибки. Вывод сетки тоже имеет фиксированное положение.
Полярность выводов транзисторов указывается буквами «Э», «Б», «К» - эмиттер, база, коллектор. Иногда эмиттер маркируют полоской или точкой. Зная тип проводимости транзистора по таблице и определив эмиттер, можно понять, где находится коллектор, выполняющий роль анода.
Таким образом, правильная маркировка контактов на корпусах радиоэлементов позволяет безошибочно идентифицировать анод и катод при монтаже схемы. Это важно для корректной работы всего устройства.
Определение по схеме устройства или таблицам для радиодеталей
Если есть принципиальная схема устройства, то по ней можно довольно легко определить назначение выводов у различных радиодеталей. На схемах обычно указываются направления и величины токов, позволяющие понять полярность подключения.
Например, у схем выпрямительных диодов и транзисторов стрелкой указано направление проводимости от анода к катоду или от эмиттера к коллектору. Это наглядно демонстрирует принцип работы полупроводникового прибора.
При отсутствии схемы можно воспользоваться справочными таблицами с типами проводимости транзисторов и их характеристиками. Из таблицы определяем тип транзистора, затем по маркировке находим эмиттер. Далее по типу проводимости PNP или NPN понимаем, где находится коллектор, являющийся анодом, а эмиттер в этом случае - катод.
У радиоламп, например триодов, на схеме изображается расположение анода, сетки и катода относительно друг друга. Такие схемы однозначно позволяют определить назначение выводов лампы.
Дополнительно на печатных платах устройств часто наносится маркировка контактов разъемов, куда впаиваются выводы деталей. Это также облегчает правильный монтаж схемы и исключает ошибки.
Таким образом, схемы и справочные таблицы позволяют точно определять назначение выводов для различных типов радиодеталей. Это особенно актуально при ремонте старой радиоаппаратуры с неразборчивой или утраченной маркировкой элементов.
Применение анода и катода в гальванике для защиты от коррозии
В гальванотехнике анод и катод широко используются при электролитическом нанесении металлических покрытий на изделия с целью их защиты от коррозии. Этот процесс называется гальваническим восстановлением металлов или просто гальванизацией.
Суть метода заключается в следующем: деталь, подлежащая защите, погружается в раствор-электролит в качестве катода вместе с металлической заготовкой, выступающей анодом. К ним подводится постоянный электрический ток определенной плотности от внешнего источника.
Под действием тока происходит анодное растворение металла анода с образованием положительно заряженных ионов, которые движутся к катоду и восстанавливаются на его поверхности в виде чистого металла. Так, например, осуществляют нанесение слоя цинка на сталь для катодной защиты от коррозии.
Толщина получаемого гальванического покрытия зависит от плотности тока и времени электролиза. Правильный подбор параметров тока позволяет получать очень тонкие и равномерные металлические покрытия.
Таким образом, благодаря использованию анодно-катодных процессов при электролизе растворов солей можно эффективно защищать металлические изделия от коррозии с помощью гальванопокрытий. Это широко применяется в современной промышленности.
Работа вакуумных ламп на основе термоэмиссии электронов

Вакуумные электронные лампы, такие как диоды и триоды, работают благодаря процессу термоэлектронной эмиссии, происходящей между нагретым катодом и анодом в вакуумированном баллоне лампы.
Катод представляет собой вольфрамовую нить накала, которая разогревается до высокой температуры приблизительно 2000°C путем пропускания через нее электрического тока. При этом с поверхности катода начинают интенсивно испускаться электроны – происходит термоэмиссия.
Анод вакуумной лампы имеет положительный потенциал по отношению к катоду. Поэтому эмитированные катодом электроны устремляются к аноду в виде термоэлектронного тока в вакууме. Этот ток можно легко регулировать, изменяя температуру катода.
У триодов имеется дополнительный электрод – управляющая сетка, расположенная между катодом и анодом. Изменяя напряжение на этой сетке, можно регулировать величину анодного тока в еще более широких пределах.
Таким образом, благодаря использованию анодно-катодной термоэмиссии в вакууме, стало возможным создание таких электронных устройств, как электронные лампы, диоды, триоды, тетроды, работа которых лежит в основе функционирования электронной техники прошлого века.
Использование в полупроводниковых диодах и транзисторах
В современной радиоэлектронной аппаратуре понятия «анод» и «катод» широко используются по отношению к полупроводниковым диодам и транзисторам, которые практически полностью вытеснили вакуумные электронные лампы.
Полупроводниковые диоды обладают односторонней проводимостью – пропускают электрический ток только в прямом направлении от анода к катоду. В обратном направлении диод является непроводящим. Это свойство используется для выпрямления переменного тока в постоянный.
У транзисторов выделяют эмиттер, базу и коллектор с разными функциями. Но по аналогии с вакуумными приборами, эмиттер часто называют катодом, коллектор - анодом, а база выполняет роль управляющего электрода.
Транзисторы могут работать в двух режимах. В режиме с общим эмиттером основной ток идет от эмиттера (катода) к коллектору (аноду), а база управляет этим током. В режиме с общей базой ток управления протекает от эмиттера к коллектору.
Таким образом, использование анодно-катодных свойств полупроводниковых диодов и транзисторов позволило создать надежные, компактные и экономичные электронные схемы, полностью вытеснившие ламповые устройства из современной радиоэлектроники.


























