Неметаллический элемент 15-й группы [Va] периодической таблицы – азот, 2 атома которого, соединяясь, образуют молекулу, – бесцветный, без запаха и вкуса газ, составляющий большую часть атмосферы Земли и являющийся составной частью всего живого.
История обнаружения
Газ азот составляет около 4/5 земной атмосферы. Он был выделен в ходе ранних исследований воздуха. В 1772 году шведский химик Карл-Вильгельм Шееле первым продемонстрировал, что такое азот. По его мнению, воздух представляет собой смесь двух газов, один из которых он назвал «огненным воздухом», т. к. тот поддерживал горение, а другой – «нечистым воздухом», потому что он оставался после того, как первый расходовался. Это были кислород и азот. Примерно в то же время азот был выделен шотландским ботаником Даниэлем Резерфордом, который первым опубликовал свои выводы, а также британским химиком Генри Кавендишем и британским священнослужителем и ученым Джозефом Пристли, который разделил с Шееле первенство открытия кислорода. Дальнейшие исследования показали, что новый газ входит в состав селитры, или нитрата калия (KNO3), и, соответственно, он был назван нитрогеном ("рождающим селитру") французским химиком Шапталем в 1790 г. Азот был впервые отнесен к химическим элементам Лавуазье, чье объяснение роли кислорода в горении опровергло теорию флогистона – популярное в XVIII в. ошибочное представление о горении. Неспособность этого химического элемента поддерживать жизнь (по-гречески ζωή) стала причиной того, что Лавуазье назвал газ азотом.

Возникновение и распространение
Что такое азот? По распространенности химических элементов он занимает шестое место. Атмосфера Земли на 75,51 % по весу и на 78,09 % по объему состоит из этого элемента и является основным его источником для промышленности. В атмосфере также содержится небольшое количество аммиака и солей аммония, а также оксиды азота и азотная кислота, образующиеся во время гроз, а также в двигателях внутреннего сгорания. Свободный азот найден во многих метеоритах, вулканических и шахтных газах и некоторых минеральных источниках, на солнце, в звездах и туманностях.
Азот также встречается в минеральных отложениях нитрата калия и натрия, но для удовлетворения потребностей человека их недостаточно. Другим материалом, богатым этим элементом, является гуано, которое можно найти в пещерах, где много летучих мышей, или в сухих местах, посещаемых птицами. Также азот содержится в дожде и почве в виде аммиака и солей аммония, а в морской воде в виде ионов аммония (NH4+), нитритов (NO2-) и нитратов (NO3-). В среднем он составляет около 16 % сложных органических соединений, таких как белки, присутствующих во всех живых организмах. Естественное его содержание в земной коре составляет 0,3 части на 1000. Распространенность в космосе – от 3 до 7 атомов на атом кремния.
Крупнейшими странами-производителями азота (в виде аммиака) в начале XXI века были Индия, Россия, США, Тринидад и Тобаго, Украина.

Коммерческое производство и использование
Промышленное производство азота основано на фракционной перегонке сжиженного воздуха. Температура его кипения равна -195,8 °С, что на 13 °С ниже, чем у кислорода, который таким образом отделяется. Азот также может быть получен в больших масштабах путем сжигания углерода или углеводородов в воздухе и отделения полученного диоксида углерода и воды из остаточного азота. В малых масштабах чистый азот производится путем нагревания азида бария Ba(N3)2. Лабораторные реакции включают нагрев раствора нитрита аммония (NH4NO2), окисление аммиака водным раствором брома или нагретым оксидом меди:
- NH4++NO2-→N2+2H2O.
- 8NH3+3Br2→N2+6NH4++6Br-.
- 2NH3+3CuO→N2+3H2O+3Cu.
Элементарный азот может быть использован в качестве инертной атмосферы для реакций, требующих исключения кислорода и влаги. Находит применение и жидкий азот. Водород, метан, окись углерода, фтор и кислород – единственные вещества, которые при температуре кипения азота не переходят в твердое кристаллическое состояние.
В химической промышленности этот химический элемент используется для предотвращения окисления или другой порчи продукта, как инертный разбавитель химически активного газа, для удаления тепла или химических веществ, а также в качестве ингибитора пожара или взрыва. В пищевой промышленности газ азот применяется для предотвращения порчи продуктов, а жидкий – для сушки замораживанием и в системах охлаждения. В электротехнической промышленности газ предотвращает окисление и другие химические реакции, создает давление в оболочке кабеля и защищает электродвигатели. В металлургии азот используется при сварке и пайке, предотвращая окисление, обуглероживание и обезуглероживание. Как неактивный газ его применяют в производстве пористой резины, пластмассы и эластомеров, он служит в качестве пропеллента в аэрозольных баллончиках, а также создает давление жидкого топлива в реактивных самолетах. В медицине быстрое замораживание жидким азотом используется для сохранения крови, костного мозга, тканей, бактерий и спермы. Он нашел применение и в криогенных исследованиях.

Соединения
Большая часть азота используется в производстве химических соединений. Тройная связь между атомами элемента настолько сильна (226 ккал на моль, вдвое больше, чем у молекулярного водорода), что молекула азота с трудом вступает в другие соединения.
Основным промышленным методом фиксации элемента является процесс Хабера-Боша для синтеза аммиака, разработанный во время Первой мировой войны, чтобы уменьшить зависимость Германии от чилийской селитры. Он включает прямой синтез NH3 – бесцветного газа с резким, раздражающим запахом – непосредственно из его элементов.
Большая часть аммиака превращается в азотную кислоту (HNO3) и нитраты – соли и сложные эфиры азотной кислоты, кальцинированную соду (Na2CO3), гидразин (N2H4) – бесцветную жидкость, используемую в качестве ракетного топлива и во многих промышленных процессах.
Азотная кислота является другим основным коммерческим соединением данного химического элемента. Бесцветная, высококоррозионная жидкость используется в производстве удобрений, красителей, лекарственных средств и взрывчатых веществ. Нитрат аммония (NH4NO3) – соль аммиака и азотной кислоты – является наиболее распространенным компонентом азотных удобрений.

Азот + кислород
С кислородом азот образует ряд оксидов, в т. ч. закись азота (N2O), в которой его валентность равна +1, окись (NO) (+2) и двуокись (NO2) (+4). Многие оксиды азота чрезвычайно летучи; они являются главными источниками загрязнения в атмосфере. Закись азота, также известная как веселящий газ, иногда используется в качестве анестезирующего средства. При вдыхании она вызывает мягкую истерию. Оксид азота быстро реагирует с кислородом с образованием коричневого диоксида, промежуточного продукта в производстве азотной кислоты и мощного окислителя в химических процессах и ракетном топливе.
Также используются некоторые нитриды, образованные соединением металлов с азотом при повышенных температурах. Нитриды бора, титана, циркония и тантала имеют специальные применение. Одна кристаллическая форма нитрида бора (BN), например, по твердости не уступает алмазу и плохо окисляется, поэтому используется в качестве высокотемпературного абразива.
Неорганические цианиды содержат группу CN-. Цианистый водород, или синильная кислота HCN, является крайне неустойчивым и чрезвычайно токсичным газом, который применяется для фумигации, концентрации руды, в других промышленных процессах. Дициан (CN)2 используется в качестве промежуточного химического вещества и для фумигации.
Азиды представляют собой соединения, которые содержат группу из трех атомов азота -N3. Большинство их неустойчиво и очень чувствительно к ударам. Некоторые из них, такие как азид свинца Pb(N3)2, используются в детонаторах и капсюлях. Азиды, подобно галогенам, охотно взаимодействуют с другими веществами и образуют множество соединений.
Азот входит в состав нескольких тысяч органических соединений. Большинство из них являются производными от аммиака, цианистого водорода, циана, закиси или азотной кислоты. Амины, аминокислоты, амиды, например, получены из аммиака или тесно связаны с ним. Нитроглицерин и нитроцеллюлоза – сложные эфиры азотной кислоты. Нитриты получают из азотистой кислоты (HNO2). Пурины и алкалоиды являются гетероциклическими соединениями, в которых азот замещает один или несколько атомов углерода.

Свойства и реакции
Что такое азот? Это бесцветный газ без запаха, который конденсируется при -195,8 °С в бесцветную, маловязкую жидкость. Элемент существует в виде молекул N2, представляемых в виде :N:::N:, у которых энергия связи, равная 226 ккал на моль, уступает только окиси углерода (256 ккал на моль). По этой причине энергия активации молекулярного азота очень высока, поэтому в обычных условиях элемент относительно инертен. Кроме того, высокостабильная молекула азота в значительной степени способствует термодинамической неустойчивости многих азотсодержащих соединений, в которых связи, пусть и достаточно сильные, но уступают связям молекулярного азота.
Относительно недавно и неожиданно была открыта способность молекул азота служить в качестве лигандов в комплексных соединениях. Наблюдение того, что некоторые растворы комплексов рутения могут поглощать атмосферный азот, привело к тому, что вскоре может быть найден более простой и лучший способ фиксации этого элемента.
Активный азот можно получить путем пропускания газа низкого давления через высоковольтный электрический разряд. Продукт светится желтым светом и гораздо охотнее вступает в реакции, чем молекулярный, с атомарным водородом, серой, фосфором и различными металлами, а также способен разлагать NO до N2 и O2.
Более ясное представление о том, что такое азот, можно получить благодаря его электронной структуре, которая имеет вид 1s22s22p3. Пять электронов внешних оболочек слабо экранируют заряд, в результате чего эффективный ядерный заряд ощущается на расстоянии ковалентного радиуса. Атомы азота относительно невелики и обладают высокой электроотрицательностью, располагаясь между углеродом и кислородом. Электронная конфигурация включает три полузаполненные внешние орбитали, позволяющие образовывать три ковалентные связи. Поэтому атом азота должен обладать чрезвычайно высокой реакционной способностью, образуя с большинством других элементов стабильные бинарные соединения, особенно когда другой элемент существенно отличается электроотрицательностью, придающей значительную полярность связям. Когда электроотрицательность другого элемента ниже, полярность придает атому азота частичный отрицательный заряд, что освобождает его неразделенные электроны для участия в координационных связях. Когда другой элемент более электроотрицателен, частично положительный заряд азота существенно ограничивает донорные свойства молекулы. При малой полярности связи, вследствие равной электроотрицательности другого элемента, множественные связи превалируют над одиночными. Если несоответствие атомных размеров препятствует образованию множественных связей, то образованная простая связь, вероятно, будет относительно слабой, и соединение будет неустойчивым.
Аналитическая химия
Часто процент азота в газовой смеси может быть определен путем измерения ее объема после поглощения других компонентов химическими реагентами. Разложение нитратов серной кислотой в присутствии ртути высвобождает окись азота, которая может быть измерена в виде газа. Азот высвобождается из органических соединений, когда они сгорают над окисью меди, а свободный азот может быть измерен в виде газа после поглощения других продуктов сгорания. Хорошо известный метод Кьельдаля по определению содержания рассматриваемого нами вещества в органических соединениях заключается в разложении соединения концентрированной серной кислотой (в случае необходимости содержащей ртуть, или ее оксид, а также различные соли). Таким образом азот преобразуется в сульфат аммония. Добавление гидроксида натрия высвобождает аммиак, который собирают обычной кислотой; остаточное количество непрореагировавшей кислоты затем определяется титрованием.

Биологическое и физиологическое значение
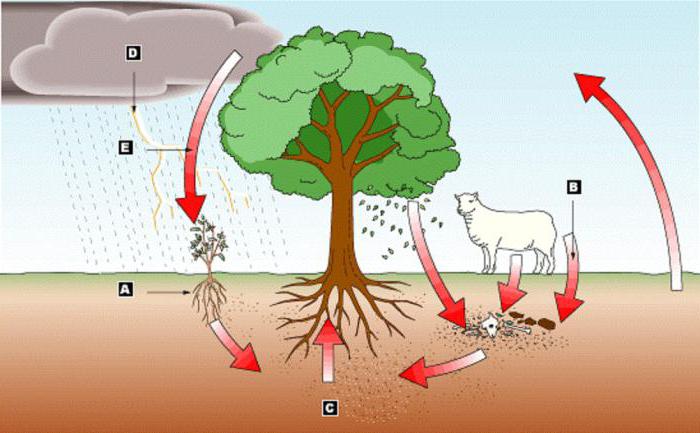
Роль азота в живой материи подтверждает физиологическую активность его органических соединений. Большинство живых организмов не может использовать этот химический элемент непосредственно и должно иметь доступ к его соединениям. Поэтому фиксация азота имеет огромное значение. В природе это происходит в результате двух основных процессов. Одним из них является действие электрической энергии на атмосферу, благодаря чему молекула азота и кислорода диссоциируют, что позволяет свободным атомам образовать NO и NO2. Двуокись затем вступает в реакцию с водой: 3NO2+H2O→2HNO3+NO.
HNO3 растворяется и приходит на Землю с дождем в виде слабого раствора. Со временем кислота становится частью комбинированного азота почвы, где нейтрализуется, образуя нитриты и нитраты. Содержание N в культивируемых почвах, как правило, восстанавливается благодаря внесению удобрений, содержащих нитраты и аммонийные соли. Выделения животных и растений и их разложение возвращает соединения азота в почву и воздух.
Другим основным процессом естественной фиксации является жизнедеятельность бобовых. Благодаря симбиозу с бактериями эти культуры способны превращать атмосферный азот непосредственно в его соединения. Некоторые микроорганизмы, такие как Azotobacter Chroococcum и Clostridium pasteurianum, способны фиксировать N самостоятельно.
Сам газ, будучи инертным, безвреден, за исключением случая, когда им дышат под давлением, и он растворяется в крови и других жидкостях тела в более высоких концентрациях. Это вызывает наркотический эффект, а если давление снижается слишком быстро, избыток азота выделяется в виде пузырьков газа в различных местах организма. Это может вызвать боль в мышцах и суставах, обмороки, частичный паралич и даже смерть. Эти симптомы называются декомпрессионной болезнью. Поэтому те, кто вынужден дышать воздухом в таких условиях, должны очень медленно снижать давление до нормального, чтобы избыток азота выходил через легкие без образования пузырьков. Лучшей альтернативой является использование для дыхания смеси кислорода и гелия. Гелий гораздо менее растворим в жидкостях организма, и опасность уменьшается.
Изотопы
Азот существует в виде двух стабильных изотопов: 14N (99,63 %) и 15N (0,37 %). Они могут быть разделены с помощью химического обмена или путем термической диффузии. Масса азота в виде искусственных радиоактивных изотопов находится в пределах 10-13 и 16-24. Наиболее стабильный период полураспада, равный 10 минутам. Первая искусственно индуцированная ядерная трансмутация была произведена в 1919 г. британским физиком Эрнестом Резерфордом, который, бомбардируя азот-14 альфа-частицами, получил ядра кислорода-17 и протоны.

Свойства
Напоследок перечислим основные свойства азота:
- Атомный номер: 7.
- Атомная масса азота: 14,0067.
- Температура плавления: -209,86 °C.
- Точка кипения: -195,8 °C.
- Плотность (1 атм, 0 °С): 1,2506 г азота на литр.
- Обычные состояния окисления: -3, +3, +5.
- Конфигурация электронов: 1s22s22p3.


























