Эрнест Резерфорд – это один из основателей фундаментального учения о внутреннем строении атома. Родился ученый в Англии, в семье эмигрантов из Шотландии. Резерфорд был четвертым ребенком в своей семье, при этом оказался самым талантливым. Особый вклад ему удалось внести в теорию строения атома.

Первоначальные представления о строении атома
Нужно отметить, что до того, как был проведен знаменитый опыт Резерфорда по рассеянию альфа-частиц, господствующей на то время идеей о строении атома была модель Томпсона. Этот ученый был уверен, что положительный заряд равномерно заполнял весь объем атома целиком. Отрицательно заряженные электроны, считал Томпсон, были будто бы вкраплениями в него.

Предпосылки к научному перевороту
После окончании школы Резерфорд как самый талантливый ученик получил грант в 50 фунтов для дальнейшего обучения. Благодаря этому он сумел поступить в колледж в Новой Зеландии. Далее молодой ученый сдает экзамены в Кентерберийском университете и начинает серьезно заниматься физикой и химией. В 1891 году Резерфорд сделал свой первый доклад на тему «Эволюция элементов». В нем впервые в истории была обозначена идея о том, что атомы представляют собой сложнейшие структуры.
Тогда в научных кругах господствовала идея Дальтона о том, что атомы неделимы. Всем, кто окружал Резерфорда, его идее показались совершенным безумием. Молодому ученому приходилось постоянно приносить извинения коллегам за свою «чепуху». Но через 12 лет Резерфорд все же сумел доказать свою правоту. У Резерфорда появился шанс продолжить свои исследования в Кавендишской лаборатории в Англии, где он начал изучать процессы ионизации воздуха. Первым открытием Резерфорда были альфа- и бета-лучи.
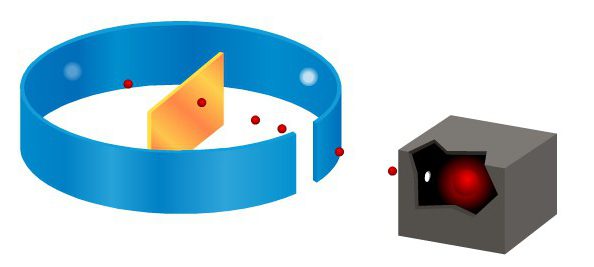
Опыт Резерфорда
Кратко об открытиии можно рассказать так: в 1912 году Резерфорд вместе со своими помощниками провел свой знаменитый опыт - альфа-частицы испускались из свинцового источника. Все частицы, кроме тех, что оказывались поглощенными свинцом, двигались вдоль установленного канала. Их узкий поток попадал на тонкий слой фольги. Эта линия была перпендикулярна листу. Опыт Резерфорда по рассеянию альфа-частиц доказал: те частицы, которые проходили сквозь лист фольги насквозь, вызывали так называемые сцинтилляции на экране.
Этот экран был покрыт особым веществом, которое начинало светиться при попадании на него альфа-частиц. Пространство между слоем золотой фольги и экраном было заполнено вакуумом для того, чтобы альфа-частицы не рассеивались в воздухе. Такой прибор позволил исследователям наблюдать частицы, рассеивающиеся под углом порядка 150°.
Если же фольгу не использовали в качестве препятствия перед пучком из альфа-частиц, то на экране образовывался светлый кружок из сцинтилляций. Но как только перед их лучом ставили барьер из золотой фольги, то картина сильно менялась. Вспышки появлялись не только вне этого кружка, но и на противоположной стороне фольги. Опыт Резерфорда по рассеянию альфа-частиц показал, что большинство частиц проходит через фольгу без заметных изменений в траектории движения.
При этом некоторые частицы отклонялись под довольно большим углом и даже отбрасывались назад. На каждые 10 000 свободно проходящих через слой золотой фольги частиц лишь одна отклонялась на угол, превышавший 10° - в виде исключения одна из частиц отклонялась на такой угол.

Причина, по которой отклонялись альфа-частицы
То, что детально рассмотрел и доказал опыт Резерфорда – строение атома. Такое положение свидетельствовало о том, что атом не представляет собой сплошное образование. Большинство частиц свободно проходили через фольгу толщиной в один атом. И поскольку масса альфа-частицы практически в 8 000 раз больше массы электрона, то последний не мог бы существенно повлиять на траекторию альфа-частицы. Это могло бы быть сделанным лишь атомным ядром – телом малых размеров, обладающим почти всей массой и всем электрическим зарядом атома. На тот момент это стало значительным прорывом английского физика. Опыт Резерфорда считается одной из важнейших ступеней в становлении науки о внутреннем строении атома.
Другие открытия, полученные в процессе изучения атома
Эти исследования стали прямым доказательством того, что положительный заряд атома находится внутри его ядра. Эта область занимает весьма малое пространство по сравнению с его целостными размерами. В таком малом объеме рассеяние альфа-частиц оказалось очень маловероятным. А те частицы, которые проходили вблизи области атомного ядра, испытывали резкие отклонения от траектории, ведь отталкивающие силы между альфа-частицей и ядром атома были очень мощными. Опыт Резерфорда по рассеянию альфа-частиц доказал вероятность того, что альфа-частица попадет прямо в ядро. Правда, вероятность была очень мала, но все же не равна нулю.
Это был не единственный факт, который доказал опыт Резерфорда. Кратко строение атома изучали и его коллеги, которые сделали ряд других важных открытий. Кроме учения о том, что альфа-частицы представляют собой быстро движущиеся ядра гелия.
Ученый смог описать строение атома, в котором ядро занимает незначительную часть всего объема. Его опыты доказали, что практически весь заряд атома сосредоточен внутри его ядра. При этом происходят как случаи отклонения альфа-частиц, так и случаи их столкновения с ядром.

Опыты Резерфорда: ядерная модель атома
В 1911 году Резерфорд после многочисленных исследований предложил модель строения атома, которую назвал планетарной. Согласно данной модели, внутри атома расположено ядро, которое содержит в себе практически всю массу частицы. Электроны движутся вокруг ядра подобно тому, как это делают планеты вокруг Солнца. Из их совокупности образуется так называемое электронное облако. Атом же имеет нейтральный заряд, как показал опыт Резерфорда.
Строение атома в дальнейшем заинтересовало ученого по имени Нильс Бор. Именно он доработал учение Резерфорда, ведь до Бора планетарная модель атома стала сталкиваться с трудностями объяснения. Так как электрон движется вокруг ядра по определенной орбите с ускорением, рано или поздно он должен упасть на ядро атома. Однако Нильс Бор смог доказать, что внутри атома законы классической механики уже не действуют.


























