Лимфатическая система человека выполняет ряд важных защитных функций, которые предупреждают развитие патогенных микроорганизмов или вирусов в жидких средах, клетках и тканях. За гуморальный иммунитет отвечают В-лимфоциты, которые при дальнейшем созревании синтезируют иммуноглобулины (Ig). Строение этих веществ позволяет находить, помечать и уничтожать пришедшие в организм антигены. В чем заключаются особенности молекул?
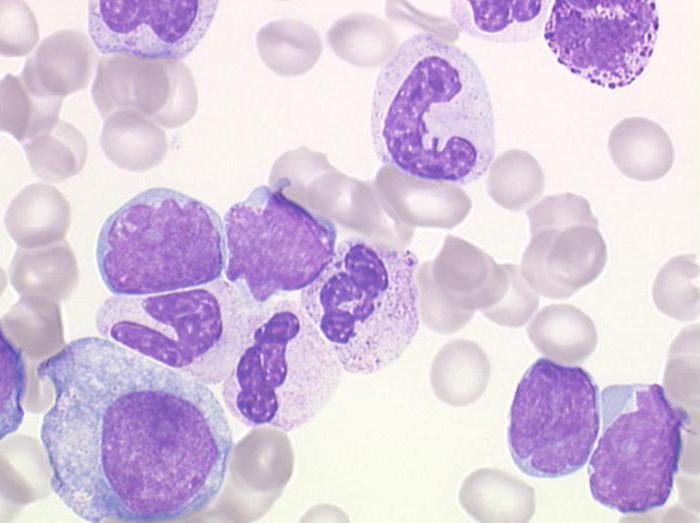
Плазматические клетки
Все лимфатические клетки организма человека делятся на две большие группы: Т-лимфоциты и В-лимфоциты. Первые отвечают за клеточный иммунитет, поглощая антигены в процессе фагоцитоза. Задача вторых заключается в синтезе специфических антител – гуморальный иммунитет.
В-лимфоциты детерминируются во вторичных лимфоидных органах (лимфатические узлы, селезенка), а затем формируют популяцию плазмоцитов, которые также называются плазматическими клетками. Они в дальнейшем мигрируют в красный костный мозг, слизистые оболочки и ткани.
Плазмоциты достигают больших размеров (до 20 мкм), окрашиваются базофильно, т. е. в фиолетовый цвет с помощью красителей. В центре этих клеток находится крупное ядро с характерными глыбками гетерохроматина, которые напоминают спицы колеса.
Цитоплазма окрашивается светлее, чем ядро. В ней располагается мощный транспортный центр, состоящий из эндоплазматической сети и аппарата Гольджи. АГ развит достаточно сильно, формируя так называемый светлый дворик клетки.
Все перечисленные структуры направлены на синтез антител, которые отвечают за гуморальный иммунитет. Строение молекулы иммуноглобулина имеет свои особенности, поэтому важно постепенное и качественное созревание этих структур в процессе синтеза.
Собственно, для этого и развита такая густая сеть ЭПС и аппарата Гольджи. Также генетический аппарат плазмоцитов, заключенный в ядре, направлен преимущественно на синтез белков антител. Зрелые плазматические клетки являются примером высокой степени детерминации, поэтому редко делятся.
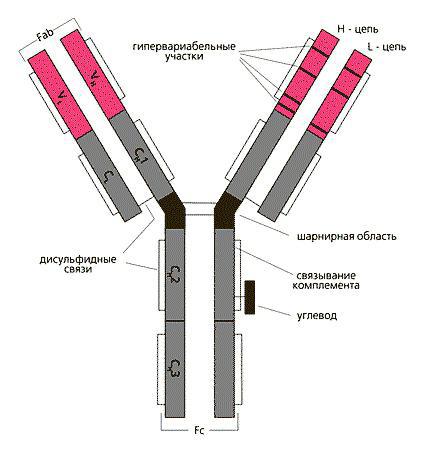
Строение антител иммуноглобулина
Эти высоко специализированные молекулы являются гликопротеидами, т. к. имеют белковую и углеводную части. Нас интересует скелет иммуноглобулинов.
Молекула состоит из 4 пептидных цепей: две тяжелые (Н-цепи) и две легкие (L-цепи). Они соединяются друг с другом с помощью дисульфидных связей, и в результате мы можем наблюдать форму молекулы, напоминающую рогатку.
Строение иммуноглобулинов направлено на соединение с антигенами с помощью специфических Fab-фрагментов. На свободных концах “рогатки” каждый такой участок образован двумя вариабельными доменами: одним от тяжелой и одним от легкой цепи. Каркасом служат постоянные домены (по 3 на каждой тяжелой и по одному на легких цепях).
Подвижность вариабельных концов иммуноглобулина обеспечивается наличием шарнирного участка в месте, где формируется дисульфидная связь между двумя Н-цепями. Так намного упрощается процесс взаимодействия антиген-антитело.
Остается нерассмотренным третий конец молекулы, который не взаимодействует с чужеродными молекулами. Он называется Fc-участком и отвечает за прикрепление иммуноглобулина к мембранам плазмоцитов и других клеток. Кстати, легкие цепи могут быть двух видов: каппа (κ) и лямбда (λ). Они соединены между собой дисульфидными связями.Также имеется пять видов тяжелых цепей, по которым классифицируют различные типы иммуноглобулинов. Это α-(альфа), δ-(дельта), ε-(эпсилон), γ-(гамма) μ- (мю) цепи.
Некоторые антитела способны образовывать полимерные структуры, которые стабилизируются за счет дополнительных J-пептидов. Так образуются димеры, тримеры, тетрамеры или пентомеры Ig определенного типа.
Еще одна дополнительная S-цепь характерна для секреторных иммуноглобулинов, строение и биохимия которых позволяют им функционировать в слизистых оболочках полости рта или кишечника. Эта дополнительная цепь предотвращает разрушение молекул антител природными ферментами.
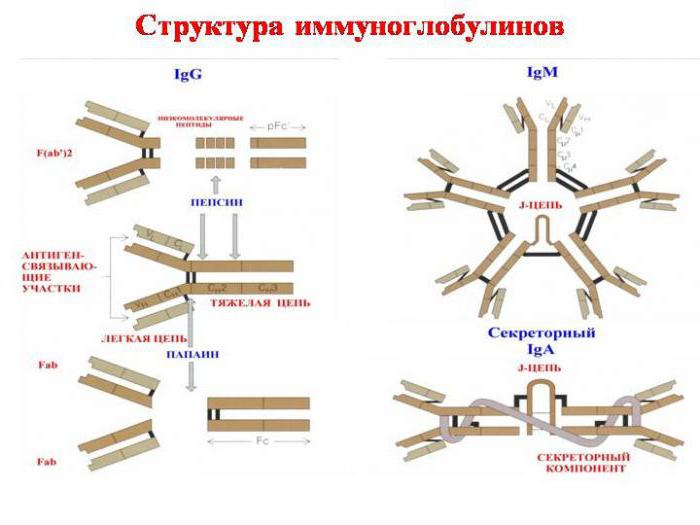
Строение и классы иммуноглобулинов
Разнообразие антител в нашем организме предопределяет вариабельность функций гуморального иммунитета. Каждый класс Ig имеет свои отличительные характеристики, по которым нетрудно догадаться об их роли в иммунной системе.
Строение и функции иммуноглобулинов напрямую зависят друг от друга. На молекулярном уровне они отличаются аминокислотной последовательностью тяжелой цепи, типы которой мы уже упомянули. Следовательно, выделяют 5 видов иммуноглобулинов: IgG, IgA, IgE, IgM и IgD.
Особенности иммуноглобулина G
IgG не образует полимеры и не встраивается в мембраны клеток. В составе молекул выявлено присутствие гамма-тяжелой цепи.
Отличительной чертой этого класса является тот факт, что только данные антитела способны проникать через плацентарный барьер и формировать иммунную защиту зародыша.
IgG составляет 70-80 % всех сывороточных антител, поэтому молекулы легко обнаруживаются лабораторными методами. В крови 12 г/л – среднее содержание этого класса, и такой показатель обычно достигается уже к 12 годам.
Строение иммуноглобулина G позволяет выполнять следующие функции:
- Нейтрализация токсинов.
- Опсонизация антигенов.
- Запуск комплемент-опосредованного цитолиза.
- Презентация антигена клеткам-киллерам.
- Обеспечение иммунитета новорожденного.
Иммуноглобулин А: особенности и функции
Этот класс антител встречается в двух формах: сывороточной и секреторной.
В сыворотке крови IgA составляет 10-15 % всех антител, а его среднее количество составляет 2,5 г/л к 10-летнему возрасту.
Больше нас интересует секреторная форма иммуноглобулина А, т. к. около 60 % молекул данного класса антител сосредоточены в слизистых оболочках организма.
Строение иммуноглобулина А также отличается своей вариативностью за счет наличия J-пептида, который может участвовать в образовании димеров, тримеров или тетрамеров. За счет этого один такой комплекс антител способен связывать большое количество антигенов.
Во время образования IgA к молекуле присоединяется еще один компонент – S-белок. Его главной задачей является защита всего комплекса от разрушительного действия ферментов и других клеток лимфатической системы человека.
Иммуноглобулин А содержится в слизистых оболочках желудочно-кишечного тракта, мочеполовой системы и дыхательных путей. Молекулы IgA обволакивают антигенные частицы, тем самым препятствуя их адгезии на стенках полых органов.
Функции этого класса антител следующие:
- Нейтрализация антигенов.
- Являются первым барьером среди всех молекул гуморального иммунитета.
- Опсонируют и маркируют антигены.
Иммуноглобулин М
Представители класса IgM выделяются большими размерами молекулы, т. к. их комплексы являются пентамерами. Всю конструкцию поддерживает J-белок, а каркасом молекулы являются тяжелые цепи ню-типа.
Пентамерная структура характерна для секреторной формы этого иммуноглобулина, однако существуют и мономеры. Последние крепятся к мембранам В-лимфоцитов, тем самым помогая клеткам обнаруживать патогенные элементы в жидкостях организма.
Всего 5-10 % составляет IgM в сыворотке крови, а его содержание в среднем не превышает 1 г/л. Антитела данного класса являются самыми древними в эволюционном плане, а синтезируются они только В-лимфоцитами и их предшественниками (плазмоциты на это не способны).
Количество антител М повышается у новорожденных, т.к. это является фактором интенсивной секреции IgG. Такая стимуляция положительно влияет на развитие иммунитета младенца.
Строение иммуноглобулина М не позволяет проникать через плацентарные барьеры, поэтому обнаружение этих антител в жидкостях плода становится сигналом о нарушении обменных механизмов, инфекции или дефекте плаценты.
Функции IgM:
- Нейтрализация.
- Опсонизация.
- Активация комплемент-зависимого цитолиза.
- Формирование иммунитета новорожденного.

Особенности иммуноглобулина D
Данный вид антител изучен достаточно мало, поэтому их роль в организме до конца не выяснена. Встречаются IgD только в виде мономеров, в сыворотке крови эти молекулы составляют не больше 0,2 % от всех антител (0,03 г/л).
Основная функция иммуноглобулина D – это рецепция в составе мембраны В-лимфоцитов, однако только 15 % всей популяции этих клеток имеют IgD. Прикрепляются антитела с помощью Fc-конца молекулы, а тяжелые цепи относятся к дельта-классу.
Строение и функции иммуноглобулина Е
Этот класс составляет незначительную долю всех антител сыворотки крови (0,00025 %). IgE, он же реагин, обладают высокой цитофильностью: мономеры этих иммуноглобулинов прикрепляются к мембранам тучных клеток и базофилов. В результате IgE влияет на выработку гистамина, который приводит к развитию воспалительных реакций.
В строении иммуноглобулина Е присутствуют тяжелые цепи эпсилон-типа.
Из-за малого количества эти антитела очень сложно обнаруживаются лабораторными методами в сыворотке крови. Повышенное содержание IgE является важным диагностическим признаком возникновения аллергических реакций.

Выводы
Строение иммуноглобулинов напрямую влияет на их функции в организме. Гуморальный иммунитет играет большую роль в поддержании гомеостаза, поэтому все антитела должны работать четко и слаженно.
Содержание всех классов Ig строго определено для человека. Любые изменения, зафиксированные в лаборатории, могут быть поводом для развития патологических процессов. Этим и пользуются врачи в своей практике.





























