Рестриктазы — это особые ферменты, способные разрезать цепочки ДНК в строго определенных местах. Именно в специфичности действия заключается главное отличие данной группы белков от других видов эндонуклеаз. Благодаря этому уникальному свойству ферменты рестрикции нашли широкое применение в генной инженерии.
Рестриктазы — это уникальные ферменты бактерий. Впервые эти белки были выделены в 1968 году из штаммов Esherihia colli. Дальнейшие исследования выявили присутствие эндонуклеаз рестрикции в одноклеточной водоросли Chlorella, а также в нескольких культурах дрожжей Sachoromyces и Pichia. В клетках других эукариотов рестриктазы пока не обнаружены.
Общая характеристика
Рестриктазы — ферменты, относящиеся к группе гидролаз, поскольку катализируют гидролиз фосфодиэфирной связи между нуклеотидами в цепочке ДНК. Место, в котором происходит разрезание, называется сайтом рестрикции. Последний может находиться как внутри опознаваемой последовательности, так и на расстоянии от нее.
Специфичный для рестриктазы участок распознавания обычно состоит из 4-8 нуклеотидов. Так как азотистые основания обращены внутрь двойной спирали, фермент находит нужную последовательность за счет взаимодействия с большой бороздкой ДНК.
Каждая рестриктаза имеет свой сайт распознавания и может функционировать только после связывания с ним.
Биологическая роль
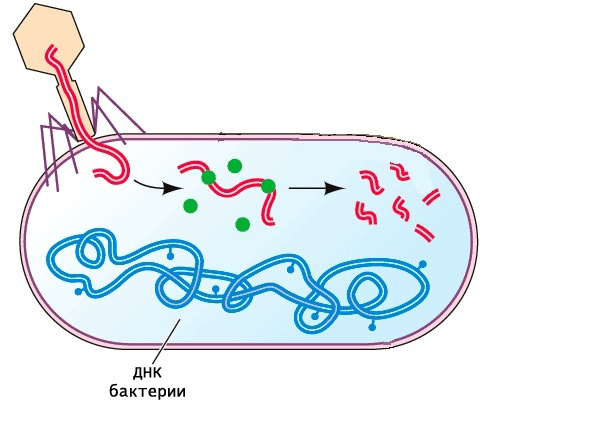
Бактерии рестриктазы — это важнейший инструмент защиты клетки от бактериофагов. Основная задача ферментов данной группы состоит в разрезании проникшего в клетку чужеродного генетического материала. Фрагментирование нуклеиновой кислоты препятствует ее репликации, а значит, и размножению вируса.
Последовательности, к которым специфичны рестриктазы, с определенной периодичностью встречаются в геноме самой бактерии и потому подвергаются метилированию, которое не позволяет рестриктазам распознать свои мишени. Этот процесс осуществляется ферментами метилазами.
Механизм, направленный на разрезание чужеродной ДНК и защищающий от нуклеазной активности собственную, называется системой рестрикции-модификации. Некоторые типы рестриктаз способны проявлять как эндонуклеазную, так и метилазную активность.
На настоящий момент известно более 1000 бактериальных рестриктаз. Очень часто они рассматриваются не как отдельные ферменты, а в комплексе систем рестрикции-модификации.
Особенности действия рестриктаз
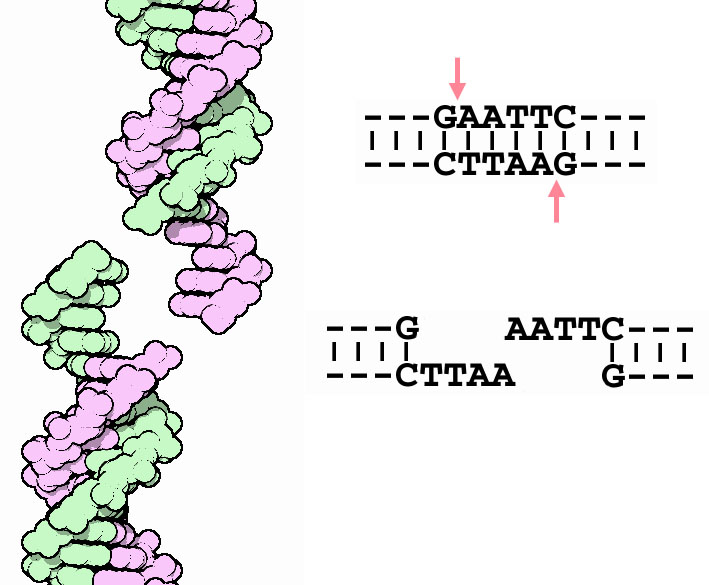
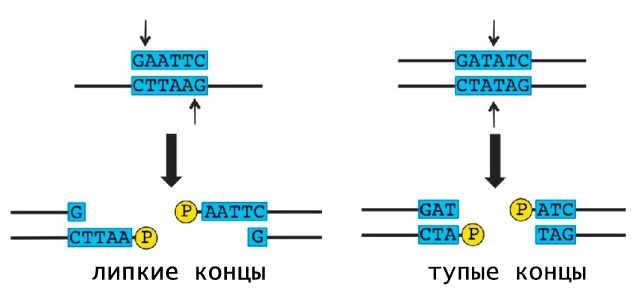
После связывания с последовательностью распознавания эндонуклеаза рестрикции поочередно расщепляются цепи ДНК. При этом могут образовываться два варианта концов:
- Липкие — одноцепочечные комплементарные друг другу последовательности, которые легко могут "сшиться" обратно. Формируются при ступенчатой траектории разрезания, когда точки расщепления двух цепей не совпадают;
- Тупые — одноцепочечные участки в месте разрыва ДНК не образуются, точки разрезания цепей находятся напротив друг друга.
Для осуществления эндонуклеазной активности рестриктазам требуется кофактор в виде Mg2+. Расположившись на месте разрыва этот ион вмешивается в конфигурацию ДНК, что способствует последующему расщеплению.
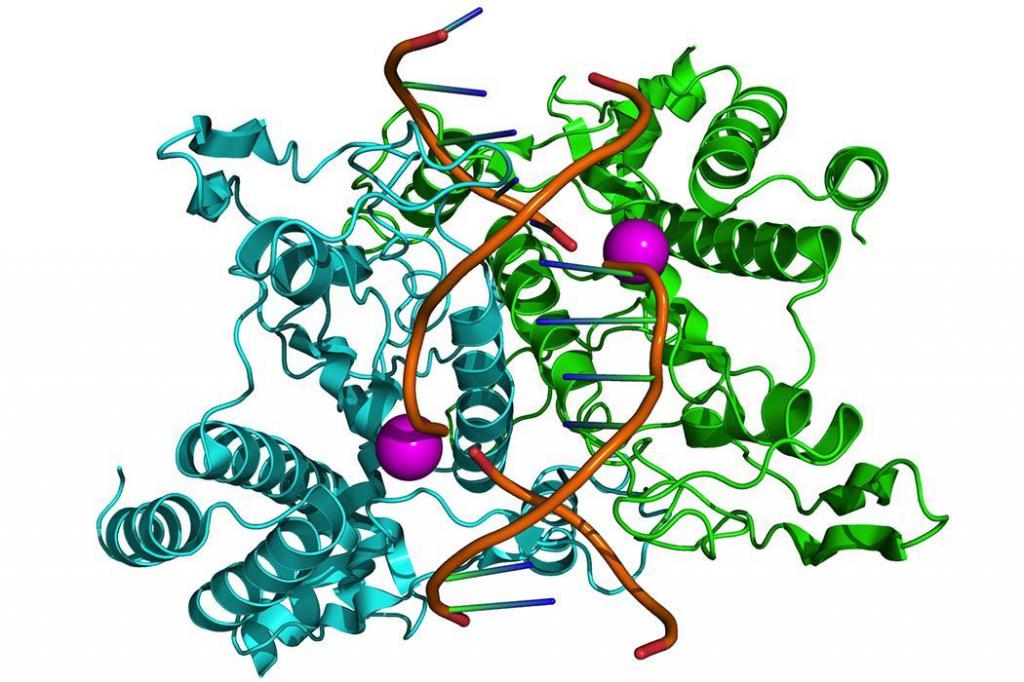
Классификация рестриктаз
По строению и механизму действия все рестриктазы разделяют на 2 класса. К первому относятся ферменты, обладающие исключительно рестрикционной активностью, а метилирование осуществляется другим белком с аналогичной субстратной специфичностью.
Рестриктазы класса II представляют собой мультиферментные комплексы, способные как разрезать, так и модифицировать ДНК. Эти белки состоят из 3 функциональных субъединиц:
- сайт-узнающей;
- метилирующей;
- рестриктирующей.
Есть и другая разновидность рестриктаз того же класса, для которой характерна структура из двух субъединиц. Такие ферменты называют бифункциональными.
Метилазная и эндонуклеазная активности у разных рестриктаз могут осуществляться одновременно, либо исключать друг друга. Эффект действия таких ферментов зависит от условий реакции.
В пределах двух классов выделят три типа рестиктаз (I, II и III), которые различаются по следующим характеристикам:
- структурная организация;
- выполняемые функции;
- особенности субстратной специфичности;
- потребность в кофакторах;
- расположение сайта рестрикции относительно участка распознавания;
- обратимость реакции рестрикционного гидролиза;
- потребность в энергии АТФ;
- механизм действия.
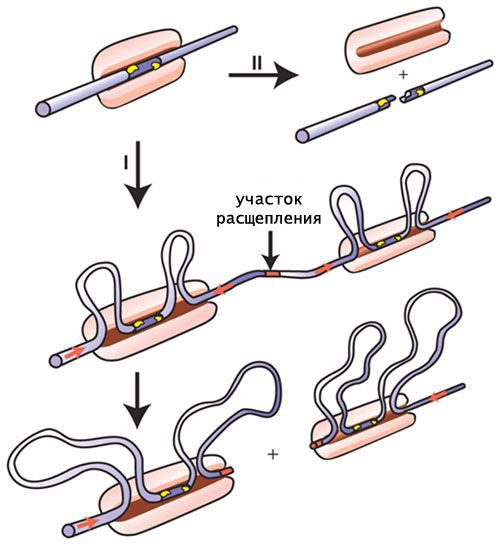
Тип II соответствует первому классу эндонуклеаз рестрикции, а первый и третий типы являются разновидностями класса II.
| Тип | I | II | III |
| Структура | 3 разные субъединицы | Одна или несколько идентичных субъединиц | 2 различные субъединицы |
| Функции | Рестрикция и метилирование | Рестрикция | Рестрикция и метилирование |
| Реакции гидролиза и метилирования | Взаимоисключающие | Отдельные реакции (для каждой свой фермент) | Возможно одновременное проявление |
| Расположение сайта разрезания | Случайное, не менее 1000 пар нуклеотидов от распознаваемой последовательности | Внутри распознаваемой последовательности | На расстоянии 24-26 нуклеотидных пар от последовательности распознавания |
| Кофакторы рестрикции | S-анедозил-L-метионин (Адо-мет), Mg2+, АТФ | Mg2+ | Mg2+, АТФ (необходимы); Адо-мет (необязателен, стимулирует реакцию) |
| Кофакторы метилирования | Адо-мет (необходим); Mg2+ и АТФ (стимулируют реакцию) | нет метилирования | Адо-мет (необходим); Mg2+ и АТФ (стимулируют реакцию) |
| Энзиматическая обратимость рестриктазной реакции | Есть | Нет | Нет |
| Последовательность распознавания | Прерывистая, вращательная симметрия отсутствует | Короткие последовательности, обладающие вращательной симметрией второго порядка | Последовательность имеет некоторые элементы симметрии либо полностью лишена последней |
| Транслокация ДНК перед разрезанием | Есть | Нет | Нет |
Кроме трех основных разновидностей рестриктаз выделяют еще два типа:
- IIS — отличается от типа II тем, что система рестрикции-модификации кодируется не двумя, а тремя генами, а сайт разрезания находится вне последовательности распознавания (на фиксированном расстоянии);
- Mcr/Mrr — содержит несколько разных субъединиц при отсутствии модификационной активности, для работы требуется ГТФ, расщепляет ДНК с метилированными аденином и цитозином.
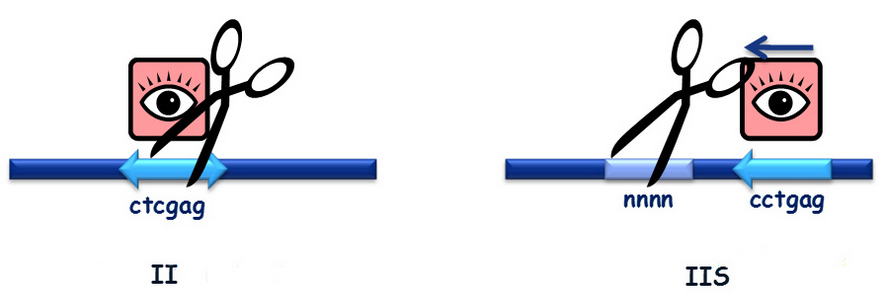
Рестриктазы первого и третьего типов характеризуются неполным гидролизом цепей ДНК и потому практически не используются в технологиях генной инженерии.
Номенклатура
Обычно в названии рестриктазы содержится информация о том, из какого микроорганизма она была выделена. При этом, информация указывается в следующем порядке:
- род и вид;
- штамм;
- номер фермента (если данный микроорганизм содержит несколько систем рестрикции-модификации).
Иногда в название включают информацию о локализации генов, кодирующих рестриктазу.
Номенклатура для рестрикционных ферментов была разработана Смиттом и Натансом. Она базируется на следующих принципах:
- Первая латинская буква обозначает род, а две последующие - вид микроорганизма.
- Далее латинской буковой указывается штамм или внехромосомный элемент, кодирующий рестриктазу.
- В конце римской цифрой обозначается номер фермента.
Таким образом, вторая по счету рестриктаза, выделенная из штамма d бактерии Haemophilus influenzae будет обозначаться HindII.
Изошизомеры
Существует еще одна классификация ферментов рестрикции, основывающаяся на их специфичности к субстрату.
Изошизомеры — это рестриктазы с разным происхождением, но одинаковой субстратной специфичностью. Такие рестриктазы могут быть выделены даже из отдаленных таксонов бактерий. Открытие изошизомеров опровергло предположение о строгой таксоноспецифичности рестриктаз, утверждавшее, что участки распознавания для этих ферментов у разных видов микроорганизмов уникальны.
Неошизомеры
Неошизомерами называются рестриктазы, имеющие общий участок распознавания, но разные сайты рестрикции. Например, для ферментов SmaI и XmaI специфична последовательность CCCGGG, но в одном случае разрезание проходит посередине (CCC/GGG), а в другом расщепляется связь между первым и вторым нуклеотидами (C/CCGGG).
Изокаудомеры
К изокаудомерам относят ферменты рестрикции с разной субстратной специфичностью, которые формируют одинаковые концы. Предполагается, что белки данной группы не являются родственными.
Применение рестриктаз
Рестриктазы являются одним из главных молекулярных инструментов, используемых в технологии рекомбинантных ДНК. Благодаря этим ферментам стало возможным вырезать из геномов различных организмов определенные фрагменты или гены, а затем сшивать их с помощью лигаз.
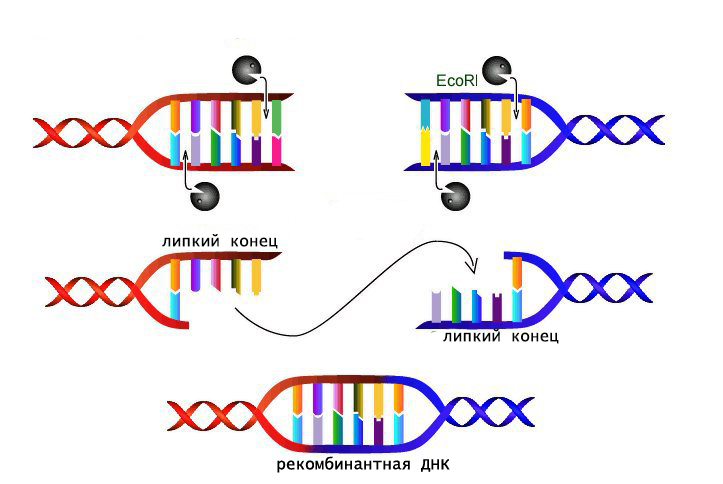
Особенно удобно использование в генной инженерии рестриктаз, образующих одинаковые липкие концы. Такие фрагменты ДНК легко соединяются по принципу комплементарности