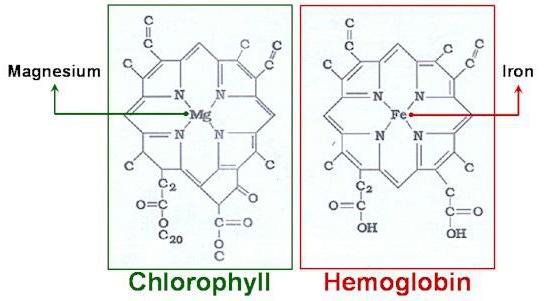
Самым большим и наиболее разнообразным среди неорганических веществ является класс комплексных соединений. К нему можно отнести и группу металлоорганических веществ, таких как хлорофилл и гемоглобин. Именно эти соединения являются тем мостом, который соединяет неорганическую и органическую химию в единую науку. Неоценима роль комплексных веществ в развитии знаний в области аналитической химии и кристаллохимии, в изучении важнейших биологических процессов: фотосинтеза, внутреннего (клеточного) дыхания.
В данной статье нами будут изучены строение и номенклатура комплексных соединений, а также рассмотрены основные принципы их классификации.
Координационная теория А. Вернера
В конце XX столетия швейцарский ученый А. Вернер доказал, что в молекуле любого комплексного вещества находятся несколько структур, которые были соответственно названы центральным ионом, лигандами (аддендами) и внешней координационной сферой. Чтобы нам стали ясны классификация и номенклатура комплексных соединений, разберем эти понятия более подробно. Итак, А. Вернером было доказано присутствие в молекуле иона (обычно положительно заряженного), занимающего центральное положение. Он стал именоваться комплексообразователем, центральным ионом или атомом. Вблизи него могут располагаться как нейтральные молекулы, называемые лигандами, так и отрицательно заряженные частицы-анионы, которые формируют внутреннюю координационную сферу вещества. Все оставшиеся частицы, не вошедшие в нее, образуют наружную оболочку молекулы.
Так, в формуле куприта натрия Na2[Cu(ОН)4], центральный атом меди в степени окисления +2 и четыре гидроксогруппы составляют внутреннюю сферу, а ионы натрия располагаются на некотором расстоянии от центрального атома во внешней сфере.
Методы определения координационных формул и названий веществ
До настоящего времени теория А. Вернера остается главной теоретической базой, на основе которой изучаются сложные комплексные соединения. Номенклатура, то есть названия этих веществ, определяются по правилам, принятым Международным обществом теоретической и прикладной химии.
Приведем несколько примеров формул веществ, в которых комплексообразователь представлен атомом платины - К2[PtCl6] или молекулами NH3 - [Ag(NH3)2]Cl. Как оказалось, формулы можно вывести с помощью следующих практических методов: реакциями двойного обмена, по молярной электропроводности растворов, рентгеноструктурным методом. Рассмотрим эти способы подробнее.
Как доказали структуру комплексных соединений платины
Вещества этой группы характеризуются присутствием в молекуле центрального атома платины. Если на соединение PtCl4×6NH3 подействовать раствором азотнокислого серебра, то весь хлор, присутствующий в веществе, связывается с атомами металла и образуются белые хлопья AgCl. Это значит, что все анионы хлора находились во внешней координационной сфере, тогда как молекулы аммиака были связаны с центральным атомом платины и совместно с ним образовали внутреннюю сферу.
Значит, координационная формула вещества будет записываться в таком виде: [Pt(NH3)6]Cl4 и называться хлорид гексаммин платины. Применяя рентгеноструктурный метод, химики изучили и другие комплексные соединения, номенклатура которых будет установлена нами в следующем разделе.
Кристаллические соединения хрома
Строение веществ этой группы было определено с помощью физического процесса дифракции рентгеновского излучения, лежащего в основе рентгеноструктурного анализа. Проходя через кристаллическую решетку, электромагнитные волны рассеиваются под действием злектронов исследуемого вещества. Это дает возможность очень точно установить, какие группы атомов находятся в узлах кристаллической решетки. Для хромсодержащих кристаллов была создана соответствующая номенклатура комплексных соединений. Примеры названий изомерных гидратов солей трехвалентного хрома, составленных с помощью рентгеноструктурного метода, будут следующими: хлорид тетрааквадихлорохрома (III), хлорид пентааквахлорохрома (III).
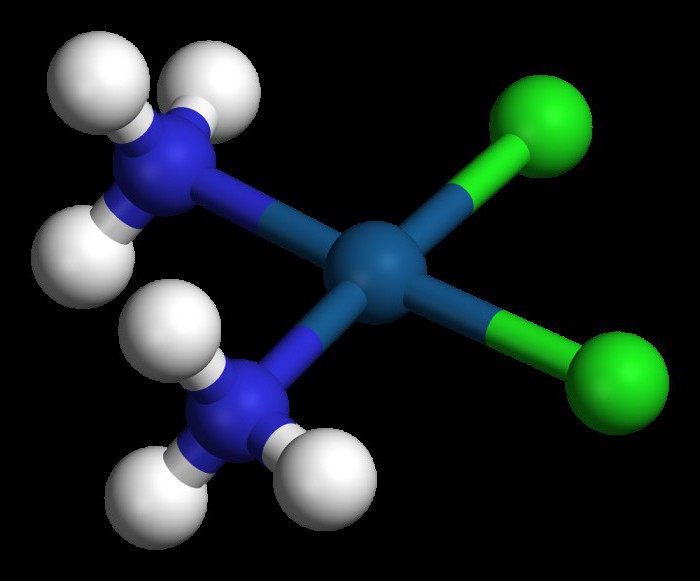
Было установлено, что в данных веществах атом хрома связан с шестью различными аддендами. Как же определяют этот показатель и какой фактор влияет на координационное число?
Как центральный атом связан с лигандами
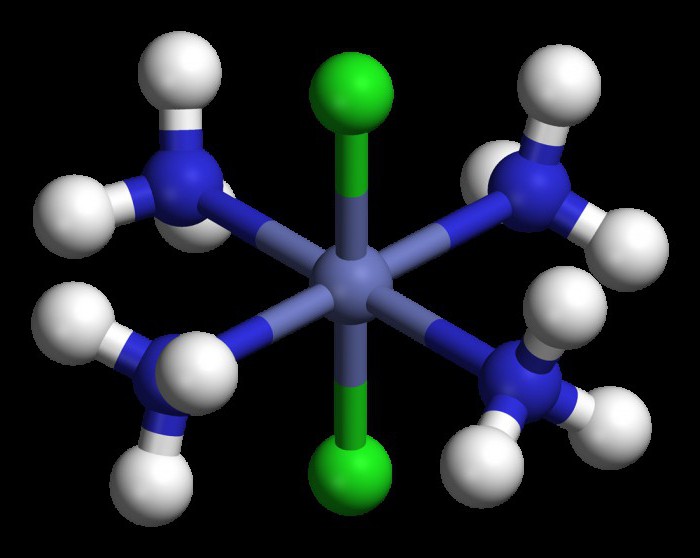
Чтобы ответить на вопрос, прозвучавший выше, вспомним, что в непосредственной близости от комплексообразователя находятся несколько структур, названных аддендами или лигандами. Их общее количество и определяет координационное число. Согласно теории А. Вернера, получение, классификация и номенклатура комплексных соединений напрямую зависят от этого показателя. Он же коррелятивно связан со степенью окисления центрального атома. В соединениях платины, хрома, железа координационное число чаще всего равно шести; если комплексообразователь представлен атомами меди или цинка – четырем, если центральным атомом является серебро или медь – двум.
Типы комплексных соединений
В химии различают как основные классы, так и переходные ряды веществ между ними. Рассмотренные в предыдущих подзаголовках комплексные соединения, номенклатура которых указывает на присутствие в их структуре молекул воды, относятся к аквакомплексам. К аммиакатам относят вещества, содержащие нейтральные частицы аммиака, например, трииод триамминродий. Своеобразен по строению молекул класс хелатных соединений. Их название происходит от биологического термина хелицеры – так называют клешни десятиногих раков. Эти вещества содержат адденды, пространственная конфигурация которых охватывает комплексообразователь, подобно клешням. К таким соединениям можно отнести оксалатный комплекс трехвалентного железа, этилендиамминовый комплекс платины со степенью окисления +4, соли аминоуксусной кислоты, в состав которых входят ионы родия, платины или меди.

Правила составления названий комплексных соединений
Наиболее часто встречающийся контрольный вопрос в заданиях по химии в курсе старшей школы звучит так: назовите комплексные соединения по ИЮПАК-номенклатуре. На конкретном примере разберем алгоритм составления названия вещества, имеющего такую формулу: (NH4)2[Pt(OH)2Cl4].
- Название начинают с определения состава внутренней координационной сферы. В ней находятся анионы гидроксильных групп и хлора. К их названиям прибавляем окончание –о. Получаем: дигидроксо-, тетрахлоро-.
- Теперь найдем комплексообразователь, используя для его обозначения латинское название, и прибавим к нему суффикс –ат, в круглых скобках укажем его степень окисления: платинат(IV).
- Закончив с обозначением внутренней сферы, перейдем к внешней части. Назовем ее катионы: в нашем примере это будут ионы аммония.
В итоге вещество будет иметь название, в котором указаны все вышеперечисленные структуры.
Применение комплексных соединений
В начале статьи мы называли важнейших представителей металлоорганических веществ, таких как гемоглобин, хлорофилл, витамины. Они играют ведущую роль в обмене веществ. Широко применяются комплексные соединения в технологических циклах выплавки черных и цветных металлов. Важную роль в металлургии играют карбонилы – особые комплексные соединения, номенклатура которых указывает на присутствие в их молекулах монооксида карбона СО в виде адденда. Эти соединения при нагревании разлагаются и восстанавливают такие металлы, как никель, железо, кобальт из их руд. Большинство комплексных соединений также используются как катализаторы в реакциях получения лаков, красок и пластмасс.


























