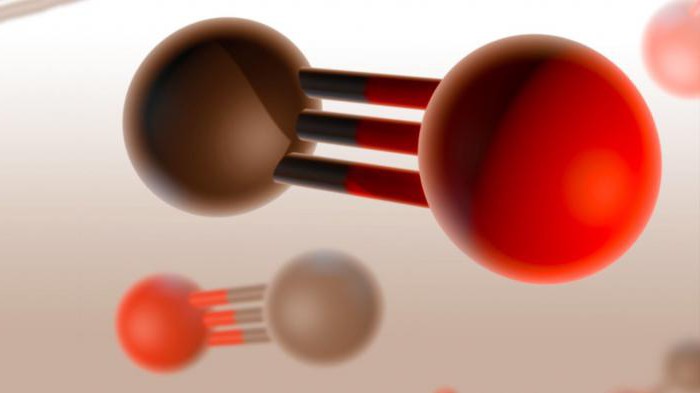
Монооксид углерода, также известный как угарный газ, имеет очень прочный молекулярный состав, является инертным по своим химическим свойствам и плохо растворяется в воде. Это соединение также невероятно токсично, при попадании в органы дыхания оно соединяется с гемоглобином крови, и тот перестает переносить кислород к тканям и органам.
Химические названия и формула
Монооксид углерода известен также под другими названиями, в том числе оксид углерода II. В быту его принято именовать угарным газом. Эта окись углерода является ядовитым бесцветным и безвкусным газом, не имеющим запаха. Его химическая формула - CO, а масса одной молекулы составляет 28,01 г/моль.

Воздействие на организм
Угарный газ соединяется с гемоглобином с образованием карбоксигемоглобина, который не имеет пропускной способности кислорода. Вдыхание его паров вызывает повреждение ЦНС (центральной нервной системы) и удушье. Результирующая нехватка кислорода вызывает головную боль, головокружение, снижение пульса и частоты дыхания, приводит к обмороку и последующей гибели организма.

Токсичный газ
Монооксид углерода получается путем частичного сгорания веществ, содержащих углерод, например, в двигателях внутреннего сгорания. В соединение входит 1 атом углерода, ковалентно связанный с 1 атомом кислорода. Угарный газ очень ядовит, и это один из наиболее распространенных причин смертельных отравлений во всем мире. Воздействие может привести к поражению сердца и других органов.

В чем польза угарного газа?
Несмотря на свою серьезную токсичность, монооксид углерода чрезвычайно полезен - благодаря современным технологиям из него создается целый ряд жизненно важных продуктов. Окись углерода хотя сегодня и считается загрязнителем, всегда присутствовала в природе, однако не в таком количестве, как, например, углекислый газ.
Ошибаются те, кто считает, что не существует соединения монооксид углерода в природе. CO растворяется в расплавленной вулканической породе при высоких давлениях в земной мантии. Содержание оксидов углерода в вулканических газах варьируется от менее 0,01% до 2%, в зависимости от вулкана. Поскольку природные этого соединения не являются величиной постоянной, точно измерить естественные выбросы газа не представляется возможным.

Химические свойства
Монооксид углерода (формула CO) относится к несолеобразующим или безразличным оксидам. Однако, при температуре +200 oС он вступает в реакцию с гидроксидом натрия. Во время этого химического процесса происходит образование формиата натрия:
NaOH + CO = HCOONa (соль муравьиной кислоты).
Свойства монооксида углерода основаны на его восстановительной способности. Монооксид углерода:
- может вступать в реакцию с кислородом: 2CO + O2 = 2CO2;
- способен взаимодействовать с галогенами: CO + Cl2 = COCl2 (фосген);
- имеет уникальное свойство восстанавливать чистые металлы из их оксидов: Fe2O3 + 3CO = 2Fe + 3CO2;
- образует карбонилы металлов: Fe + 5CO = Fe(CO)5;
- прекрасно растворяется в хлороформе, уксусной кислоте, этаноле, гидроксиде аммония и бензоле.
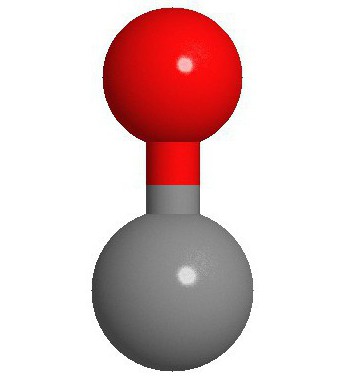
Структура молекулы
Два атома, из которых, собственно, и состоит молекула окиси углерода (СО), связаны между собой тройной связью. Две из них образованы путем слияния p-электронов атомов углерода с кислородом, а третья - благодаря особому механизму за счет свободной 2р-орбитали углерода и 2р-электронной пары кислорода. Такая структура обеспечивает молекуле высокую прочность.
Немного истории
Еще Аристотель из древней Греции описывал токсичные пары, производимые горящими углями. Сам механизм смерти известен не был. Однако одним из древних методов казни было запирание преступившего закон в парной, где находились тлеющие угли. Греческий врач Гален предположил, что в составе воздуха происходят определенные изменения, которые причиняют вред при вдыхании.
Во время Второй мировой войны газовая смесь с примесями монооксида углерода, была применена в качестве топлива для автотранспортных средств в тех частях мира, где было ограниченное количество бензина и дизельного топлива. Были установлены внешние (за некоторыми исключениями) генераторы древесного угля или древесного газа, а смесь атмосферного азота, моноксида углерода и небольшого количества других газов подавалась в газовый смеситель. Это был так называемый древесный газ.
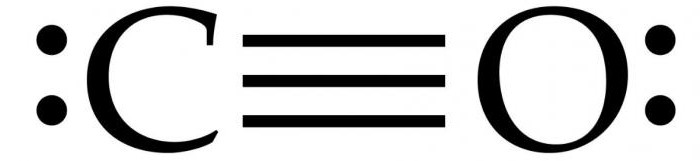
Окисление монооксида углерода
Окись углерода образуется при частичном окислении углеродсодержащих соединений. СО образуется, когда кислорода недостаточно для производства двуокиси углерода (CO2), например, при работе печи или двигателя внутреннего сгорания в замкнутом пространстве. Если присутствует кислород, а также некоторые другие атмосферные концентрации, окись углерода горит, излучая синий свет, образуя двуокись углерода, известную как углекислый газ.
Угольный газ, широко применяемый до 1960 годов прошлого века для внутреннего освещения помещений, приготовления пищи и отопления, имел СО в составе в качестве преимущественного компонента топлива. Некоторые процессы в современных технологиях, таких как выплавка железа, все еще производят монооксид углерода в качестве побочного продукта. Само соединение СО окисляется в СО2 при комнатной температуре.

Есть ли СО в природе?
Существует ли монооксид углерода в природе? Одним из его естественных по происхождению источников являются фотохимические реакции, происходящие в тропосфере. Эти процессы, как предполагается, способны генерировать около 5×1012 кг вещества е;егодно. Среди других источников, как уже было сказано выше, находятся вулканы, лесные пожары и другие виды горения.
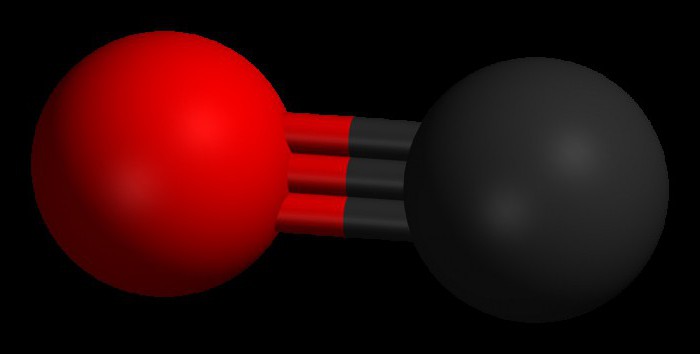
Молекулярные свойства
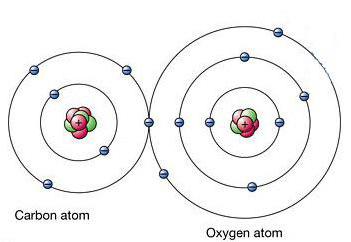
Монооксид углерода имеет молярную массу 28,0, что делает его немного менее плотным, чем воздух. Длина связи между двумя атомами - 112,8 микрометров. Это достаточно близко, что обеспечивает одну из самых сильных химических связей. Оба элемента в соединении СО вместе имеют около 10 электронов в одной валентной оболочке.
Как правило, в органических карбонильных соединениях возникает двойная связь. Характерной особенностью молекулы СО является то, что между атомами возникает прочная тройная связь с 6 общими электронами в 3 связанных молекулярных орбиталях. Поскольку 4 из общих электронов происходят от атома кислорода и только 2 от углерода, одна связанная орбиталь занята двумя электронами из О2, образуя дательную или дипольную связь. Это вызывает поляризацию C ← O молекулы с маленьким зарядом "-" на углероде и небольшим зарядом "+" на кислороде.
Остальные две связанные орбитали занимают одну заряженную частицу от углерода и одну от кислорода. Молекула является асимметричной: кислород имеет большую плотность электронов, чем углерод, и также слегка положительно заряжен по сравнению с отрицательным углеродом.
Получение
В промышленности получение монооксид углерода СО осуществляется путем нагревания без доступа воздуха углекислого газа или водяных паров с углем:
СО2 + С = 2СО;
Н2О + С = СО + Н2.
Последнюю получившуюся смесь еще называют водяным или синтез-газом. В лабораторных условиях оксид углерода II путем воздействия на органические кислоты концентрированной серной кислоты, которая выступает в качестве водоотнимающего средства:
НСООН = СО + Н2О;
Н2С2О4 = СО2 + Н2О.
Основные симптомы и помощь при отравлении СО
Вызывает ли монооксид углерода отравление? Да, и очень сильное. Отравление угарным газом является наиболее частым явлением во всем мире. Наиболее распространенные симптомы:
- чувство слабости;
- тошнота;
- головокружение;
- усталость;
- раздражительность;
- плохой аппетит;
- головная боль;
- дезориентация;
- нарушение зрения;
- рвота;
- обморок;
- судороги.
Воздействие этого токсичного газа может привести к значительным повреждениям, которые зачастую могут привести к длительными хроническим патологическим состояниям. Монооксид углерода способен причинить серьезный ущерб плоду беременной женщины. Пострадавшим, например, после пожара, следует оказать незамедлительную помощь. необходимо срочно вызвать скорую помощь, дать доступ свежего воздуха, убрать стесняющую дыхание одежду, успокоить, согреть. Сильное отравление, как правило, лечится только под присмотром врачей, в стационаре.
Применение
Угарный газ, как уже было сказано, ядовит и опасен, однако он является одним из базовых соединений, которые применяются в современной промышленности для органического синтеза. СО используют для получения чистых металлов, карбонилов, фосгена, сероокиси углерода, метилового спирта, формамида, ароматических альдегидов, муравьиной кислоты. Это вещество также применяется в качестве горючего. Несмотря на его токсичность и ядовитость, его часто используют в качестве сырья для получения различных веществ в химической промышленности.
Угарный газ и углекислый газ: в чем разница?
Монооксид и диоксид углерода (СО и CO2) часто ошибочно принимают друг за друга. Оба газа без запаха и цвета, и оба негативно воздействуют на сердечно-сосудистую систему. Оба газа могут проникать в организм через вдыхание, кожу и глаза. Эти соединения при воздействии на живой организм имеют ряд общих симптомов - головные боли, головокружение, судороги и галлюцинации. Большинство людей с трудом определяют разницу и не понимают, что выхлопные газы автомобилей испускают как CO, так и CO2 . В помещении увеличение концентрации этих газов может быть опасным для здоровья и безопасности человека, подверженного их воздействию. В чем же разница?
При высоких концентрациях оба могут быть смертельными. Разница заключается в том, что CO2 является общим природным газом, необходимым для всей растительной и животной жизни. CO не является обычным явлением. Это побочный продукт бескислородного сжигания топлива. Критическое химическое различие заключается в том, что CO2 содержит один атом углерода и два атома кислорода, тогда как у CO их всего по одному. Углекислый газ является негорючим, в то время как монооксид имеет большую вероятность к воспламенению.
Двуокись углерода, естественно, встречается в атмосфере: люди и животные дышат кислородом и выдыхают углекислый газ, то есть живые существа способны выдерживать его в небольшом количестве. Этот газ необходим также для осуществления растениями фотосинтеза. Однако монооксид углерода не возникает естественным образом в атмосфере и может вызвать проблемы со здоровьем даже в низких концентрациях. Плотность обоих газов также различна. Углекислый газ тяжелее и плотнее воздуха, в то время как монооксид углерода немного легче. Эту их особенность стоит учитывать при установлении в домах соответствующих датчиков.