Ещё древние философы высказывали предположение, что материя строится из атомов. Однако о том, что сами «кирпичики» мироздания состоят из мельчайших частиц, учёные начали догадываться лишь на стыке XIX и XX веков. Опыты, доказывающие это, произвели в науке в своё время настоящую революцию. Именно количественное соотношение составных частей отличает один химический элемент от другого. Каждому из них отведено своё место в Периодической системе Менделеева согласно порядковому номеру. Но существуют разновидности атомов, занимающие в таблице одни и те же клетки, несмотря на различие в массе и свойствах. Почему это так и о том, что такое изотопы в химии, будет рассказано далее.

Атом и его частицы
Исследуя структуру материи посредством бомбардировки альфа-частицами, Э. Резерфорд доказал в 1910 году, что основное пространство атома заполнено пустотой. И только в центре находится ядро. Вокруг него по орбиталям двигаются отрицательные электроны, составляя оболочку этой системы. Так была создана планетарная модель «кирпичиков» материи.
Что такое изотопы? Вспомните из курса химии, что ядро тоже имеет сложное строение. Оно состоит из положительных протонов и не имеющих заряда нейтронов. Количество первых определяет качественные характеристики химического элемента. Именно число протонов отличает вещества друг от друга, наделяя их ядра определённым зарядом. И по этому признаку им присваивается порядковый номер в таблице Менделеева. Но количество нейтронов у одного и того же химического элемента дифференцирует их на изотопы. Определение в химии данному понятию поэтому можно дать следующее. Это разновидности атомов, отличающиеся по составу ядра, обладающие одинаковым зарядом и порядковым номеров, но имеющие разные массовые числа, ввиду различий в количестве нейтронов.

Обозначения
Изучая химию в 9 классе и изотопы, школьники узнают о принятых условных обозначениях. Буквой Z отмечается заряд ядра. Это цифра совпадает с количеством протонов и поэтому является их показателем. Сумма этих элементов с нейтронами, отмечаемыми значком N, составляет А – массовое число. Семейство изотопов одного вещества, как правило, обозначается значком того химического элемента, которых в таблице Менделеева наделяется порядковым номером, совпадающим с числом протонов в нём. Левый верхний индекс, добавляемый к указанному значку соответствует массовому числу. К примеру, 238U. Заряд элемента (в данном случае урана, отмеченного порядковым номером 92) обозначается похожим индексом снизу.
Зная эти данные, легко можно подсчитать количество нейтронов у данного изотопа. Оно равно массовому числу за вычетом порядкового номера: 238 – 92 = 146. Количество нейтронов могло бы быть меньше, от этого данный химический элемент не перестал бы оставаться ураном. Следует заметить, что чаще всего у других, более простых, веществ число протонов и нейтронов приблизительно совпадает. Подобные сведения помогают понять, что такое изотоп в химии.
Нуклоны
Индивидуальностью определённый элемент наделяет именно число протонов, а количество нейтронов на неё никаким образом не влияет. Но атомная масса составляется из этих двух указанных элементов, имеющих общее наименование «нуклоны», представляя собой их сумму. Однако этот показатель не зависит от числа электронов, формирующих отрицательно заряженную оболочку атома. Почему? Стоит только сравнить.
Доля массы протона в атоме велика и составляет приблизительно 1 а. е. м. или 1,672 621 898(21)·10-27кг. Нейтрон близок к показателям этой частицы (1,674 927 471(21)·10-27кг). А вот масса электрона в тысячи раз меньше, считается ничтожной и не учитывается. Вот почему, зная верхний индекс элемента в химии, состав ядра изотопов узнать несложно.
Изотопы водорода
Изотопы некоторых элементов настолько известны и распространены в природе, что получили собственные наименования. Ярким и наиболее простым примером тому может служить водород. В естественных условиях он содержится в своей самой распространённой разновидности протия. Этот элемент имеет массовое число 1, а ядро его состоит из одного протона.
Так что такое изотопы водорода в химии? Как известно, атомы этого вещества имеют первый номер в таблице Менделеева и соответственно наделены в природе зарядовым числом 1. Но количество нейтронов в ядре атома у них различно. Дейтерий, являясь тяжёлым водородом, помимо протона имеет в составе ядра ещё одну частицу, то есть нейтрон. В результате это вещество проявляет собственные физические свойства, в отличие от протия, обладая собственным весом, температурой плавления и кипения.
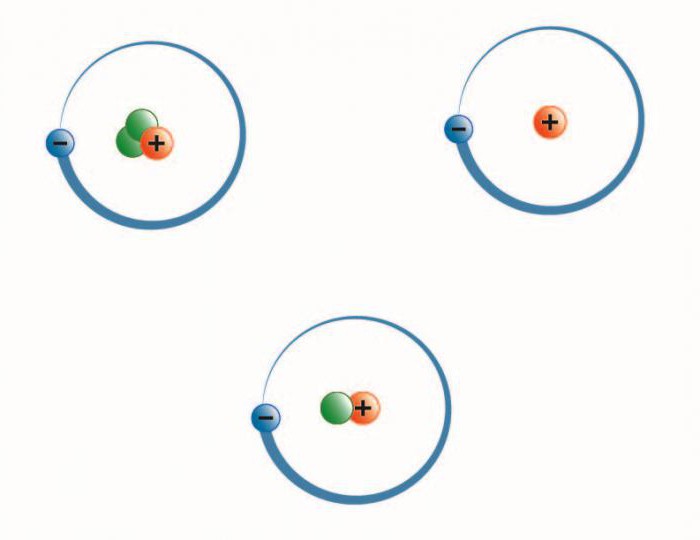
Тритий
Сложнее всех устроен тритий. Это сверхтяжёлый водород. В соответствии с определением изотопов в химии, он имеет зарядовое число 1, но массовое число 3. Его часто называют тритоном, потому что помимо одного протона, он имеет в составе ядра два нейтрона, то есть состоит из трёх элементов. Наименование этого элемента, открытого в 1934 году Резерфордом, Олифантом и Хартеком, было предложено ещё до его выявления.
Это неустойчивое вещество, проявляющее радиоактивные свойства. Ядро его обладает способностью расщепляться с выделение бета-частицы и электронного антинейтрино. Энергия распада данного вещества не очень велика и составляет 18,59 кэВ. Поэтому подобная радиация не является для человека слишком опасной. От неё способна защитить обыкновенная одежда и хирургические перчатки. А получаемый с пищей этот радиоактивный элемент быстро выводится из организма.
Изотопы урана
Гораздо опаснее оказываются различные типы урана, которых на сегодняшний день науке известно 26. Поэтому, рассказывая о том, что такое изотопы в химии, невозможно не упомянуть об этом элементе. Несмотря на разнообразие видов урана, в природе его изотопов встречается всего три. К ним относятся 234U, 235U, 238U. Первый из них, обладая подходящими свойствами, активно применяется как топливо в ядерных реакторах. А последний - для производства плутония-239, который сам, в свою очередь, незаменим как ценнейшее топливо.
Каждый из радиоактивных элементов характеризуется собственным периодом полураспада. Это отрезок времени, в течение которого вещество расщепляется в отношении ½. То есть в результате этого процесса количество сохранившейся части вещества вдвое уменьшается. Этот отрезок времени для урана огромен. К примеру, для изотопа-234 он исчисляется в 270 тысячелетий, а для двух других указанных разновидностей он гораздо значительнее. Рекордный период полураспада - у урана-238, продолжающийся миллиарды лет.

Нуклиды
Не каждый из видов атома, характеризующихся собственным и строго определённым числом протонов и электронов, настолько стабилен, чтобы существовать хоть сколько-нибудь продолжительный период, достаточный для его изучения. Те из них, которые обладают относительной устойчивостью, называются нуклидами. Стабильные образования такого рода радиоактивному распаду не подвергаются. Нестабильные называются радионуклидами и тоже, в свою очередь, делятся на короткоживущие и долгожители. Как известно из уроков химии 11 класса о строении атомов изотопов, наибольшим числом радионуклидов обладают осмий и платина. По одному стабильному имеют кобальт и золото, а наибольшее количество устойчивых нуклидов у олова.
Вычисление порядкового номера изотопа
Теперь постараемся обобщить сведения, описанные ранее. Поняв, что такое изотопы в химии, пришло время выяснить, как можно использовать полученные знания. Рассмотрим это на конкретном примере. Допустим, известно, что некоторый химический элемент обладает массовым числом 181. При этом оболочка атома данного вещества содержит в себе 73 электрона. Как можно, воспользовавшись таблицей Менделеева, узнать название данного элемента, а также число протонов и нейтронов в составе его ядра?
Приступим к решению задачи. Определить наименование вещества можно, зная его порядковый номер, который соответствует количеству протонов. Так как число положительных и отрицательных зарядов в атоме равны, то оно составляет 73. Значит, это тантал. При том, общее количество нуклонов в сумме составляет 181, а значит, протонов у данного элемента 181 – 73 = 108. Достаточно просто.
Изотопы галлия
Элемент галлий в периодической системе имеет порядковый номер 71. В природе у этого вещества есть два изотопа - 69Ga и 71Ga. Как определить процентное соотношение разновидностей галлия?
Решение задач на изотопы по химии почти всегда связано с информаций, которую можно получить из таблицы Менделеева. В этот раз следует поступить аналогичным образом. Определим из указанного источника среднюю атомную массу. Она равна 69,72. Обозначив за x и y количественное соотношение первого и второго изотопа, примем сумму их равной 1. А значит, в виде уравнения это запишется: x + y = 1. Отсюда следует, что 69x + 71y = 69,72. Выразив y через x и подставив первое уравнение во второе, получаем, что x = 0,64, а y = 0,36. Это значит, что 69Ga содержится в природе 64 %, а процентное соотношение 71Ga составляет 34 %.
Превращения изотопов
Радиоактивное расщепление изотопов с трансформацией их в другие элементы разделяется на три основных типа. Первым из них является альфа-распад. Он происходит с испусканием частицы, представляющей собой ядро атома гелия. То есть это образование, состоящие из совокупности пар нейтронов и протонов. Поскольку количество последних определяет зарядовое число и номер атома вещества в периодической системе, то в результате этого процесса происходит качественное превращение одного элемента в другой, а в таблице он сдвигается влево на две клетки. При этом массовое число элемента уменьшается на 4 единицы. Это мы знаем из разделов химии о строении атомов изотопов.
При потере ядром атома бета-частицы, по сути представляющей собой электрон, меняется его состав. Один из нейтронов трансформируется в протон. Это значит, что качественные характеристики вещества вновь меняются, а элемент сдвигается в таблице на одну клетку вправо, практически не теряя при этом в массе. Обычно подобное превращение сопряжено с электромагнитным гамма-излучением.
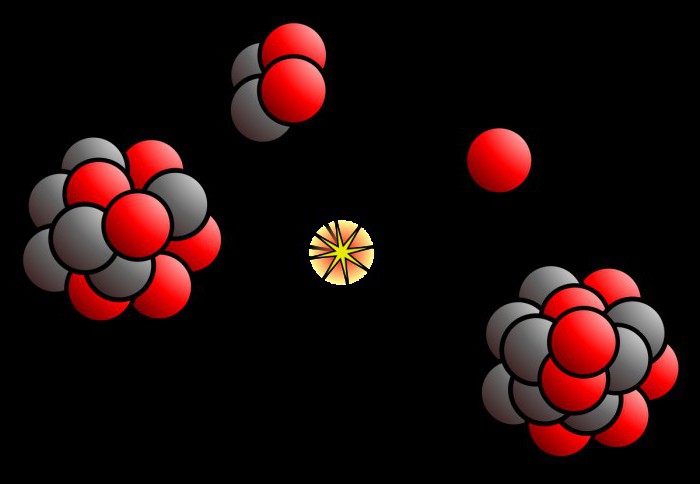
Превращение изотопа радия
Вышеизложенные сведения и знания из химии 11 класса об изотопах снова помогают решать практические задачи. К примеру, следующие: 226Ra при распаде превращается в химический элемент IV группы, обладающий массовым числом 206. Сколько альфа- и бета-частиц при этом он должен потерять?
Учитывая изменения в массе и группу дочернего элемента, воспользовавшись таблицей Менделеева, легко определить, что образовавшимся при расщеплении изотопом будет свинец с зарядом 82 и массовым числом 206. А учитывая зарядовое число этого элемента и исходного радия, следует предположить, что ядро его потеряло пять альфа-частиц и четыре бета-частицы.
Использование радиоактивных изотопов
Всем прекрасно известно, какой вред живым организмам может нанести радиоактивное излучение. Однако свойства радиоактивных изотопов бывают для человека полезны. Они с успехом применяются во многих отраслях промышленности. С их помощью возможно обнаружить утечку в инженерных и строительных сооружениях, подземных трубопроводах и нефтепроводах, накопительных баках, теплообменниках на электростанциях.
Указанные свойства активно используются также в научных экспериментах. К примеру, муха цеце является переносчиком многих серьёзных заболеваний для человека, скота и домашних животных. В целях предотвращения подобного самцов этих насекомых стерилизуют посредством слабого радиоактивного излучения. Изотопы также бывают незаменимы при изучении механизмов некоторых химических реакций, ведь атомами данных элементов можно метить воду и другие вещества.
При биологических исследованиях часто также используются меченые изотопы. К примеру, именно таким образом было установлено, как фосфор влияет на почву, рост и развитие культурных растений. С успехом свойства изотопов применяются и в медицине, что позволило лечить раковые опухоли и другие тяжёлые заболевания, определять возраст биологических организмов.


























