Одно и то же химическое соединение имеет постоянный состав, вне зависимости от места и способа получения образца. К такому выводу одним из первых пришел основатель современной химии, французский ученый А. де Лавуазье. Он сумел определить состав воды, воздуха, органических веществ, считал, что частицы входят в состав веществ в определенных пропорциях. Позже другим химиком из Франции Ж. Л. Прустом был сформулирован закон постоянства состава. Оба исследователя немало сил приложили, чтобы отстоять свои идеи в споре с научным сообществом.

Взгляды на строение вещества на рубеже XVIII и XIX веков
Химические элементы, соединяясь друг с другом в разных соотношениях, образуют множество веществ. Каждое из них характеризуется определенным набором атомов и соотношением их масс. Но до конца XVIII столетия многие ученые считали иначе. Проблема для них заключалась в неточности количественных методик. К тому же позиции атомно-молекулярных воззрений в то время были зыбкими, господствовала теория флогистона — мифического элемента. В установление количественного состава вещества значительный вклад внесли:
- А. де Лавуазье;
- М. В. Ломоносов;
- Ж. Л. Пруст;
- Д. Дальтон.
Заслуга Ж. Л. Пруста заключается в том, что он усовершенствовал количественные методы Лавуазье, строго им следовал. Ученый предложил закон постоянства состава, сохранения соотношений элементов в образцах соединений. Работу в этом направлении Пруст начал еще в конце XVIII века, но признание его труды получили только в 1808 году. Джон Дальтон примерно в это же время ввел представление об атомах и массах этих частиц, кратных соотношениях.
Биография Ж. Л. Пруста

Закон постоянства состава. Примеры
Ж. Л. Пруст открыл глюкозу, прославился блестящей победой в научной полемике с соотечественником Бертолле, причиной которой стал закон постоянства состава. Формулировка, предложенная Прустом, гласит: когда несколько элементов образуют химически чистый образец, то он состоит из одних и тех же атомов. Отношения их масс и числа также носят постоянный характер. Примеры:
- Хлорид натрия (NaCl) можно получить при взаимодействии соляной кислоты с гидроксидом натрия. Второй способ — обработка соляной кислотой карбоната натрия. В двух разных химических реакциях получаем соединение, формула которого NaCl. И в первом, и во втором случае вещество содержит 39,33% натрия и 60,66% хлора.
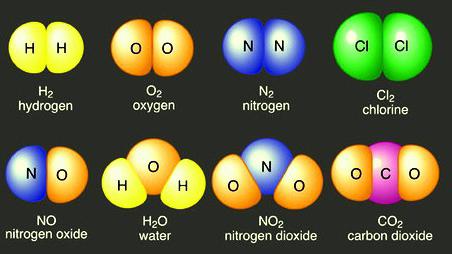
- Кислород (химический знак O) при образовании молекулы воды соединяется с одним и тем же количеством водорода (H). Если взаимодействует 1,11 г водорода с 8,89 г кислорода, то образуется 10 г воды (H2O). Увеличение количества одного из веществ приводит к такому же результату. Не прореагируют атомы того элемента, которого взяли в избытке. Масса воды в этом опыте остается такой же – 10 г, состав ее молекул отражает формула H2O.
Значение открытия постоянства состава
В начале XIX века в теоретической химии утвердились законы, которые соединяют вещества, описывают их соотношения. Изучали качественные и количественные характеристики многие ученые, предложившие универсальные формулировки. Основополагающими были идеи М. В. Ломоносова о сохранении массы в химических превращениях. Установленный Ж. Л. Прустом закон постоянства состава также имеет большое значение для науки и практики. На основании этой закономерности формулу воды записывают только в виде H2O, а состав серной кислоты – H2SO4. Но закон Пруста не имеет такого всеобъемлющего характера, как учение Ломоносова. Поэтому его формулировку уточнили после открытия изотопов. Так называют атомы одного и того же элемента, имеющие разную массу. Соотношение частиц в составе образца является постоянной величиной, но только при условии неизменного изотопного состава. Например, массовый состав водорода и кислорода в обычной и тяжелой воде отличается. Вторая жидкость содержит изотоп водорода — дейтерий. Масса тяжелой воды больше, чем обычной.
Современные взгляды на состав вещества

В соответствии с формулировкой Пруста соотношение масс атомов, составляющих определенное вещество, носит постоянный характер, не зависит от способа получения образца. В начале XX столетия при изучении сплавов металлов были открыты соединения с переменным составом. В этом случае единице веса одного химического элемента могут соответствовать различные массы другого элемента. Например, в соединениях таллия с висмутом на единицу массы первого приходится от 1,2 до 1,8 единицы веса второго элемента. Такие примеры можно найти среди интерметаллических веществ, оксидов, соединений серы, азота, углерода, водорода с металлами. Следовательно, законы, открытые Прустом и Дальтоном, справедливы полностью только в отношении тех веществ, что имеют молекулярное строение. К ним относятся многие кислоты, оксиды, гидриды. Качественная и количественная структура подобных соединений является постоянной. Например, состав воды в атмосфере, Мировом океане, ледниках и живых организмах отражает формула H2O.


























