В этом материале не только рассказано о том, как расположены частицы в твердых телах, но и как движутся они в газах или в жидкостях. Также будут описаны виды кристаллических решеток в различных веществах.
Агрегатное состояние
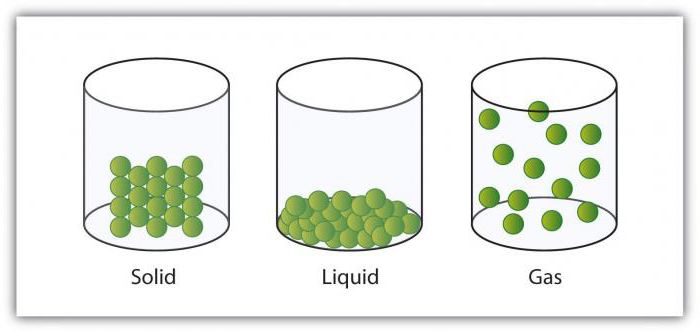
Существуют определенные стандарты, указывающие на наличие трех типичных агрегатных состояний, а именно: твердое вещество, жидкость и газ.
Определим составляющие для каждого агрегатного состояния.
- Твердые вещества практически стабильны по объему и форме. Последнюю изменить крайне проблематично без дополнительных энергетических затрат.
- Жидкость может легко менять форму, но при этом сохраняет объем.
- Газообразные вещества не сохраняют ни форму, ни объем.
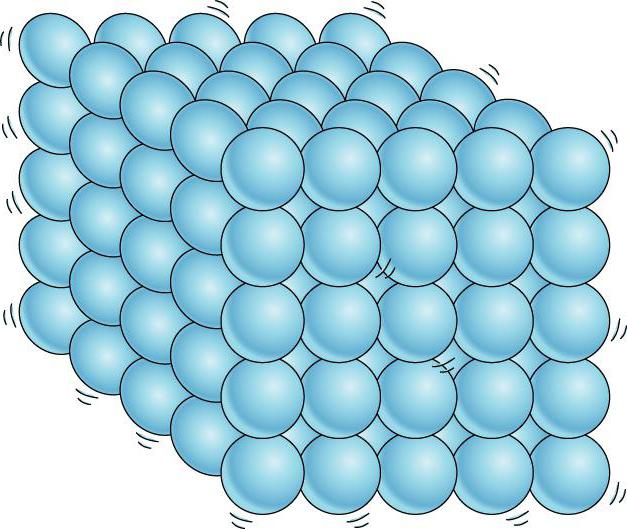
Главным критерием, по которому определяется агрегатное состояние, является расположение молекул и способы их движения. В газообразном веществе минимальное расстояние между отдельно взятыми молекулами значительно больше их самих. В свою очередь, молекулы жидких веществ не расходятся на большие расстояния в обычных для них условиях и сохраняют свой объем. Действующие частицы в твердых телах располагаются в строго определенном порядке, каждая из них, подобно маятнику часов, движется около определенной точки в кристаллической решетке. Это придает твердым веществам особенную прочность и жесткость.
Поэтому в данном случае наиболее актуален вопрос, как расположены действующие частицы в твердых телах. Во всех остальных случаях атомы (молекулы) не имеют настолько упорядоченной структуры.
Особенности жидкости
Необходимо обратить особое внимание на то, что жидкости являются своеобразным промежуточным звеном между твердыми состоянием тела и его газообразной фазой. Так, при понижении температуры жидкость затвердевает, а при повышении ее выше, чем точка кипения данного вещества, переходит в газообразное состояние. Однако жидкость имеет общие черты и с твердыми, и с газообразными веществами. Так, в 1860 году выдающийся отечественный ученый Д. И. Менделеев установил существование так называемой критической температуры – абсолютного кипения. Это такое значение, при котором исчезает тонкая граница между газом и веществом в твердом состоянии.
Следующий критерий, объединяющий два соседних агрегатных состояния, – изотропность. В данном случае их свойства одинаковы на всех направлениях. Кристаллы, в свою очередь, анизотропны. Подобно газам, жидкости не имеют фиксированной формы и занимают полностью объем сосуда, в котором находятся. То есть они обладают низкой вязкостью и высокой текучестью. Сталкиваясь между собой, микрочастицы жидкости или газа совершают свободные перемещения. Раньше считалось, что в объеме, занимаемом жидкостью, упорядоченного движения молекул нет. Таким образом, жидкость и газ противопоставлялись кристаллам. Но в результате последующих исследований было доказано сходство между твердыми и жидкими телами.
В жидкой фазе при температуре, близкой к затвердеванию, тепловое движение напоминает движение в твердых телах. В этом случае жидкость все же может иметь определенную структуру. Поэтому, давая ответ на такой вопрос, как расположены частицы в твердых телах в жидкостях и газах, можно сказать, что в последних движение молекул хаотичное, неупорядоченное. а вот в твердых веществах молекулы занимают в большинстве случаев определенное, фиксированное положение.
Жидкость при этом является своеобразным промежуточным звеном. Причем чем ближе ее температура к кипению, тем больше молекулы движутся как в газах. Если же температура ближе к переходу в твердую фазу, то микрочастицы начинают двигаться все более и более упорядоченно.
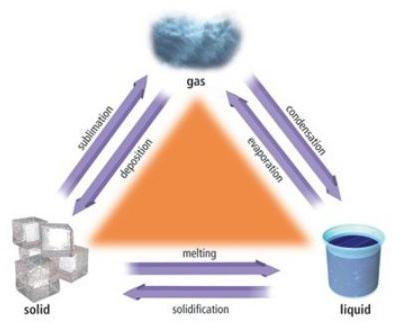
Изменение состояния веществ
Рассмотрим на самом простом примере изменение состояния воды. Лед – это твердая фаза воды. Температура его - ниже нуля. При температуре, равной нулю, лед начинает таять и превращается в воду. Это объясняется разрушением кристаллической решетки: при нагревании частицы начинают двигаться. Температура, при которой вещество изменяет агрегатное состояние, называется точкой плавления (в нашем случае у воды она равна 0). Заметим, что температура льда будет оставаться на одном уровне до полного его плавления. При этом атомы или молекулы жидкости будут двигаться так же, как в твердых телах.
После этого продолжим нагревать воду. Частицы при этом начинают двигаться интенсивнее до тех пор, пока наше вещество не достигнет следующей точки изменения агрегатного состояния – точки кипения. Такой момент наступает при разрыве связей между образующими ее молекулами за счет ускорения движения - тогда оно приобретает свободный характер, и рассматриваемая жидкость переходит в газообразную фазу. Процесс трансформации вещества (воды) из жидкой фазы в газообразную называется кипением.
Температуру, при которой вода закипает, называют точкой кипения. В нашем случае это значение равно 100 градусов по Цельсию (температура зависима от давления, нормальное давление составляет одну атмосферу). Заметим: пока существующая жидкость целиком и полностью не превратится в пар, температура ее остается постоянной.
Возможен и обратный процесс перехода воды из газообразного состояния (пара) в жидкость, который называется конденсация.
Далее можно наблюдать процесс замерзания - процесс перехода жидкости (воды) в твердую форму (исходное состояние описано выше – это лед). Описанные ранее процессы позволяют получить прямой ответ на то, как расположены частицы в твердых телах, в жидкостях и газах. Расположение и состояние молекул вещества зависит от его агрегатного состояния.
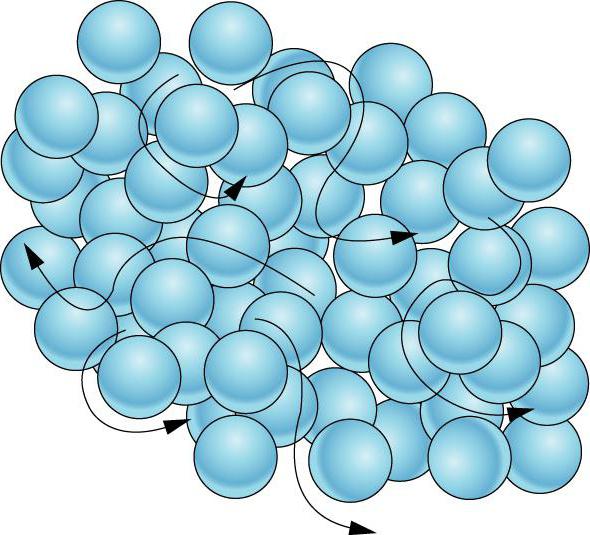
Что такое твердое тело? Как в нем ведут себя микрочастицы?
Твердое тело – это состояние материальной среды, отличительная особенность которого заключается в сохранении постоянной формы и постоянном характере теплового движения микрочастиц, совершающих незначительные колебания. Тела могут находиться в твердом, жидком и газообразном состоянии. Есть еще и четвертое состояние, которое современные ученые склонны относить к числу агрегатных - это так называемая плазма.
Итак, в первом случае любое вещество, как правило, имеет постоянную неизменную форму, и на это оказывает ключевое воздействие то, как расположены частицы в твердых телах. На микроскопическом уровне видно, что атомы, из которых состоит твердое тело, соединены друг с другом химическими связями и находятся в узлах кристаллической решетки.
Но есть и исключение — аморфные вещества, которые находятся в твердом состоянии, но наличием кристаллической решетки не могут похвастаться. Именно отталкиваясь от этого и можно дать ответ на то, как расположены частицы в твердых телах. Физика в первом случае указывает на то, что атомы или молекулы находятся в узлах решетки. А вот во втором случае подобной упорядоченности уж точно нет, и такое вещество более похоже на жидкость.
Физика и возможное строение твердого тела
В этом случае вещество стремится сохранить свой объем и, конечно же, форму. То есть для того, чтобы изменить последнюю, необходимо приложить усилия, и не имеет значения, металлический ли это предмет, кусок пластика или пластилин. Причина заключается в его молекулярном строении. А если точнее выразиться, во взаимодействии молекул, из которых состоит тело. Они в данном случае расположены наиболее близко. Такое расположение молекул носит повторяющийся характер. Именно поэтому силы взаимного притяжения между каждым из таких компонентов очень велики.
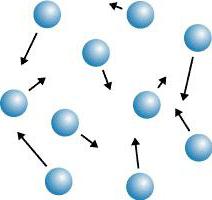
Взаимодействие микрочастиц объясняет характер их движения. Форму или объём подобного твердого тела скорректировать в ту или иную сторону очень трудно. Частицы твердого тела неспособны хаотично двигаться по всему объему твердого тела, а могут лишь колебаться возле определенной точки пространства. Молекулы твердого тела колеблются хаотично в разные стороны, но натыкаются на себе подобные, которые возвращают их в первоначальное состояние. Именно поэтому частицы в твердых телах располагаются, как правило, в строго определенном порядке.
Частицы и их расположение в твердом теле
Твердые тела могут быть трех видов: кристаллические, аморфные и композиты. Именно химический состав влияет на расположение частиц в твердых телах.
Кристаллические твердые тела обладают упорядоченной структурой. Их молекулы или атомы образуют кристаллическую пространственную решетку правильной формы. Таким образом, твердое тело, находящееся в кристаллическом состоянии, имеет определенную кристаллическую решетку, которая, в свою очередь, задает определенные физические свойства. Это и есть ответ на то, как расположены частицы в твердом теле.
Приведем пример: много лет назад в Петербурге на складе хранился запас белых блестящих оловянных пуговиц, которые при понижении температуры потеряли свой блеск и из белых стали серыми. Пуговицы рассыпались в серый порошок. «Оловянная чума» - так назвали эту «болезнь», но на самом деле это была перестройка структуры кристаллов под воздействием низкой температуры. Олово при переходе из белой разновидности в серую рассыпается в порошок. Кристаллы, в свою очередь, делятся на моно- и поликристаллы.
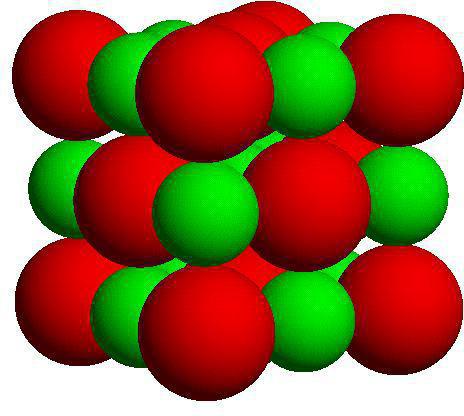
Монокристаллы и поликристаллы
Монокристаллы (поваренная соль) – это одиночные однородные кристаллы, представленные непрерывной кристаллической решеткой в форме правильных многоугольников. Поликристаллы (песок, сахар, металлы, камни) – это кристаллические тела, которые срослись из мелких, хаотично расположенных кристаллов. В кристаллах наблюдается такое явление, как анизотропия.
Аморфность: особый случай
Аморфные тела (смола, канифоль, стекло, янтарь) не имеют четкого строгого порядка в расположении частиц. Это нестандартный случай того, в каком порядке находятся частицы в твердых телах. В данном случае наблюдается явление изотропии, физические свойства аморфных тел одинаковы по всем направлениям. При высоких температурах они становятся подобны вязким жидкостям, а при низких - похожи на твердые тела. При внешнем воздействии одновременно обнаруживают упругие свойства, то есть при ударе раскалываются на миниатюрные частицы, как твердые тела, и текучесть: при длительном температурном воздействии начинают течь, как жидкости. Не имеют определенных температур плавления и кристаллизации. При нагревании аморфные тела размягчаются.
Примеры аморфных веществ
Возьмем, например, обыкновенный сахар и выясним расположение частиц в твердых телах в различных случаях на его примере. В этом случае один и тот же материал может встречаться в кристаллическом или аморфном виде. Если расплавленный сахар застывает медленно, молекулы образуют ровные ряды – кристаллы (кусковой сахар, или сахарный песок). Если расплавленный сахар, например, вылить в холодную воду, остывание произойдет очень быстро, и частицы не успеют сформировать правильные ряды - расплав затвердеет, не образуя кристаллов. Так получается сахарный леденец (это и есть некристаллический сахар).
Но через некоторое время такое вещество может перекристаллизоваться, частицы собираются в правильные ряды. Если сахарный леденец полежит несколько месяцев, он начнет покрываться рыхлым слоем. Так появляются на поверхности кристаллы. Для сахара сроком будет несколько месяцев, а для камня – миллионы лет. Уникальным примером может служить углерод. Графит – это кристаллический углерод, структура его слоистая. А алмаз – это самый твердый на земле минерал, способный резать стекло и распиливать камни, его применяют для бурения и полировки. В этом случаи вещество одно – углерод, но особенность заключается в способности образовывать разные кристаллическые формы. Это еще один вариант ответа на то, как расположены частицы в твердом теле.
Итоги. Заключение
Строение и расположение частиц в твердых телах зависит от того, к какому виду принадлежит рассматриваемое вещество. Если вещество кристаллическое, то расположение микрочастиц будет носить упорядоченный характер. Аморфные структуры такой особенностью не обладают. А вот композиты могут принадлежать как к первой, так и ко второй группе.
В одном случае жидкость себя ведет аналогично твердому веществу (при низкой температуре, которая близка к температуре кристаллизации), но может вести и как газ (при ее повышении). Поэтому в данном обзорном материале было рассмотрено, как расположены частицы не только в твердых телах, а и в прочих основных агрегатных состояниях вещества.


























