Буферная система: классификация, пример и механизм действия
Огромную роль для нормального функционирования человеческого организма играет кислотно-основное равновесие. Циркулирующая в организме кровь представляет собой смесь живых клеток, которые находятся в жидкой среде обитания. Первой чертой охраны, что контролирует уровень pH в крови, выступает буферная система. Это физиологический механизм, который обеспечивает сохранение параметров кислотно-основного баланса, препятствуя перепадам pH. Что он собой представляет и какие имеет разновидности, узнаем ниже.
Описание
Буферная система - это уникальный механизм. В организме человека существует их несколько, и все они состоят из плазмы и клеток крови. Буферы представляют собою основания (белки и неорганические соединения), которые связывают или отдают Н+ и ОН-, уничтожая сдвиг pH в течение тридцати секунд. Способность буфера поддерживать кислотно-основный баланс зависит от количества элементов, из которых он слагается.
Виды буферов крови
Кровь, которая постоянно движется, представляет собой живые клетки, которые существуют в жидкой среде. pH в норме составляет 7,37-7,44. Связка же ионов происходит определенным буфером, классификация буферных систем приведена ниже. Сам же он состоит из плазмы и кровяных клеток и может быть фосфатным, белковым, бикарбонатным или гемоглобиновым. Все эти системы имеют достаточно простой механизм действия. Их деятельность нацелена на урегулирование уровня ионов в крови.
Особенности буфера гемоглобинового
Гемоглобиновая буферная система является самой мощной из всех, она представляет собой щелочь в капиллярах тканей и кислоту в таком внутреннем органе, как легкие. На ее долю приходится около семидесяти пяти процентов всей буферной емкости. Этот механизм участвует во множестве процессах, что происходят в крови человека, и имеет в своем составе глобин. При переходе гемоглобинового буфера в другую форму (оксигемоглобин), наблюдается изменение этой формы, изменяются и кислотные свойства действующего вещества.
Качество восстановленного гемоглобина меньшее, чем у угольной кислоты, но становится намного лучше, когда он окисляется. Когда приобретается кислотность pH, гемоглобин соединяет ионы водорода, получается так, что он уже восстановленный. Когда происходит очищение углекислого газа в легких, pH получается щелочным. В это время гемоглобин, который окислился, выступает донором протонов, при помощи чего происходит уравновешивание кислотно-основного баланса. Так, буфер, что состоит из оксигемоглобина и его калиевой соли, способствует выделению из организма углекислоты.
Эта буферная система выполняет немаловажную роль в дыхательном процессе, так как совершает транспортную функцию по переносу к тканям и внутренним органам кислорода и удалению из них углекислоты. Кислотно-основное равновесие внутри эритроцитов при этом придерживается на постоянном уровне, следовательно, в крови также.
Таким образом, когда кровь насыщается кислородом, гемоглобин превращается в сильную кислоту, а когда кислород он отдает, то превращается в достаточно слабую органическую кислоту. Системы оксигемоглобина и гемоглобина - взаимопревращающиеся, они существуют как одно целое.
Особенности бикарбонатного буфера
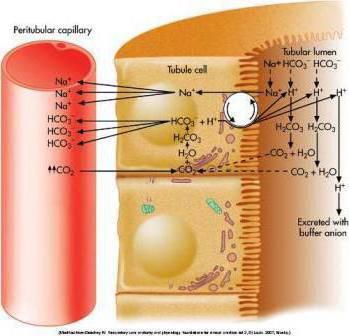
Бикарбонатная буферная система выступает также мощной, но и самой управляемой в организме. На ее долю приходится около десяти процентов всей буферной емкости. Она имеет универсальные свойства, которые обеспечивают ее двухстороннюю эффективность. В состав этого буфера входит сопряженная кислотно-щелочная пара, что состоит из таких молекул, как угольная кислота (источник протона) и бикарбонат аниона (акцептор протона).
Так, бикарбонатная буферная система способствует протеканию систематического процесса, где в кровь попадает мощная кислота. Этот механизм связывает кислоту с бикарбонатом анионов, образуя кислоту угольную и ее соль. При попадании щелочи в кровь буфер связывается с угольной кислотой, образуя бикарбонатную соль. Так как гидрокарбоната натрия в крови человека больше, чем угольной кислоты, данная буферная емкость будет иметь высокую кислотность. Другими словами, гидрокарбонатная буферная система (бикарбонатная) очень хорошо проводит компенсацию веществ, которые повышают кислотность крови. К ним относится и молочная кислота, концентрация которой увеличивается при интенсивных физических нагрузках, а данный буфер очень быстро реагирует на изменения кислотно-основного баланса в крови.
Особенности фосфатного буфера
Фосфатная буферная система человека занимает близко двух процентов всей буферной емкости, что связано с содержанием в крови фосфатов. Этот механизм поддерживает показатель pH в моче и жидкости, что находится внутри клеток. Буфер состоит из неорганических фосфатов: одноосновного (выполняет роль кислоты) и двухосновного (выполняет роль щелочи). При нормальном показателе pH соотношение кислоты и основания равняется 1:4. При увеличении количества ионов водорода фосфатная буферная система связывается с ними, образуя кислоту. Этот механизм больше кислотный, чем щелочной, поэтому он отлично нейтрализует поступающие в кровь человека кислые метаболиты, например, молочную кислоту.
Особенности белкового буфера
Белковый буфер играет не такую особую роль в стабилизации кислотно-щелочного баланса, по сравнению с другими системами. На его долю приходится около семи процентов всей буферной емкости. Белки состоят из молекул, которые объединяются в кислотно-щелочные соединения. В кислой среде они выступают щелочами, которые связывают кислоты, в щелочной среде все происходит наоборот.
Это приводит к тому, что образуется белковая буферная система, которая достаточно эффективна при значении pH от 7,2 до 7,4. Большая доля белков представлена альбуминами и глобулинами. Так как белковый заряд нулевой, то при нормальном показателе pH он находится в виде щелочи и соли. Эта буферная емкость зависит от количества белков, их структуры и свободных протонов. Данный буфер может нейтрализовать и кислые, и щелочные продукты. Но емкость она имеет больше кислотную, чем щелочную.
Особенности эритроцитов
В норме эритроциты имеют постоянный показатель pH – 7,25. Здесь оказывают действие гидрокарбонатный и фосфатный буферы. Но по мощности они отличаются от тех, что находятся в крови. В эритроцитах белковый буфер играет особую роль в обеспечении органов и тканей кислородом, а также удалению из них углекислоты. Кроме этого, он поддерживает постоянное значение внутри эритроцитов pH. Белковый буфер в эритроцитах тесно связан с гидрокарбонатной системой, так как соотношение кислоты и соли здесь меньшее, чем в крови.
Пример буферной системы
Растворы сильных кислот и щелочей, которые обладаю слабыми реакциями, имеют непостоянный показатель pH. Но смесь кислоты уксусной с ее солью сохраняет имеет стабильное значение. Даже если к ним добавить кислоту или щелочь, кислотно-основное равновесие не изменится. В качестве примера можно рассмотреть ацетатный буфер, который состоит из кислоты СН3СООН и ее соли СН3СОО. Если добавить сильную кислоту, то основание соли свяжет ионы Н+ и превратится в кислоту уксусную. Снижение уровня анионов соли уравновешивается увеличением молекул кислоты. В результате этого наблюдается незначительное изменение в соотношении кислоты и ее соли, поэтому pH изменяется совсем незаметно.
Механизм действия буферных систем
При поступлении в кровь кислых или щелочных продуктов буфер обеспечивает постоянное значение pH до тех пор, пока поступившие продукты не выведутся или не используются в процессах метаболизма. В крови человека представлены четыре буфера, каждый из которых состоит из двух частей: кислоты и ее соли, а также сильной щелочи.
Эффект буфера обуславливается тем, что он связывает и нейтрализует ионы, которые поступают соответствующим ему составом. Поскольку в природе организм больше всего сталкивается с недоокисленными продуктами обмена, свойства буфер имеет антикислотные больше, чем антищелочные.
Каждая буферная система имеет свой принцип работы. При снижении уровня pH ниже отметки 7,0 начинается их активная деятельность. Они начинают связывать излишки свободных ионов водорода, образуя комплексы, которые перемещают кислород. Он, в свою очередь, перемещается к системе пищеварения, легким, коже, почкам и так далее. Такая транспортировка кислых и щелочных продуктов способствует их разгрузке и выведению.
В организме человека только четыре буферные системы играют важные роли в сохранении кислотно-основного равновесия, но существуют и другие буферы, например, ацетатная буферная система, которая имеет слабую кислоту (донор) и ее соль (акцептор). Способность этих механизмов противостоять изменениям pH при попадании кислоты или соли в кровь является ограниченной. Они поддерживают кислотно-щелочное равновесие только в том случае, когда сильная кислота или щелочь поступают в определенном количестве. Если оно будет превышено, pH резко изменится, буферная система прекратит свое действие.
Эффективность буферов
Буферы крови и эритроцитов имеют различную эффективность. У последних она выше, так как здесь присутствует гемоглобиновый буфер. Уменьшение количества ионов происходит по направлению от клетки до межклеточной среды, а затем до крови. Это говорит о том, что самая большая буферная емкость у крови, а меньшую имеет внутриклеточная среда.
При метаболизме в клетках появляются кислоты, которые проходят в межклеточную жидкость. Это происходит тем легче, чем их больше появляется в клетках, поскольку переизбыток ионов водорода увеличивает проницаемость мембраны клетки. Нам уже известна классификация буферных систем. В эритроцитах они имеют более эффективные свойства, так как здесь еще играют роль коллагеновые волокна, которые реагируют набуханием на накопление кислоты, они ее поглощают и освобождают от ионов водорода эритроциты. Такая его способность обуславливается свойством абсорбции.
Взаимодействие буферов в организме
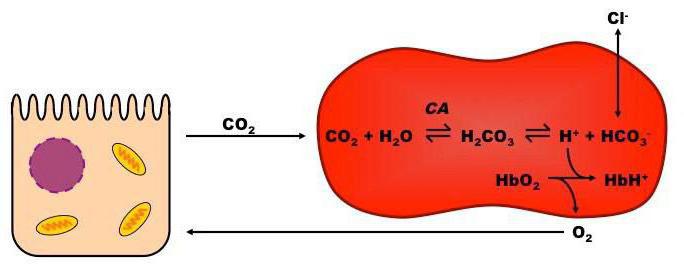
Все механизмы, которые находятся в организме, взаимосвязаны между собой. Буферы крови состоят из нескольких систем, вклад которых в поддержание кислотно-щелочного баланса различный. При попадании крови в легкие она получает кислород путем его связывания в эритроцитах гемоглобином, образуя оксигемоглобин (кислоту), что поддерживает уровень pH. При содействии карбоангидразы происходит параллельное очищение крови легких от углекислоты, которая в эритроцитах представлена в виде слабой двухосновной угольной кислотой и карбаминогемоглобином, а в крови – углекислотой и водой.
При уменьшении в эритроцитах количества слабой двухосновной угольной кислоты происходит проникновение ее из крови в эритроцит, и очищение крови от углекислоты. Таким образом, из клеток в кровь постоянно проходит слабая двухосновная угольная кислота, а из крови в эритроциты для соблюдения нейтральности поступают неактивные анионы хлорида. В результате этого в красных клетках крови среда более кислотная, чем в плазме. Все системы буферов обосновываются отношением донор-акцептор протона (4:20), что связано с особенностями метаболизма организма человека, который образует большее число кислотных продуктов, чем щелочных. Очень важным здесь является показатель кислотных буферных емкостей.
Обменные процессы в тканях
Кислотно-основной баланс поддерживается буферами и метаболическими превращениями в тканях организма. Этому помогают биохимические и физико-химические процессы. Они способствуют потере кислотно-щелочных свойств продуктов обмена веществ, их связыванию, образованию новых соединений, которые быстро выводятся из организма. Например, большое количество молочной кислоты выводится в гликоген, органические кислоты нейтрализуются солями натрия. Сильные кислоты и щелочи растворяются в липидах, а органические кислоты подвергаются окислению, образуя угольную кислоту.
Таким образом, буферная система - это первый помощник при нормализации кислотно-щелочного баланса в организме человека. Стабильность pH нужна для нормальной работы биологических молекул и структур, органов и тканей. При нормальных условиях буферные процессы поддерживают равновесие между появлением и удалением ионов водорода и углекислого газа, что способствует обеспечению в крови постоянного уровня pH.
Если происходит сбой в работе буферных систем, то у человека появляются такие патологии, как алкалоз или ацидоз. Все буферные системы взаимосвязаны и направлены на поддержание стабильного кислотно-основного равновесия. В организме человека постоянно образуется большое число кислых продуктов, которое эквивалентно тридцати литрам сильной кислоты.
Постоянство реакций внутри организма обеспечивают мощные буферы: фосфатный, белковый, гемоглобиновый и бикарбонатный. Существуют и другие буферные системы, но эти являются основными и самыми нужными для живого организма. Без их помощи у человека начнут развиваться различные патологии, которые могут привести к коме или летальному исходу.