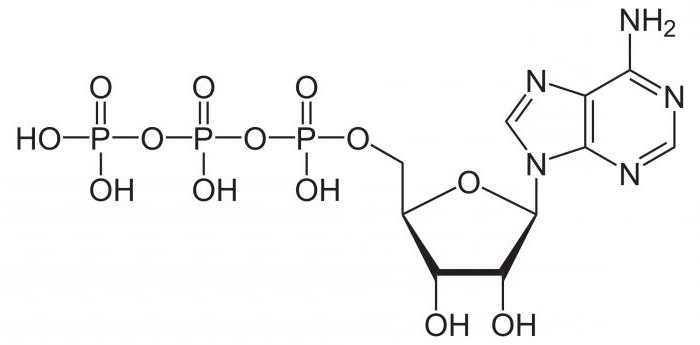
Все биохимические реакции в клетках любого организма протекают с расходованием энергии. Дыхательная цепь – это последовательность специфических структур, которые расположены на внутренней мембране митохондрий и служат для образования АТФ. Аденозинтрифосфат является универсальным источником энергии и способен аккумулировать в себе от 80 до 120 кДж.
Дыхательная цепь электронов - что это такое?
Электроны и протоны играют важную роль в образовании энергии. Они создают разность потенциалов на противоположных сторонах мембраны митохондрий, что порождает направленное движение частиц – ток. Дыхательная цепь (она же ЭТЦ, цепь переноса электронов) является посредником при переносе положительно заряженных частиц в межмембранное пространство и отрицательно заряженных частиц в толще внутренней мембраны митохондрий.
Главная роль в образовании энергии принадлежит АТФ-синтазе. Этот сложный комплекс видоизменяет энергию направленного движения протонов в энергию биохимических связей. К слову, практически идентичный комплекс находится и в хлоропластах растений.
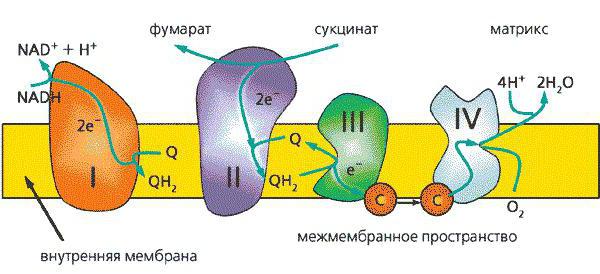
Комплексы и ферменты дыхательной цепи
Перенос электронов сопровождается биохимическими реакциями в присутствии ферментативного аппарата. Эти биологически активные вещества, многочисленные копии которых образуют большие комплексные структуры, служат посредниками при переносе электронов.
Комплексы дыхательной цепи – это центральные компоненты транспортировки заряженных частиц. Всего во внутренней мембране митохондрий находятся 4 таких образования, а также АТФ-синтаза. Все эти структуры объединены общей целью – перенос электронов по ЭТЦ, перенос протонов водорода в межмембранное пространство и, как следствие, синтез АТФ.
Комплекс представляет собой скопление белковых молекул, среди которых встречаются ферменты, структурные и сигнальные протеины. Каждый из 4 комплексов выполняет свою, только свойственную ему, функцию. Давайте разберемся, для каких задач в ЭТЦ присутствуют эти структуры.
I комплекс
В переносе электронов в толще мембраны митохондрий главную роль выполняет дыхательная цепь. Реакции отщепления протонов водорода и сопутствующих им электронов – одна из центральных реакций ЭТЦ. Первый комплекс транспортной цепи принимает на себя молекулы НАД*Н+ (у животных) или НАДФ*Н+ (у растений) с последующим отщеплением четырех протонов водорода. Собственно, из-за этой биохимической реакции I комплекс также называется НАДН – дегидрогеназой (по названию центрального фермента).
В состав дегидрогеназного комплекса входят железосерные белки 3 видов, а также флавинмононуклеотиды (ФМН).
II комплекс
Работа данного комплекса не сопряжена с переносом протонов водорода в межмембранное пространство. Основная функция этой структуры заключается в поставке дополнительных электронов в электрон-транспортную цепь посредством окисления сукцината. Центральный фермент комплекса – сукцинат-убихинон-оксидоредуктаза, который катализирует отщепление электронов от янтарной кислоты и перенос на липофильный убихинон.
Поставщиком протонов водорода и электронов ко второму комплексу также является ФАД*Н2. Однако КПД флавинадениндинуклеотида меньше, чем у его аналогов – НАД* Н или НАДФ*Н.
В состав II комплекса входят три вида железосерных белков и центральный фермент сукцинат-оксидоредуктаза.
III комплекс
Следующий по счету компонент, ЭТЦ, состоит из цитохромов b556, b560 и c1, а также железосерного белка Риске. Работа третьего комплекса сопряжена с переносом двух протонов водорода в межмембранное пространство, и электронов от липофильного убихинона на цитохром С.
Особенностью белка Риске является то, что он растворяется в жире. Другие протеины этой группы, которые встречались в составе комплексов дыхательной цепи, водорастворимы. Эта особенность влияет на положение белковых молекул в толще внутренней мембраны митохондрий.
Третий комплекс функционирует как убихинон-цитохром с-оксидоредуктаза.
IV комплекс
Он же цитохром-оксидантный комплекс, является конечным пунктом в ЭТЦ. Его работа заключается в переносе электрона с цитохрома-с на атомы кислорода. Впоследствии отрицательно заряженные атомы О будут вступать в реакцию с протонами водорода с образованием воды. Главный фермент – цитохром с-кислород-оксидоредуктаза.
В состав четвертого комплекса входят цитохромы a, a3 и два атома меди. Центральная роль в переносе электрона к кислороду досталась цитохрому a3. Взаимодействие этих структур подавляется цианидом азота и угарным газом, что в глобальном смысле приводит к прекращению синтеза АТФ и гибели.
Убихинон
Убихинон – это витаминоподобное вещество, липофильное соединение, которое свободно перемещается в толще мембраны. Дыхательная цепь митохондрий не может обойтись без этой структуры, т. к. она отвечает за транспортировку электронов от комплексов I и II к комплексу III.
Убихинон является производным бензохинона. Эта структура на схемах может обозначаться буквой Q или сокращенно ЛУ (липофильный убихинон). Окисление молекулы приводит к образованию семихинона – сильного окислителя, который потенциально опасен для клетки.
АТФ-синтаза
Главная роль в образовании энергии принадлежит АТФ-синтазе. Эта грибоподобная структура использует энергию направленного движения частиц (протонов) для преобразования ее в энергию химических связей.
Основной процесс, который встречается на протяжении всей ЭТЦ, - это окисление. Дыхательная цепь отвечает за перенос электронов в толще мембраны митохондрий и аккумулирование их в матриксе. Одновременно с этим комплексы I, III и IV перекачивают протоны водорода в межмембранное пространство. Разница зарядов на сторонах мембраны приводит к направленному движению протонов через АТФ-синтазу. Так Н+ попадают в матрикс, встречают электроны (которые связаны с кислородом) и образуют нейтральное для клетки вещество – воду.
АТФ-синтаза состоит из F0 и F1 субъединиц, которые вместе образуют роутер молекулы. F1 состоит из трех альфа и трех бета-субъединиц, которые вместе образуют канал. Этот канал имеет в точности такой же диаметр, какой имеют протоны водорода. При прохождении положительно заряженных частиц через АТФ-синтазу головка F0 молекулы крутится на 360 градусов вокруг своей оси. За это время к АМФ или АДФ (аденозинмоно- и дифосфат) присоединяются фосфорные остатки с помощью макроэргических связей, в которых заключено большое количество энергии.
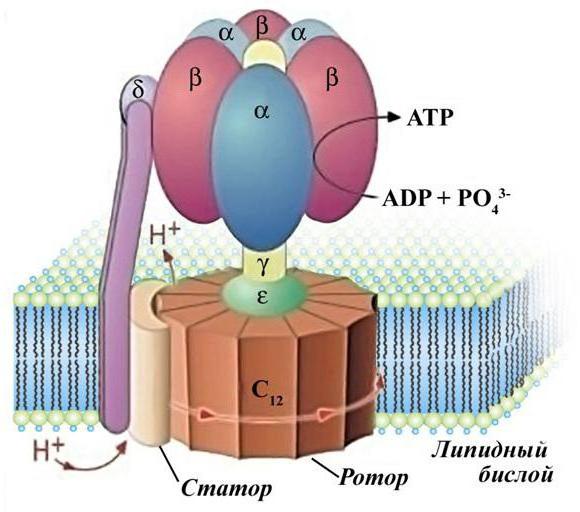
АТФ-синтазы встречаются в организме не только в митохондриях. У растений эти комплексы также расположены на мембране вакуолей (тонопласте), а также на тилакоидах хлоропласт.
Также в клетках животных и растений присутствуют АТФ-азы. Они имеют схожую структуру, как и у АТФ-синтаз, однако их действие направлено на отщепление фосфорных остатков с затратой энергии.
Биологический смысл дыхательной цепи
Во-первых, конечным продуктом реакций ЭТЦ является так называемая метаболическая вода (300-400 мл в сутки). Во-вторых, происходит синтез АТФ и запасание энергии в биохимических связях этой молекулы. В сутки синтезируется 40-60 кг аденозинтрифосфата и столько же используется в ферментативных реакциях клетки. Срок жизни одной молекулы АТФ составляет 1 минуту, поэтому дыхательная цепь должна работать слаженно, четко и без ошибок. В противном случае клетка погибнет.
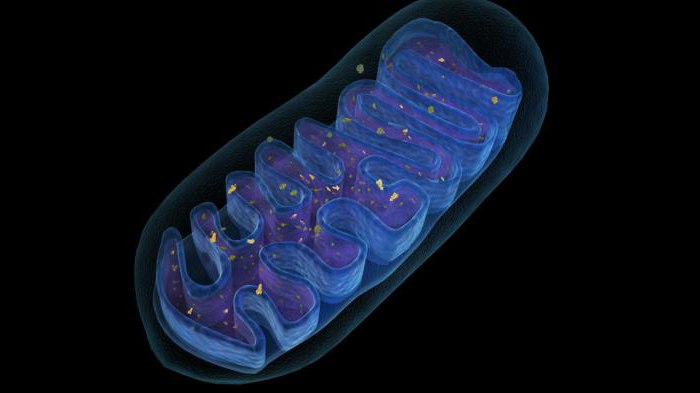
Митохондрии считаются энергетическими станциями любой клетки. Их количество зависит от энергозатрат, которые необходимы для тех или иных функций. Например, в нейронах можно насчитать до 1000 митохондрий, которые часто образуют скопление в так называемой синаптической бляшке.
Отличия дыхательной цепи у растений и животных
У растений дополнительной «энергетической станцией» клетки является хлоропласт. На внутренней мембране этих органелл также найдены АТФ-синтазы, и это является преимуществом перед животными клетками.
Также растения могут выживать в условиях высокой концентрации угарного газа, азота и цианидов за счет цианид-устойчивого пути в ЭТЦ. Дыхательная цепь, таким образом, заканчивается на убихиноне, электроны с которого сразу переносятся на атомы кислорода. В результате синтезируется меньше АТФ, однако растение может пережить неблагоприятные условия. Животные в таких случаях при длительном воздействии погибают.
Можно сравнить КПД НАД, ФАД и цианид-устойчивого пути с помощью показателя образования АТФ при переносе 1 электрона.
- с НАД или НАДФ образуется 3 молекулы АТФ;
- с ФАД образуется 2 молекулы АТФ;
- по цианид-устойчивому пути образуется 1 молекула АТФ.

Эволюционное значение ЭТЦ
Для всех эукариотических организмов одним из основных источников энергии является дыхательная цепь. Биохимия синтеза АТФ в клетке делится на два типа: субстратное фосфорилирование и окислительное фосфорилирование. ЭТЦ используется в синтезе энергии второго типа, т. е. за счет окислительно-восстановительных реакций.
У прокариотических организмов АТФ образуется только в процессе субстратного фосфорилирования на стадии гликолиза. Шестиуглеродные сахара (преимущественно глюкоза) вовлекаются в цикл реакций, и на выходе клетка получает 2 молекулы АТФ. Этот тип синтеза энергии считается наиболее примитивным, т. к. у эукариот в процессе окислительного фосфорилирования образуется 36 молекул АТФ.
Однако это не значит, что современные растения и животные потеряли способность к субстратному фосфорилированию. Просто этот тип синтеза АТФ стал только одним из трех этапов получения энергии в клетке.
Гликолиз у эукариот проходит в цитоплазме клетки. Там находятся все необходимые ферменты, которые смогут расщепить глюкозу до двух молекул пировиноградной кислоты с образованием 2 молекул АТФ. Все последующие этапы проходят в матриксе митохондрий. Цикл Кребса, или цикл трикарбоновых кислот, также протекает в митохондриях. Это замкнутая цепь реакций, в результате работы которой синтезируются НАД*Н и ФАД*Н2. Эти молекулы пойдут как расходный материал в ЭТЦ.


























