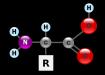
Ароматические аминокислоты – это органические соединения, в составе которых есть карбоксильная группа, бензольное кольцо, аминогруппа. Наличие нескольких функциональных групп объясняет двойственность свойств этих органических веществ.
Нахождение в природе
Ароматические аминокислоты входят в состав тканей и клеток живых организмов. Несмотря на многообразие представителей данного класса, только 20 аминокислот являются мономерами для построения белков и пептидов. Бензойная кислота, например, содержится в клюкве, имеет отличные антиоксидантные свойства.
Многие микроорганизмы и растения способны самостоятельно синтезировать некоторые ароматические аминокислоты, необходимые для полноценного функционирования.
Они принимают активное участие в углеводном и белковом обмене, входят в состав нуклеиновых кислот, витаминов, гормонов, пигментов, алкалоидов, антибиотиков, токсинов. Некоторые являются посредниками в процессе передачи нервных импульсов.
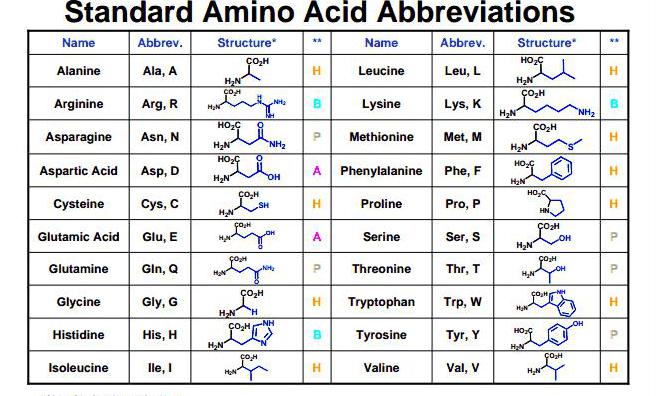
Классификация
Существует деление представителей данного класса органических кислородсодержащих соединений по структурным признакам.
С учетом расположения амино- и карбоксильной функциональных групп, выделяют
α-, β-, γ-, δ-, ε- кислоты.
По численности групп различают основные, нейтральные, кислые вещества.
В зависимости от строения углеводородного радикала выделяют аминокислоты ароматического ряда, алифатические, гетероциклические, серосодержащие вещества.
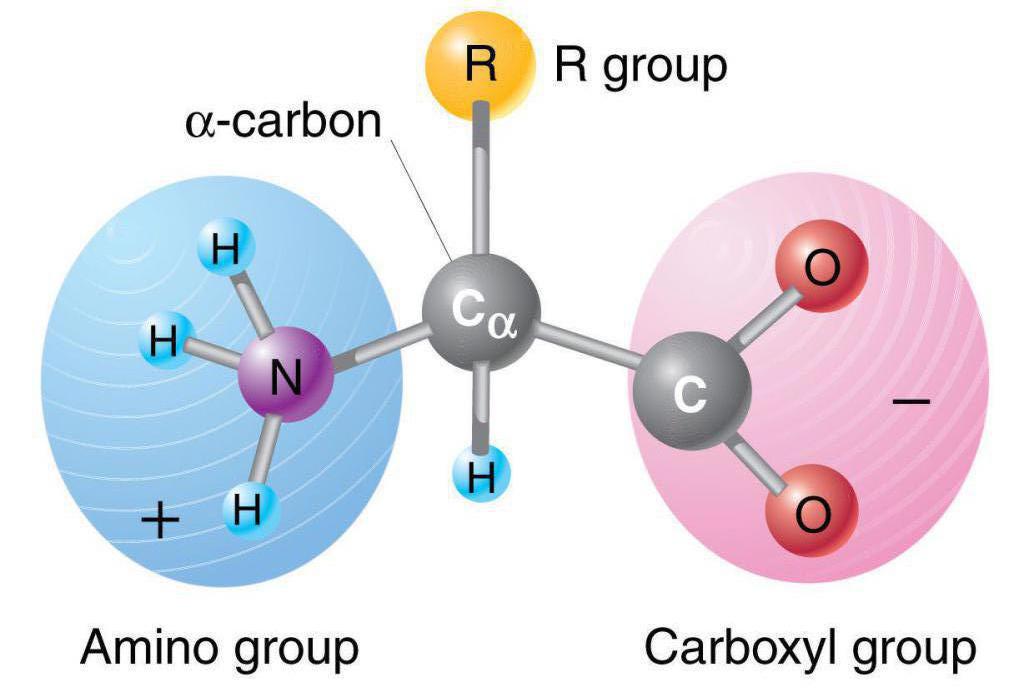
Важные сведения
Для того чтобы назвать эти органические соединения, используется систематическая номенклатура. Ароматические аминокислоты – производные бензола, в боковой цепи которого появляется одна либо несколько карбоксильных (кислотных) групп. Простейшим представителем данного класса является бензойная кислота. Введение в боковую цепь гидроксильной группы приводит к образованию салициловой кислоты.
Производные ароматических аминокислот - сложные эфиры и амиды - используются в химической промышленности.
Историческая справка о бензойной кислоте
Бензойную кислоту человечество знает с давних времен. В шестнадцатом веке она была выделена путем сублимации из смолы. В 19-м веке немецкие химики изучили химические свойства данного соединения, сравнили ее с гиппуровой кислотой. Благодаря противогрибковому и противомикробному действию бензойная кислота стала использоваться в виде пищевого консерванта в процессе изготовления продуктов питания. Ее обозначают на этикетках продуктов как добавку Е 210.
Физические и химические свойства
По своему внешнему виду бензойная кислота похожа на продолговатые тонкие белые иглы, обладающие специфическим блеском. Она отлично растворяется в различных средах: спиртах, жирах, воде. Температура плавления данной ароматической аминокислоты - 122 градуса по Цельсию. Она переходит из твердого состояния в газ.
В больших объемах бензойную кислоту получают путем окисления толуола (метилбензола).
Она является природным соединением, так как обнаружена в некоторых ягодах: бруснике, чернике, клюкве. Кроме того, бензойная кислота образуется в таких кисломолочных продуктах, как йогурт, простокваша. Соединение не токсично, не опасно для человека, если употреблять его в небольших количествах.
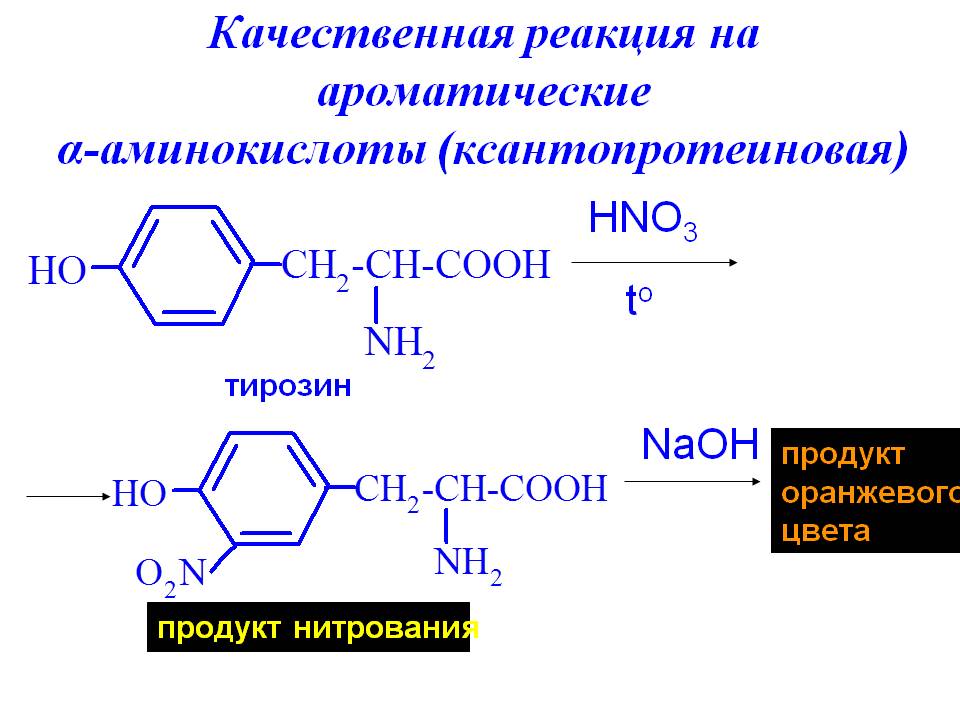
Химические свойства
Качественная реакция на ароматические аминокислоты – электрофильное замещение в ароматическом кольце (нитрование концентрированной азотной кислотой). Ксантопротеиновая реакция применяется для обнаружения следующих ароматических кислот: тирозина, фенилаланина, триптофана, гистидина. Процесс сопровождается образованием продукта, окрашенного в яркий желтый цвет.
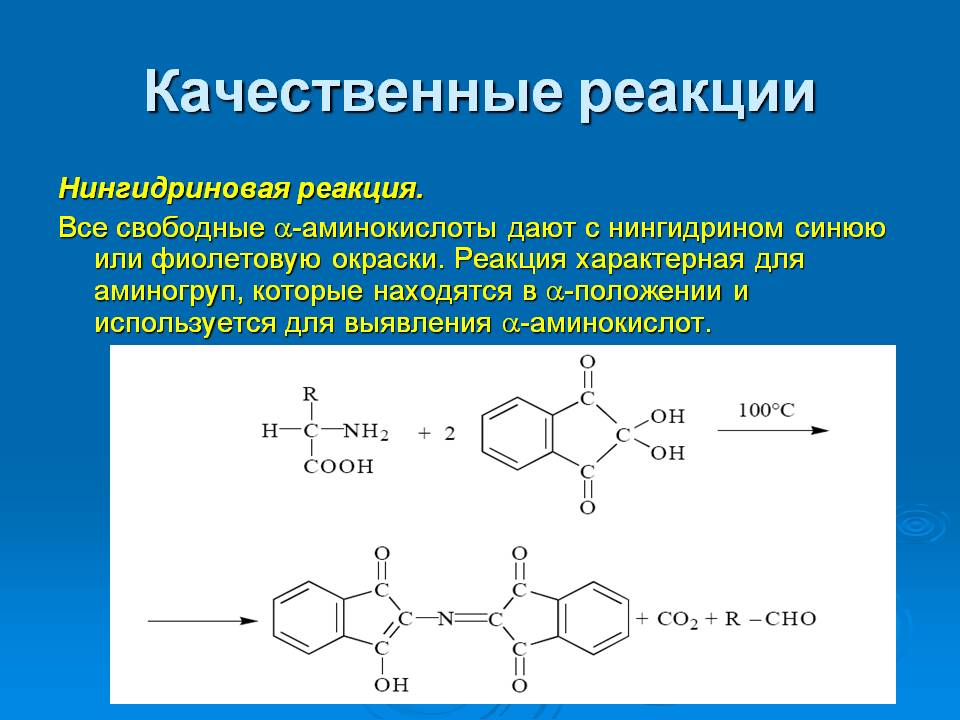
Еще одна качественная реакция на ароматические аминокислоты – нингидриновая, которая используется при проведении количественного и качественного определения не только аминокислот, но и аминов. При нагревании нингидрина в щелочном растворе с соединениями, в которых присутствуют первичные аминогруппы, получается продукт, имеющий сине-фиолетовую окраску.
Данная химическая реакция используется и для выявления вторичных аминогрупп в составе ароматических кислот: оксипролина и пролина. Об их присутствии можно судить по образованию устойчивого продукта желтого яркого цвета. При проведении современного химического анализа ароматических аминокислот применяют именно нингидриновую реакцию.
Метод бумажной хроматографии дает возможность выявлять каждую аминокислоту во взятой смеси в количестве от двух до пяти микрограммов.
Применение
Пищевой консервант Е 210 (бензойную кислоту) используют в кондитерской, пивоваренной, хлебопекарной промышленности. Приведем некоторый список продуктов, производство которых неразрывно связано с использованием бензойной кислоты: мороженое, овощные консервы, пиво, ликеры, заменители сахара, маринованная и соленая рыба, жевательная резинка, масло, маргарин.
Не обходится без этой ароматической кислоты и изготовление некоторых косметических средств. Часто ее добавляют и в лекарственные препараты, к примеру, в антисептические мази. Фармацевты проявляют внимание к бензойной кислоте из-за ее консервирующих свойств.
Данное органическое соединение прекрасно справляется с разнообразными грибками, микробами, простыми паразитами. Именно поэтому бензойную кислоту добавляют в детские сиропы от кашля. Она оказывает отхаркивающее действие, размягчает мокроту, выводит ее из бронхов. Высока эффективность медицинских растворов, предназначенных для ножных ванн, в составе которых присутствует бензойная кислота.
Органическое соединение способствует устранению избыточной потливости ног. Бензойная кислота считается эффективным средством борьбы с грибковыми поражениями кожи. В химической промышленности бензойная кислота применяется как основной реагент в изготовлении многих органических соединений.
Попадая в организм человека, бензойная кислота вступает в химическое взаимодействие с белковыми молекулами.
Происходит ее трансформирование в гиппуровую кислоту, затем она выводится с мочой из организма.