Все биохимические реакции, протекающие в организме, подвержены специфическому контролю, который осуществляется через активирующее или ингибирующее воздействие на регуляторные ферменты. Последние обычно находятся в начале цепочек метаболических превращений и либо запускают многоэтапный процесс, либо тормозят его. Регулированию также подвергаются некоторые единичные реакции. Конкурентное ингибирование является одним из основных механизмов контроля каталитической активности ферментов.
Что такое ингибирование?
Механизм ферментативного катализа основан на связывании активного центра энзима с молекулой субстрата (комплекс ES), в результате чего происходит химическая реакция с образованием и освобождением продукта (E+S = ES = EP = E+P).
Ингибированием фермента называют снижение скорости или полную остановку процесса катализа. В более узком смысле под этим термином подразумевают уменьшение сродства активного центра к субстрату, что достигается путем связывания молекул энзимов с веществами-ингибиторами. Последние могут действовать различными способами, на основании чего поделены на несколько типов, которым соответствуют одноименные механизмы ингибирования.
Основные типы ингибирования
По характеру протекания процесса ингибирование бывает двух видов:
- Необратимое – вызывает стойкие изменения в молекуле фермента, лишающие ее функциональной активности (последняя не подлежит восстановлению). Оно может иметь как специфический, так и неспецифический характер. Ингибитор прочно связывается с энзимом путем ковалентного взаимодействия.
- Обратимое – основной вид негативной регуляции ферментов. Осуществляется за счет обратимого специфического присоединения ингибитора к белку-энзиму слабыми нековалентными связями, поддается кинетическому описанию по уравнению Михаэлиса-Ментен (исключение составляет аллостерическая регуляция).
Выделяют два основных типа обратимого ингибирования ферментов: конкурентное (может быть ослаблено увеличением концентрации субстрата) и неконкурентное. В последнем случае происходит снижение максимально возможной скорости катализа.
Основная разница между конкурентным и неконкурентным ингибированием заключается в месте присоединения регуляторного вещества к ферменту. В первом случае ингибитор связывается непосредственно с активным центром, а во втором – с другим участком энзима, либо с фермент-субстратным комплексом.

Существует также смешанный тип ингибирования, при котором связывание с ингибитором не предотвращает образование ES, но замедляет катализ. В этом случае вещество-регулятор находится в составе двойных или тройных комплексов (EI и EIS). При бесконкурентном типе фермент связывается только с ES.
Особенности обратимого конкурентного ингибирования ферментов
Конкурентный механизм ингибирования основан на структурном сходстве регуляторного вещества с субстратом. В результате образуется комплекс активного центра с ингибитором, условно обозначаемый как EI.
Обратимое конкурентное ингибирование имеет следующие особенности:
- связывание с ингибитором происходит в активном центре;
- инактивация молекулы фермента обратима;
- ингибирующий эффект может быть уменьшен увеличением концентрации субстрата;
- ингибитор не влияет на максимальную скорость ферментативного катализа;
- комплекс EI может распадаться, что характеризуется соответствующей константой диссоциации.
При таком типе регуляции ингибитор и субстрат как бы соперничают (конкурируют) друг с другом за место в активном центре, откуда и произошло название процесса.
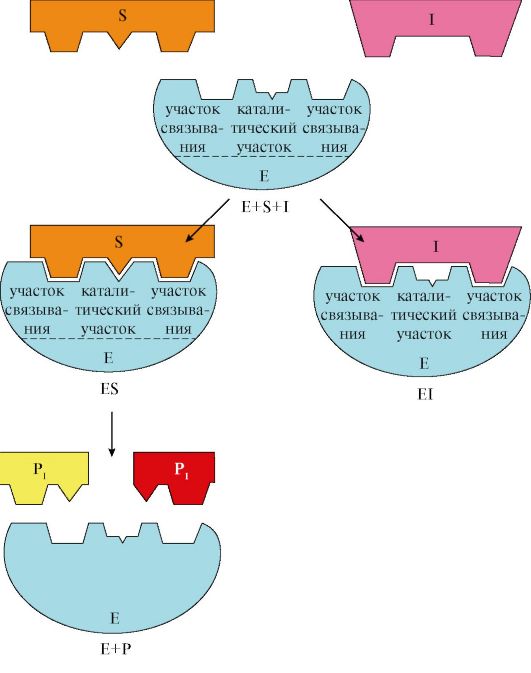
В итоге конкурентное ингибирование можно определить как обратимый процесс торможения ферментативного катализа, основанный на специфическом сродстве активного центра к веществу-ингибитору.
Механизм действия
Связывание ингибитора с активным центром препятствует образованию фермент-субстратного комплекса, необходимого для осуществления катализа. В итоге молекула энзима становится неактивной. Тем не менее каталитический центр может связаться не только с ингибитором, но и с субстратом. Вероятность образования того или иного комплекса зависит от соотношения концентраций. Если молекул субстрата значительно больше, то фермент будет реагировать с ними чаще, чем с ингибитором.
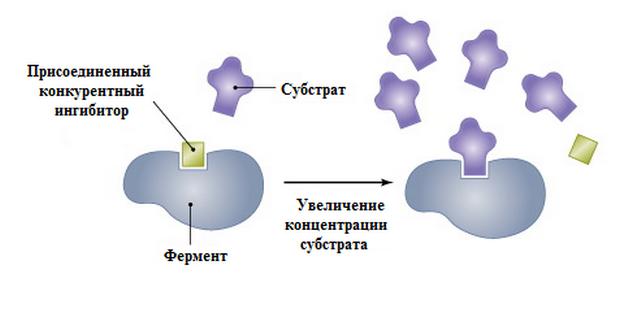
Влияние на скорость химической реакции
Степень торможения катализа при конкурентном ингибировании определяется тем, какое количество фермента будут образовывать EI-комплексы. При этом можно увеличить концентрацию субстрата до такой степени, что роль ингибитора будет вытеснена, а скорость катализа достигнет максимально возможного значения, соответствующего величине Vmax по уравнению Михаэлиса-Ментен.
Такое явление объясняется сильным разбавлением ингибитора. Как следствие, вероятность связывания с ним молекул фермента сводится к нулю, а активные центры реагируют только с субстратом.
Кинетические зависимости ферментативной реакции при участии конкурентного ингибитора
Конкурентное ингибирование увеличивает константу Михаэлиса (Km), которая равна концентрации субстрата, необходимой для достижения ½ максимальной скорости катализа в начале реакции. Количество фермента, гипотетически способного связаться с субстратом, остается постоянным, а число фактически образующихся ES-комплексов зависит только от концентрации последнего (комплексы EI не постоянны и могут быть вытеснены субстратом).
Конкурентное ингибирование ферментов легко определить по графикам кинетической зависимости, построенным для разных концентраций субстрата. В этом случае величина Km будет меняться, а Vmax оставаться постоянной величиной.

При неконкурентном ингибировании все наоборот: ингибитор связывается вне активного центра и присутствие субстрата никак не может на это повлиять. В результате часть молекул фермента "выключается" из катализа, и максимально возможная скорость снижается. Тем не менее активные молекулы энзима могут беспрепятственно связываться с субстратом как при маленькой, так и при высокой концентрации последнего. Следовательно, константа Михаэлиса остается постоянной.
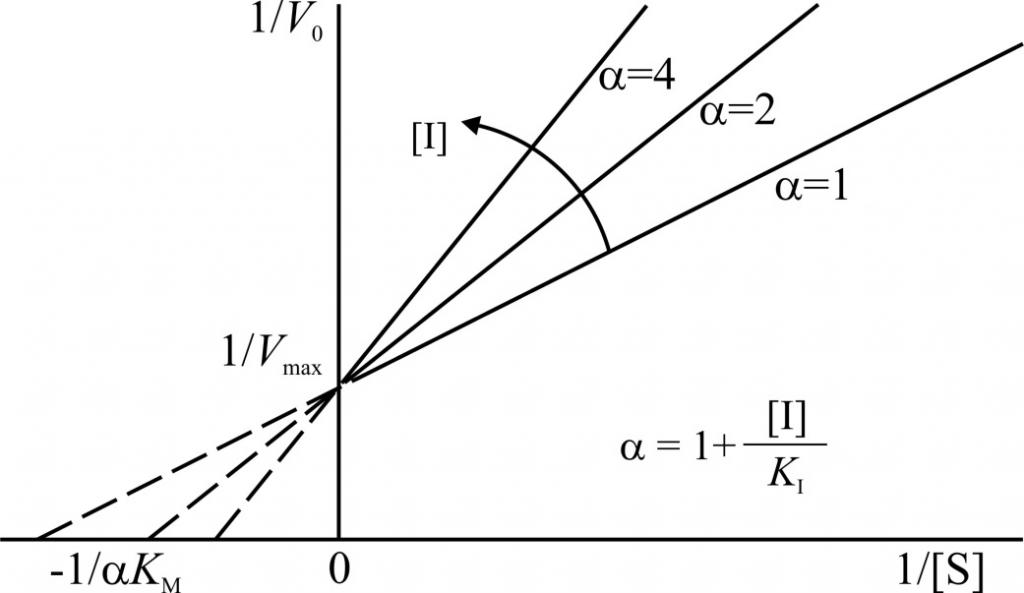
Графики конкурентного ингибирования в системе двойных обратных координат представляют собой несколько прямых, пересекающих ось ординат в точке 1/Vmax. Каждая прямая соответствует определенной концентрации субстрата. Разные точки пересечения с осью абсцисс (1/[S]) говорят об изменении константы Михаэлиса.
Действие конкурентного ингибитора на примере малоната
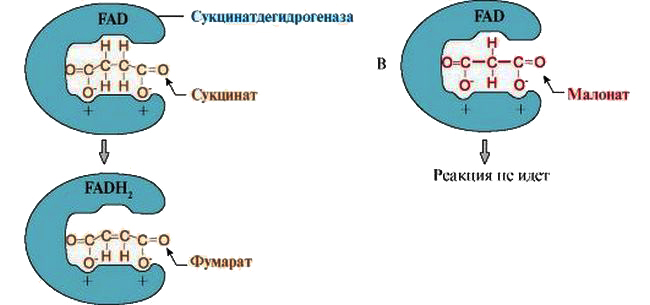
Типичным примером конкурентного ингибирования является процесс снижения активности сукцинатдегидрогиназы — фермента, катализирующего окисление янтарной кислоты (сукцината) в фумаровую. В роли ингибитора здесь выступает малонат, имеющий структурное сходство с сукцинатом.

Добавление ингибитора в среду вызывает образование комплексов малоната с сукцинатдегидрогиназой. Такая связь не вызывает повреждения активного центра, но блокирует его доступность для янтарной кислоты. Увеличение концентрации сукцината снижает ингибирующий эффект.
Использование в медицине
На механизме конкурентного ингибирования основано действие многих лекарственных препаратов, представляющих собой структурные аналоги субстратов некоторых метаболических путей, торможение которых является необходимой частью лечения заболеваний.
Например, для улучшения проводимости нервных импульсов при мышечных дистрофиях требуется повысить уровень ацетилхолина. Это достигается угнетением активности гидролизующей его ацетилхолинэстеразы. В роли ингибиторов выступают четвертичные аммониевые основания, входящие в состав лекарственных препаратов (прорезин, эндрофоний и т. д.).
В особую группу выделяют антиметаболиты, которые помимо ингибирующего действия проявляют свойства псевдосубстрата. В таком случае формирование комплекса EI приводит к образованию биологически инертного аномального продукта. К антиметаболитам относят сульфаниламиды (используются при лечении бактериальных инфекций), аналоги нуклеотидов (применяются для остановки клеточного роста раковой опухоли) и т. д.


























