Алифатические аминокислоты - производные карбоновых кислот - широко распространены в природе. Они играют важную роль во многих жизненно важных процессах. На их основе изготавливают некоторые виды лекарственных средств.
Алифатическая аминокислота – что это?
Аминокислоты выполняют важные функции в организме человека и других животных, так как являются нейромедиаторами и «кирпичиками» для построения белков. Также они нужны для правильного обмена веществ.
Алифатические аминокислоты – это разновидность аминокарбоновых аминокислот, у которых амино- и карбоксильная группы связаны с алифатическим атомом углерода. Термин «алифатический» подразумевает линейные или разветвленные цепи из атомов данного элемента.
Основная масса аминокислот, которые были выделены из живых организмов, относятся именно к алифатическим. В химии используют, в основном, обиходные названия этих веществ по исходным белкам, из которых они были получены, так как по систематической номенклатуре у них слишком громоздкие наименования.
Типы соединений по строению
Алифатические аминокислоты, в зависимости от положения амино- и карбоксильных групп, подразделяют на следующие виды:
-
Альфа-изомеры. К ним относится основная масса природных соединений, которые находятся в растениях, микроорганизмах, животных. Их находят также в метеоритах, причем структура этих веществ такая же, как и у земных живых существ.
-
Бетта-аминокислоты. Примером является β-аланин, который служит частью кофермента А. Последний принимает участие в синтезе и окислении жирных кислот.
-
Гамма-изомеры. Один из ярких представителей этой группы – ɣ-аминомасляная кислота (ГАМК), важнейший нейромедиатор нервной системы, отвечающий за торможение нервных процессов, ослабление и подавление возбуждения.
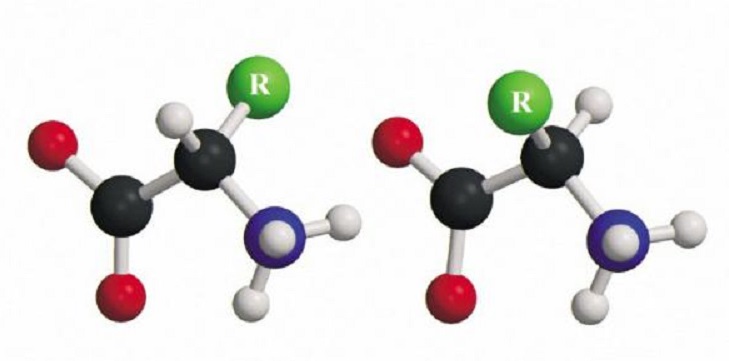
Все аминокислоты альфа-типа, кроме глицина, имеют асимметричную структуру, существуют в виде двух зеркальных, не совмещаемых в пространстве отражений (L- и D-аминокислоты) и обладают естественной оптической активностью. Важнейшими L-аминокислотами являются глицин, аланин, серин, цистеин, аспарагиновая кислота, тирозин, лейцин, глутамин, изолейцин, аргинин, лизин, пролин.
Примеры алифатических аминокислот приведены на рисунке ниже.
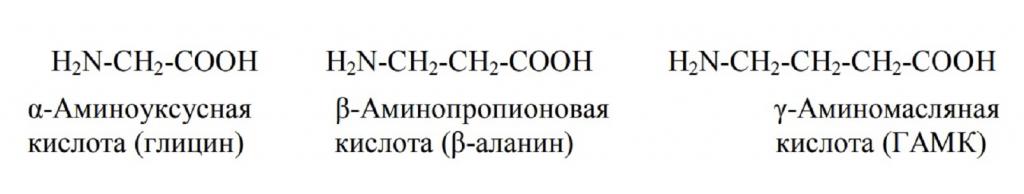
Виды веществ по другим критериям
Существует также классификация по характеру участия алифатических аминокислот в синтезе белка.
-
Протеиногенные соединения из L-ряда, которые присоединяются в состав белков в рибосомах под контролем РНК. Их последовательность кодируется генетически. Таких аминокислот всего двадцать.
-
Непротеиногенные (некодируемые), не входящие в состав белков, но выполняющие важные функции (в основном, участие в обменных процессах). Некоторые из них являются токсинами и ядовиты для человека.
По кислотно-основным свойствам алифатические аминокислоты подразделяют на 3 типа:
-
кислые (аспарагиновая и глутаминовая кислоты);
-
нейтральные, содержащие одно и то же число основных и кислотных групп;
-
основные (гистидин, аргинин, лизин и другие).
Физико-химические характеристики

Для алифатических аминокислот характерны следующие свойства:
-
структура в виде биполярных ионов в кристаллическом состоянии;
-
высокая температура плавления (у α-аминокислот нет ее четкого значения);
-
хорошая растворимость в воде и водных растворах щелочей, кислот;
-
амфотерность;
-
основные свойства в кислой среде и наоборот;
-
если pH среды больше, чем изоэлектрическая точка, то алифатические аминокислоты образуют с щелочами соли, которые хорошо растворяются в воде.
Из смесей этих веществ с их натриевыми или калиевыми солями делают буферные растворы, применяемые для химического анализа.
Синтез
В лабораторных условиях производство данных соединений представляет собой сложную задачу, так как они являются оптически активными, и в естественных условиях их выработка происходит с участием ферментов. Поэтому химическим путем получают только рацемические аминокислоты, представляющие собой смесь оптических изомеров.
В качестве исходного вещества применяют α-галоидкарбоновые кислоты, которые при реагировании с аммиаком дают алифатические аминокислоты. Существуют и другие способы получения – из кетокислот и их производных в процессе восстановительного аминирования, из малонового эфира, аминоуксусной кислоты (глицина). Для синтеза аминокислот в промышленном масштабе используют микробиологические технологии. При помощи генной инженерии эти вещества выделяют из белковых молекул, вырабатываемых специально культивируемыми микроорганизмами.
Роль в природе

Только в растениях и микроорганизмах выявлено более 200 алифатических аминокислот, а всего их насчитывается на сегодняшний день свыше пятисот. Они входят в состав антибактериальных веществ (например, пенициллина), которые вырабатывают микроорганизмы, а также формируют клеточные стенки большинства бактерий.
В организме животных эти вещества выполняют следующие основные функции:
-
синтез белков, ферментов, гормонов, коэнзимов и других важных органических соединений;
-
образование биологически активных аминов (дофамин, норадреналин, адреналин, серотонин и других);
-
участие в передаче нервных импульсов и в метаболических процессах.
В клетках головного мозга человека происходит активный обмен веществ с участием аминокислот, концентрация которых превосходит в 7 раз таковую в плазме крови.
Применение в медицине
Использование этих соединений в лечебных целях основано на их свойстве участвовать в обмене азотистых элементов и синтезе биологически активных веществ. Существует множество препаратов, где содержатся алифатические аминокислоты. Ниже перечислены некоторые из них и их назначение в терапевтической практике.
-
Глутаминовая кислота – патологии ЦНС, эпилепсия, психозы, задержка психического развития у детей, ДЦП, болезнь Дауна.
-
Метионин – токсические поражения печени (цирроз, отравления мышьяком, хлороформом и другими токсинами), а также заболевания этого органа при хроническом алкоголизме, сахарном диабете.
-
Аминалон – нейротропное средство.
-
Цистеин – при катаракте.
-
Ацетилцистеин – при заболеваниях органов дыхания в качестве муколитика.



























