Этиламины представляют собой класс органических соединений, относящихся к аминам и содержащих в своем составе этильную группу -C2H5. Наиболее широко используются моноэтиламин, диэтиламин и триэтиламин.
Химическое строение
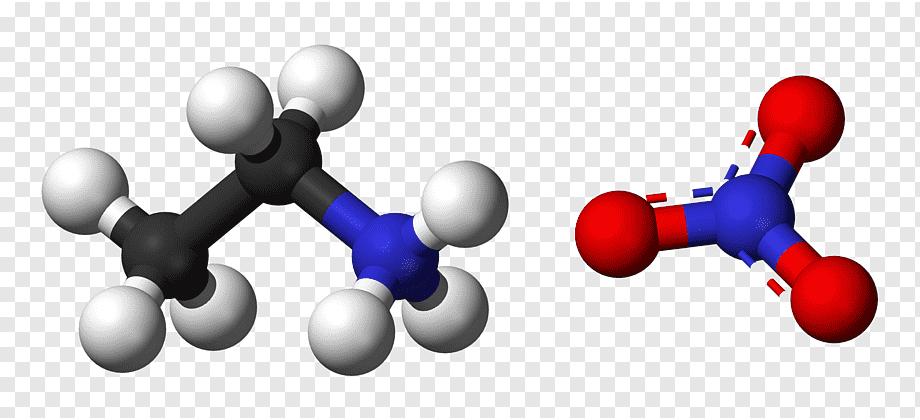
Общая формула этиламинов: C2H5NRR', где R и R' - различные радикалы. Наиболее распространены этиламины, содержащие в структуре только этильные радикалы.
- Моноэтиламин имеет структурную формулу C2H5NH2.
- Диэтиламин имеет структурную формулу (C2H5)2NH.
- Триэтиламин имеет структурную формулу (C2H5)3N.
Таким образом, этиламины отличаются количеством этильных групп, присоединенных к атому азота. Эти группы придают молекулам основные свойства.
Физические свойства
Этиламины представляют собой бесцветные жидкости с характерным аминным запахом. Их физические свойства зависят от количества этильных групп:
- Моноэтиламин имеет температуру кипения 16,6°C.
- Диэтиламин имеет температуру кипения 56,3°C.
- Триэтиламин имеет температуру кипения 89,4°C.
Чем больше этильных групп в молекуле, тем выше температура кипения. Этиламины смешиваются с водой, этанолом и другими полярными растворителями. Они обладают высокой токсичностью.
Химические свойства
Благодаря наличию атома азота и свободной электронной пары, этиламины проявляют свойства оснований и аминов. Они реагируют с кислотами с образованием солей:
C2H5NH2 + HCl → C2H5NH3Cl (моноэтиламин гидрохлорид)
Также этиламины способны вступать в реакции нуклеофильного замещения, окисления, восстановления и другие.
Получение
В промышленности этиламины получают путем взаимодействия этанола с аммиаком при высокой температуре и давлении в присутствии катализаторов:
C2H5OH + NH3 → C2H5NH2 + H2O
Образуется смесь моно-, ди- и триэтиламинов, которые затем разделяют с помощью ректификации. Другие этиламины можно получить алкилированием аммиака или моноэтиламина диэтилсульфатом, хлорэтаном и другими алкилирующими агентами.
Применение
Этиламины находят широкое применение в различных отраслях промышленности:
- Производство пестицидов, пластификаторов, лекарственных препаратов.
- Синтез моющих средств, ингибиторов коррозии.
- Обработка текстильных изделий.
- Нефтегазовая и химическая промышленность.
Помимо этого, этиламины используют как исходные вещества для получения более сложных органических соединений. Благодаря своей реакционной способности они легко вступают в химические реакции.
В целом, этиламины являются важным классом азотсодержащих органических соединений, обладающих ценными свойствами и широким спектром применения.

Методы очистки
После синтеза этиламины содержат примеси исходных реагентов и побочных продуктов реакции, поэтому требуют дополнительной очистки. Для этой цели применяют различные методы:
- Ректификация для удаления летучих примесей.
- Жидкостная экстракция органическими растворителями.
- Ионный обмен для удаления ионных примесей.
- Кристаллизация из подходящих растворителей.
Выбор методов зависит от природы примесей, требований к чистоте продукта и экономической целесообразности процесса.
Токсичность и меры безопасности
В чистом виде этиламины представляют опасность для здоровья. Они обладают раздражающим действием на слизистые оболочки и кожу. При вдыхании вызывают отек легких. Хроническое воздействие может привести к поражению печени и почек.
При работе с этиламинами необходимо соблюдать следующие меры предосторожности:
- Использовать средства индивидуальной защиты.
- Обеспечить эффективную вентиляцию помещений.
- Избегать попадания на кожу и в глаза.
- При разливе нейтрализовать раствором кислоты.
Хранение
Ввиду высокой реакционной способности и токсичности, этиламины требуют особых условий хранения. Рекомендуется соблюдать следующие правила:
- Хранить в герметичной стальной или стеклянной таре.
- В сухом прохладном помещении при температуре не выше 25°С.
- Вдали от источников тепла, влаги и прямого солнечного света.
- Отдельно от сильных окислителей и кислот.
Правильные условия хранения предотвращают разложение этиламинов и продлевают срок их годности.
Утилизация отходов
Отработанные растворы этиламинов являются опасными отходами и требуют особой утилизации. Для этих целей применяют такие методы, как:
- Химическое окисление раствором гипохлорита натрия или пероксида водорода.
- Термическое обезвреживание в печах при температуре свыше 900°С.
- Закачка в глубокие подземные горизонты.
Выбор метода зависит от объемов отходов, наличия инфраструктуры и экономических соображений. Правильная утилизация предотвращает негативное воздействие на окружающую среду.























