В химических реакциях по месту разрушения двойной связи в алкенах и тройной в алкинах могут присоединяться различные частицы. Каким закономерностям подчиняется этот процесс? Исследовал поведение несимметричных гомологов этилена при гидрогалогенировании и гидратации русский ученый В. В. Марковников. Он установил, что механизм протекания реакции зависит от того, с каким числом водорода связан углерод при двойной связи. Гипотеза, которую выдвинул ученый, подтвердилась после открытий в области строения атома. Правило Марковникова заложило основы создания научной теории, имеющей практическое применение. Она позволяет более рационально организовать производство полимеров, смазочных масел, спиртов.
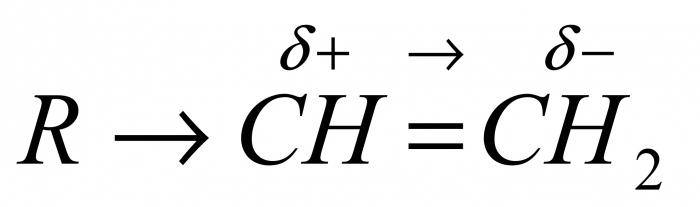
Правило Марковникова
Русский ученый в своей деятельности много времени уделял изучению механизма присоединения несимметричных реагентов к непредельным углеводородам. В своей статье, изданной на немецком языке в 1870 году, В. В. Марковников обратил внимание научного сообщества на избирательность взаимодействия галогеноводородов с атомами углерода, находящимися при двойной связи в несимметричных алкенах. Русский исследователь привел данные, которые он получил опытным путем в своей лаборатории. Марковников писал, что галоген обязательно присоединяется к тому атому углерода, который содержит наименьшее количество атомов водорода. Большую популярность работы ученого приобрели в начале XX века. Предложенная им гипотеза механизма взаимодействия получила название «правило Марковникова».
Жизнь и деятельность ученого-органика

- получил циклобутандикарбоновую кислоту;
- исследовал нефть Кавказа и открыл в ней органические вещества особого состава — нафтены;
- установил разницу в температурах плавления соединений с разветвленными и прямолинейными цепочками;
- доказал изомерию жирных кислот.
Труды ученого в значительной мере содействовали развитию отечественной химической науки и промышленности.
Суть гипотезы, выдвинутой Марковниковым
Ученый много лет посвятил изучению реакций присоединения реагентов к непредельным углеводородам с одной двойной связью (алкенам). Он заметил, что если в составе соединений присутствует водород, то он направляется к тому углеродному атому, который содержит больше частиц этого вида. Анион присоединяется к соседнему углероду. Это и есть правило Марковникова, его суть. Ученый гениально предсказал поведение частиц, о строении которых в то время еще имелись не очень четкие представления. В соответствии с правилом, к этиленовым углеводородам присоединяются сложные вещества, имеющие состав НХ, где Х:
- галоген;
- гидроксил;
- кислотный остаток серной кислоты;
- другие частицы.
Современное звучание правила Марковникова отличается от формулировок ученого: атом водорода из молекулы НХ, присоединяемой алкеном, направляется к тому углероду при двойной связи, который уже содержит больше водорода, а частица Х направляется к наименее гидрогенизированному атому.
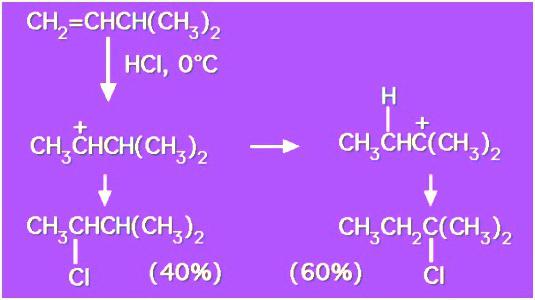
Механизм присоединения электрофильных частиц
Рассмотрим виды химических превращений, в которых применяется правило Марковникова. Примеры:
- Реакция присоединения к пропену хлороводорода. В ходе взаимодействия между частицами происходит разрушение двойной связи. Анион хлора направляется к менее гидрогенизированному углероду, находившемуся при двойной связи. Водород взаимодействует с наиболее гидрогенизированным из этих атомов. Образуется 2-хлор пропан.
- В реакции присоединения молекулы воды гидроксил из ее состава подходит к менее гидрогенизированному углероду. Водород присоединяется к наиболее гидрогенизированному атому при двойной связи.
Существуют исключения из предложенного Марковниковым правила в тех реакциях, где реагентами выступают алкены, у которых углерод при двойной связи уже имеет рядом электроотрицательную группу. Она частично отбирает электронную плотность, к которой обычно притягивается положительно заряженный водород. Не соблюдается правило и в реакциях, идущих по радикальному, а не электрофильному механизму (эффект Хариша). Эти исключения не умаляют достоинств правила, выведенного выдающимся русским химиком-органиком В. В. Марковниковым.

























