Гидролиз солей - важный процесс, применяемый во многих отраслях промышленности. Контроль степени гидролиза позволяет оптимизировать технологические процессы и повысить качество продукции. В данной статье мы подробно рассмотрим современные методы определения степени гидролиза и проанализируем основные факторы, оказывающие влияние на этот важный показатель.
1. Основные понятия гидролиза
Гидролиз - это реакция обмена между растворенным веществом, чаще всего солью, и молекулами воды. Существует несколько разновидностей гидролиза:
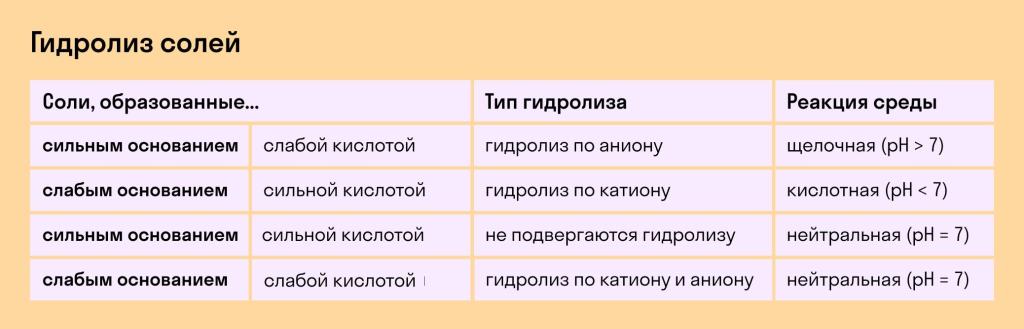
- Гидролиз по аниону - происходит в солях слабых кислот и сильных оснований;
- Гидролиз по катиону - наблюдается в солях слабых оснований и сильных кислот;
- Смешанный гидролиз - протекает в солях, образованных слабыми кислотами и слабыми основаниями.
Степень гидролиза - это отношение количества соли, вступившей в реакцию с водой, к общему количеству растворенной соли, выраженное в процентах. Этот показатель характеризует полноту протекания гидролиза.
Степень гидролиза солей тем выше, чем слабее кислота или основание, образующие данную соль.
Константа гидролиза также является важной характеристикой этого процесса. Она показывает соотношение между концентрациями продуктов и исходных веществ степень гидролиза в состоянии равновесия.
2. Качественная оценка степени гидролиза
Для приблизительной оценки степени и константы гидролиза конкретной соли можно сравнить значения констант гидролиза и диссоциации образующих ее кислоты и основания.
Если константа гидролиза существенно превышает константу диссоциации, то гидролиз будет протекать практически полностью. При сопоставимых константах степень гидролиза будет средней. А если константа диссоциации намного больше, то гидролиз будет слабым.
Также на качественном уровне о степени гидролиза можно судить по изменению кислотности или щелочности раствора после растворения соли.
Рассмотрим несколько примеров.
При растворении ацетата натрия CH3COONa, образованного слабой уксусной кислотой и сильным NaOH, происходит заметный гидролиз по аниону с образованием гидроксид-ионов. Это приводит к щелочной реакции раствора. Значит, степень гидролиза этой соли довольно высока.
Гидрофосфат натрия NaHPO4, напротив, дает слабокислую реакцию раствора, поскольку гидролиз по катиону протекает незначительно. Степень гидролиза этой соли невысока.
Для более точной оценки степени гидролиза применяют различные физико-химические методы анализа, о которых речь пойдет далее.
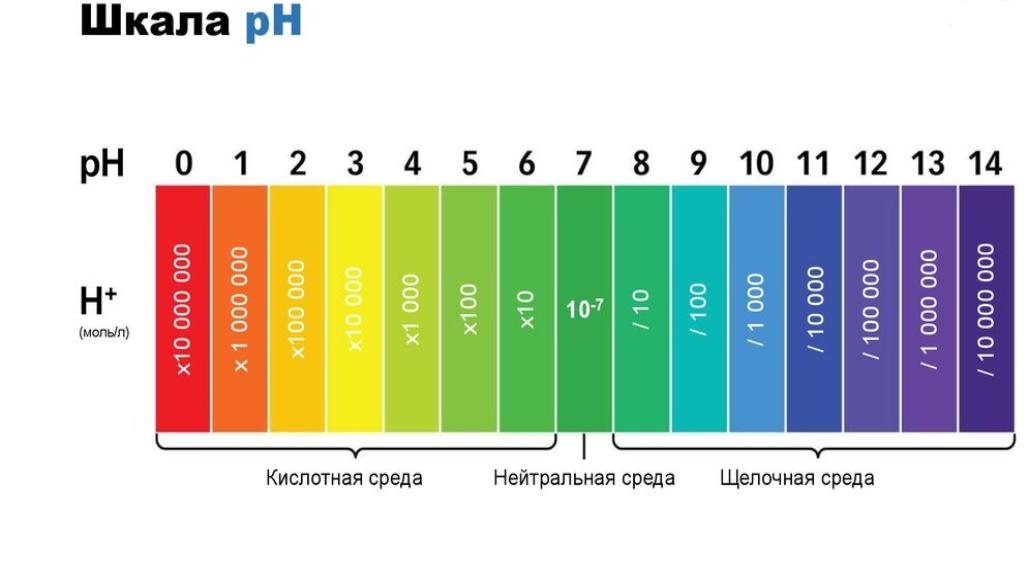
3. Измерение рН раствора
Одним из распространенных методов количественной оценки степени гидролиза солей является измерение рН раствора после растворения в нем анализируемой соли. Для этого используют иономер или рН-метр.
По изменению рН можно определить тип гидролиза и приблизительно оценить его степень. Чем сильнее сдвиг рН в кислую или щелочную область, тем выше степень гидролиза.
Более точные данные дает построение кривых титрования раствора солью до и после гидролиза. По смещению точки эквивалентности можно количественно вычислить степень гидролиза.
4. Кондуктометрическое определение
Электропроводность растворов электролитов зависит от концентрации и природы ионов. Этот параметр можно точно измерить с помощью кондуктометра.
При гидролизе соли происходит частичное связывание ионов, что приводит к снижению электропроводности раствора. По величине этого снижения можно вычислить степень гидролиза.
5. Спектрофотометрическое определение
Данный метод основан на зависимости светопоглощения растворов от химического состава и концентрации компонентов. С помощью спектрофотометра измеряют оптическую плотность или коэффициент поглощения анализируемого раствора.
Заранее строят градуировочные графики концентрация-оптическая плотность для продуктов гидролиза. По полученным данным затем можно точно вычислить их концентрацию и степень гидролиза солей.
6. Хроматографический анализ
С помощью хроматографии можно разделить компоненты реакционной смеси и количественно определить содержание каждого вещества.
Получив хроматограмму раствора соли до и после гидролиза, сравнивают площади пиков исходных веществ и продуктов реакции. Эти данные позволяют рассчитать степень гидролиза.
7. Факторы, влияющие на степень гидролиза
На величину степени гидролиза оказывают влияние различные факторы:
- Природа образующих соль кислоты и основания. Чем слабее кислота или основание, тем выше степень гидролиза;
- Концентрация реагирующих веществ. Повышение концентрации соли или продуктов гидролиза замедляет реакцию;
- Температура. Повышение температуры ускоряет гидролиз, так как эта реакция эндотермическая;
- Присутствие посторонних веществ, взаимодействующих с продуктами гидролиза, может сместить равновесие.
Учитывая эти факторы, можно оптимизировать условия проведения гидролиза, чтобы достичь требуемой степени гидролиза.
8. Расчет константы гидролиза
Для количественной оценки гидролиза, помимо его степени, используют величину константы равновесия этой реакции. Она показывает соотношение между концентрациями продуктов и исходных веществ в состоянии равновесия.
Константу гидролиза можно вычислить по известным константам диссоциации кислоты и основания, образующих данную соль, а также по значению ионного произведения воды.
Зная константу гидролиза, можно рассчитать величину рН среды и сравнить ее с экспериментально измеренным значением рН.
9. Пример расчета
Рассмотрим в качестве примера среднюю соль - ацетат аммония NH4CH3COO. Она образована слабым основанием NH3 и слабой кислотой CH3COOH.
Сначала вычисляем константу гидролиза этой соли. Затем по полученному значению рассчитываем рН ее раствора с концентрацией 0,1 моль/л. По сдвигу рН определяем степень гидролиза.
10. Гидролиз в промышленности
Гидролиз широко используется в различных отраслях промышленности. Например, в производстве мыла, бумаги, искусственного волокна, при получении гидролизного спирта и многих других процессах.
Контроль степени гидролиза позволяет оптимизировать технологические режимы, снизить расход реагентов, повысить выход целевых продуктов. Поэтому методы определения степени гидролиза, о которых шла речь в данной статье, широко востребованы в промышленности.
























