Человеческий организм называют биохимической фабрикой совершенно не зря. Ведь каждую минуту в нем происходят тысячи, десятки и сотни тысяч процессов окисления, расщепления, восстановления и прочих реакций. Что позволяет им протекать с такой огромной скоростью, обеспечивая каждую клетку энергией, питанием и кислородом?
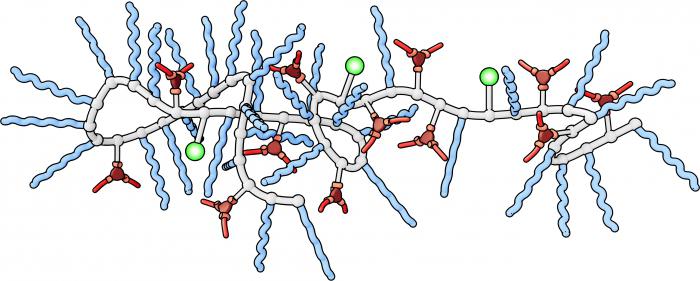
Понятие о катализаторах
Как в неорганической, так и в органической химии очень широко используются специальные вещества, способные ускорять протекание химических реакций в несколько тысяч, а иногда и миллионов раз. Название этих соединений - "катализаторы". В неорганической химии это оксиды металлов, платина, серебро, никель и другие.
Их главное действие - образование временных комплексов с участниками реакции, за счет понижения энергии активации процесс осуществляется в несколько раз быстрее. После этого комплекс распадается, и из сферы можно вывести катализатор в том же количественном и качественном составе, что и до начала процесса.
Существует два варианта каталитических реакций:
- гомогенные - ускоритель и участники в одном агрегатном состоянии;
- гетерогенные - ускоритель и участники в разных состояниях, есть граница раздела фаз.
Кроме того, есть и противоположные по действию соединения - ингибиторы. Они направлены на замедление необходимых реакций. Так, например, они позволяют снизить количество времени на формирование коррозии.
Биологические катализаторы по своей природе отличаются от неорганических, да и свойства их несколько специфичны. Поэтому в живых системах катализ другой.
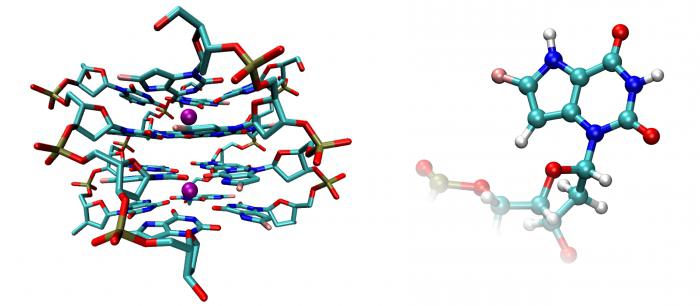
Ферменты - что это?
Доказано, что если бы действие специальных веществ, ускоряющих обозначенные процессы, не осуществлялось внутри живых систем, то обычное яблоко в желудке переваривалось бы около двух дней. За такое количество времени начались бы процессы разложения и интоксикация продуктами гниения. Однако этого не происходит, и фрукт полностью перерабатывается уже за полтора часа. Осуществляют это биологические катализаторы, которые в большом количестве присутствуют в составе каждого организма. Но что они собой представляют и на чем основано такое действие?
Биологические катализаторы белковой природы - это ферменты. Их основа - сложные структурная организация, обладающая рядом специфичных свойств. Проще говоря, это уникальные белки, способные снижать энергию активации процессов в живых организмах и осуществлять их со скоростью, превышающей обычные значения в несколько миллионов раз.
Можно привести множество примеров подобных молекул:
- каталаза;
- амилаза;
- оксиредуктаза;
- глюкозооксидаза;
- липаза;
- инвертаза;
- лизоцим;
- протеаза и другие.
Таким образом, можно сделать вывод: ферменты - биологические катализаторы белковой природы, которые действуют как сильные ускорители, позволяя осуществлять тысячи процессов в живых организмах с очень высокой скоростью. На их действии основано пищеварение, окисление, восстановление.
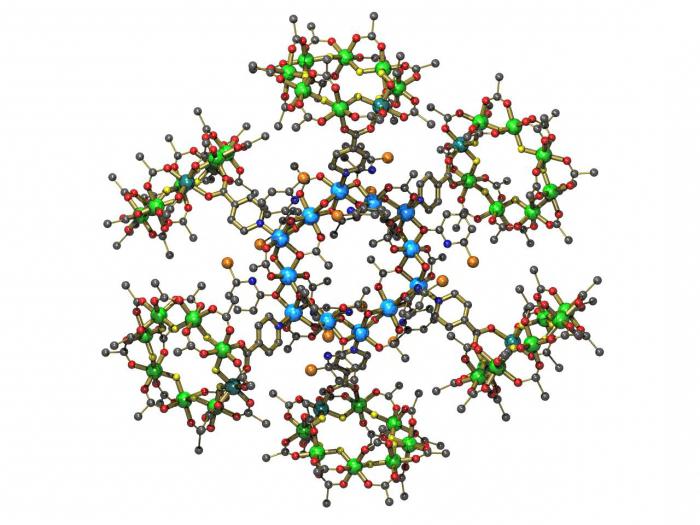
Сходства неорганических и белковых катализаторов
Ферменты как биологические катализаторы имеют ряд свойств, схожих с неорганическими. К таковым можно отнести следующие:
- Ускоряют только термодинамически возможные реакции.
- Не влияют на смещение химического равновесия в равновесных системах, а одинаково ускоряют как прямой, так и обратный процесс.
- В итоге в сфере реакции остаются только продукты, катализатор в их число не входит.
Однако, помимо схожести, существуют еще и отличительные особенности ферментов.
Различия в зависимости от природы
Биологические катализаторы имеют несколько специфических особенностей:
- Высокая степень избирательности. То есть один белок способен активизировать только какую-то определенную реакцию или группу схожих. Чаще всего работает схема "фермент - субстрат одного процесса".
- Чрезвычайно высокая степень активности, ведь некоторые виды белков способны ускорять реакции в миллионы раз.
- Ферменты сильно зависят от условий среды. Проявляют активность только в определенном интервале температур. Также сильно влияет рН среды. Существует кривая, показывающая значения минимума, максимума и оптимума по показателям для каждого фермента.
- Существуют специальные соединения, называемые эффекторами, которые способны угнетать природу биологических катализаторов либо, наоборот, положительно влиять на них.
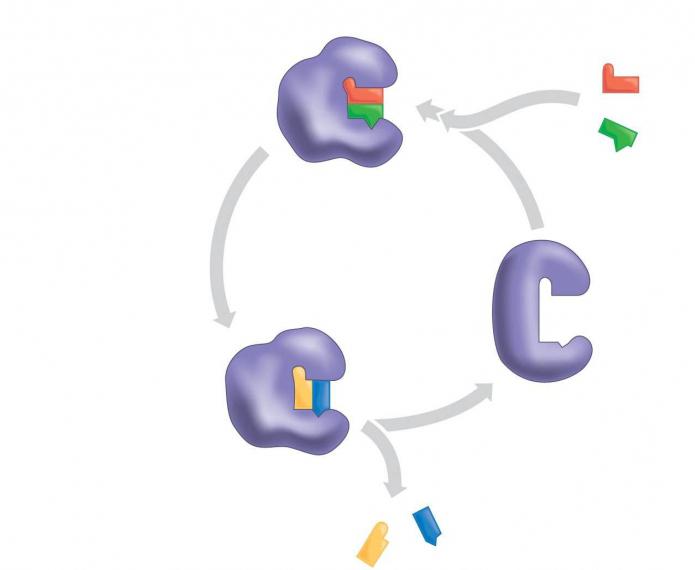
- Субстрат, на котором работает фермент, должен быть строго специфичен. Существует теория, которая носит название ключа и замка. Она описывает механизм действия фермента на субстрате. Катализатор, подобно ключу, встраивается в субстрат своим активным центром, и начинается реакция.
- После процесса фермент частично либо полностью разрушается.
Таким образом, очевидно, что значение белковых катализаторов крайне велико для живых организмов. Однако действие их подчиняется определенным правилам и ограничивается рамками условий окружающей среды.
Изучение катализа в школе
В рамках школьной программы катализаторы изучаются как на химии, так и на биологии. На уроках химии они изучаются с точки зрения веществ, позволяющих осуществлять промышленные синтезы, получать большое количество разнообразных продуктов. На уроках биологии рассматриваются именно биологические катализаторы. 9 класс подразумевает изучение молекулярной биологии и основ биохимии. Поэтому именно на данной ступени образования учащиеся и получают основы знаний о ферментах как действующих веществах в организмах живых существ.
На уроках проводятся опыты, подтверждающие химическую активность данных веществ в определенных температурных интервалах и рН среды:
- исследование действия перекиси водорода как катализатора на сырую и вареную морковь;
- воздействие на мясо (обработанное термически и сырое), картофель и прочие продукты.
Ферменты в организме человека
Каждый школьник, достаточно образованный и перешедший рубеж среднего звена образования, знает, как называются биологические катализаторы. Ферменты в организме имеют строго специфическую специализацию. Поэтому для каждого процесса можно назвать свое катализирующее вещество.
Так, все ферменты организма можно разделить на несколько групп:
- оксидоредуктазы, например, каталаза или алкогольдегидрогеназа;
- трансферазы - кеназа;
- гидролазы, важные для пищеварения: пепсин, амилаза, липопротеинлипаза, эстераза и другие;
- лигазы, например, ДНК-полимераза;
- изомеразы;
- лиазы.
Так как все эти соединения имеют белковую природу, а также комплекс витаминов в составе, то повышение температуры тела чревато денатурацией структуры, а следовательно, прекращением всех биохимических реакций. В этом случае организм близок к смерти. Поэтому высокую температуру тела обязательно сбивают во время болезни.
Использование белковых катализаторов в промышленности
Часто ферменты используются в разных отраслях промышленности:
- химической;
- текстильной;
- пищевой.
На полках магазинов можно видеть чистящие средства и стиральные порошки с содержанием энзимов - это и есть ферменты, улучшающие качество стирки белья.
Для чего нужны биологические катализаторы?
Переоценить их значение сложно. Ведь они не только позволяют живым организмам жить, дышать, питаться, осуществлять процессы метаболизма, но и дают нам возможность уничтожать промышленные отходы, получать лекарства, защищать и оберегать свое здоровье и состояние окружающей среды.


























