Изучая состав вещества, ученые пришли к выводу, что вся материя состоит из молекул и атомов. Долгое время атом (в переводе с греческого "неделимый") считался наименьшей конструкционной единицей вещества. Однако дальнейшие исследования показали, что атом имеет сложное строение и, в свою очередь, включает более мелкие частицы.
Из чего состоит атом?
В 1911 году ученый Резерфорд высказал предположение, что в атоме имеется центральная часть, обладающая положительным зарядом. Так впервые появилось понятие об атомном ядре.

По схеме Резерфорда, названной планетарной моделью, атом состоит из ядра и элементарных частиц с отрицательным зарядом - электронов, движущихся вокруг ядра, подобно тому, как планеты обращаются по орбите вокруг Солнца.
В 1932 году другой ученый, Чедвик, открыл нейтрон - частицу, не имеющую электрического заряда.
Согласно современным представлениям, строение атомного ядра соответствует планетарной модели, предложенной Резерфордом. Ядро несет в себе большую часть атомной массы. Также оно имеет положительный заряд. В атомном ядре находятся протоны - положительно заряженные частицы и нейтроны - частицы, не несущие заряда. Протоны и нейтроны называются нуклонами. Отрицательно заряженные частицы - электроны - движутся по орбите вокруг ядра.
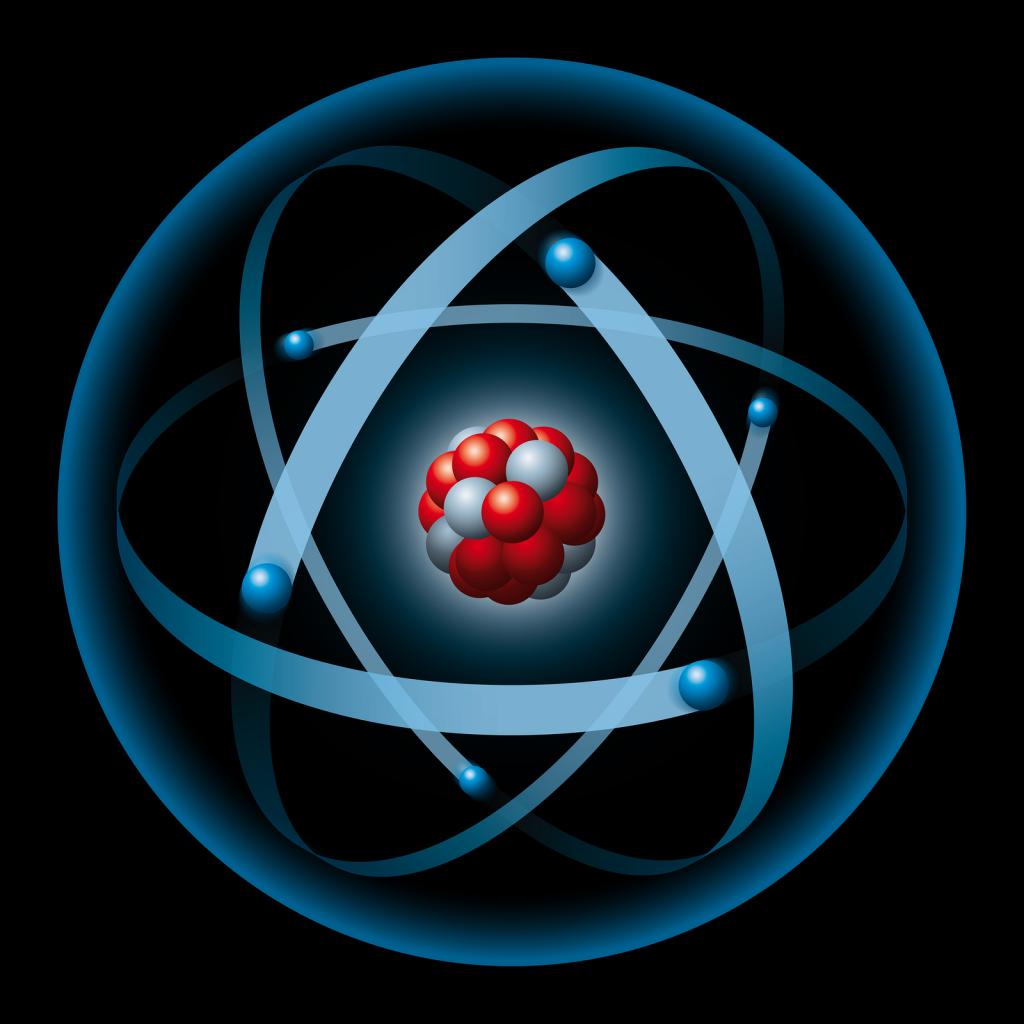
Количество протонов в ядре равняется числу электронов, движущихся по орбите. Следовательно, сам атом является частицей, не несущей заряда. Если атом захватит чужие электроны или потеряет свои, то он становится положительным или отрицательным и называется ионом.
Электроны, протоны и нейтроны обобщенно называют субатомными частицами.
Заряд атомного ядра
Ядро имеет зарядовое число Z. Оно определяется количеством протонов, входящих в состав атомного ядра. Узнать это количество просто: достаточно обратиться к периодической системе Менделеева. Порядковый номер элемента, которому принадлежит атом, равняется количеству протонов в ядре. Таким образом, если химическому элементу кислороду соответствует порядковый номер 8, то количество протонов тоже будет равняться восьми. Поскольку число протонов и электронов в атоме совпадает, то электронов тоже будет восемь.
Количество нейтронов называют изотопическим числом и обозначают буквой N. Их число может различаться в атоме одного и того же химического элемента.
Сумма протонов и электронов в ядре называется массовым числом атома и обозначается буквой А. Таким образом, формула подсчета массового числа выглядит так: А=Z+N.
Изотопы
В случае, когда элементы имеют равное количество протонов и электронов, но разное число нейтронов, их называют изотопами химического элемента. Изотопов может быть один или несколько. Они помещаются в одну и ту же ячейку периодической системы.
Изотопы имеют большое значение в химии и физике. Например, изотоп водорода - дейтерий - в сочетании с кислородом дает совершенно новую субстанцию, которую называют тяжелой водой. Она имеет иную температуру кипения и замерзания, чем обычная. А сочетание дейтерия с другим изотопом водорода - тритием приводит к термоядерной реакции синтеза и может использоваться для выработки огромного количества энергии.

Масса ядра и субатомных частиц
Размеры и масса атомов и субатомных частиц ничтожно малы в представлениях человека. Размер ядер составляется примерно 10-12см. Массу атомного ядра измеряют в физике в так называемых атомных единицах массы - а.е.м.
За одну а.е.м. принимают одну двенадцатую часть массы атома углерода. Используя привычные единицы измерения (килограммы и граммы), массу можно выразить следующим равенством: 1 а.е.м. = 1,660540·10-24г. Выраженная таким образом, она называется абсолютной атомной массой.
Несмотря на то, что атомное ядро является самой массивной составляющей атома, его размеры относительно электронного облака, окружающего его, чрезвычайно малы.
Ядерные силы
Атомные ядра являются чрезвычайно устойчивыми. Это значит, что протоны и нейтроны удерживаются в ядре какими-то силами. Это не могут быть электромагнитные силы, поскольку протоны являются одноименно заряженными частицами, а известно, что частицы, обладающие одинаковым зарядом, отталкиваются друг от друга. Гравитационные силы же слишком слабы, чтобы удержать нуклоны вместе. Следовательно, частицы удерживаются в ядре иным взаимодействием - ядерными силами.

Ядерное взаимодействие считается самым сильным из всех существующих в природе. Поэтому данный тип взаимодействия между элементами атомного ядра называют сильным. Оно присутствует у множества элементарных частиц, как и электромагнитные силы.
Особенности ядерных сил
- Короткодействие. Ядерные силы, в отличие от электромагнитных, проявляются лишь на очень малых расстояниях, сопоставимых с размерами ядра.
- Зарядовая независимость. Данная особенность проявляется в том, что ядерные силы действуют одинаково на протоны и нейтроны.
- Насыщение. Нуклоны ядра взаимодействуют лишь с определенным числом других нуклонов.
Энергия связи ядра
С понятием сильного взаимодействия тесно связано другое - энергия связи ядер. Под энергией ядерной связи понимают то количество энергии, которое требуется, чтобы разделить атомное ядро на составляющие его нуклоны. Она равняется энергии, необходимой для формирования ядра из отдельных частиц.
Для вычисления энергии связи ядра необходимо знать массу субатомных частиц. Вычисления показывают, что масса ядра всегда меньше, чем сумма входящих в его состав нуклонов. Дефектом массы называют разницу между массой ядра и суммой его протонов и электронов. При помощи формулы Эйнштейна о связи массы и энергии (Е=mc2) можно вычислить энергию, выработанную при образовании ядра.
О силе энергии связи ядра можно судить по следующему примеру: при образовании нескольких граммов гелия вырабатывается столько же энергии, сколько при сгорании нескольких тонн каменного угля.
Ядерные реакции
Ядра атомов могут взаимодействовать с ядрами других атомов. Такие взаимодействия называются ядерными реакциями. Реакции бывают двух типов.
- Реакции деления. Они происходят, когда более тяжелые ядра в результате взаимодействия распадаются на более легкие.
- Реакции синтеза. Процесс, обратный делению: ядра сталкиваются, тем самым образуя более тяжелые элементы.
Все ядерные реакции сопровождаются выбросом энергии, которая впоследствии используется в промышленности, в военной сфере, в энергетике и так далее.

Ознакомившись с составом атомного ядра, можно сделать следующие выводы.
- Атом состоит из ядра, содержащего протоны и нейтроны, и электронов, находящихся вокруг него.
- Массовое число атома равняется сумме нуклонов его ядра.
- Нуклоны удерживаются сильным взаимодействием.
- Огромные силы, придающие атомному ядру стабильность, называются энергиями связи ядра.


























