Источники тока химические (сокращенно ХИТ) — приспособления, в которых энергия окислительно-восстановительной реакции преобразуется в электрическую. Другие их названия — электрохимический элемент, гальванический элемент, электрохимическая ячейка. Принцип их действия заключается в следующем: в результате взаимодействия двух реагентов происходит химическая реакция с выделением энергии постоянного электрического тока. В прочих источниках тока процесс получения электроэнергии происходит по многоступенчатой схеме. Сначала выделяется тепловая энергия, затем она превращается в механическую и лишь после этого в электрическую. Преимущество ХИТ — одноступенчатость процесса, то есть электричество получается сразу, минуя стадии получения тепловой и механической энергий.

История
Как появились первые источники тока? Химические источники получили название гальванических элементов в честь итальянского ученого восемнадцатого века — Луиджи Гальвани. Он был врачом, анатомом, физиологом и физиком. Одним из направлений его исследований было изучение реакций животных на различные внешние воздействия. Химический способ получения электроэнергии был открыт Гальвани случайно, во время одного из опытов над лягушками. Он подсоединил к оголенному нерву на лягушачьей лапке две металлические пластины. При этом произошло мускульное сокращение. Собственное объяснение этого явления Гальвани было неверным. Но результаты его опытов и наблюдений помогли его соотечественнику Алессандро Вольта в последующих исследованиях.
Вольта изложил в своих трудах теорию возникновения электрического тока в результате химической реакции между двумя металлами при контакте с мускульной тканью лягушки. Первый химический источник тока выглядел как емкость с соляным раствором, с погруженными в него пластинами из цинка и меди.
В промышленных масштабах ХИТ начали производиться еще во второй половине девятнадцатого века, благодаря французу Лекланше, который изобрел первичный марганцево-цинковый элемент с солевым электролитом, названный его именем. Через несколько лет эта электрохимическая ячейка была усовершенствована другим ученым и являлась единственным первичным химическим источником тока до 1940 года.
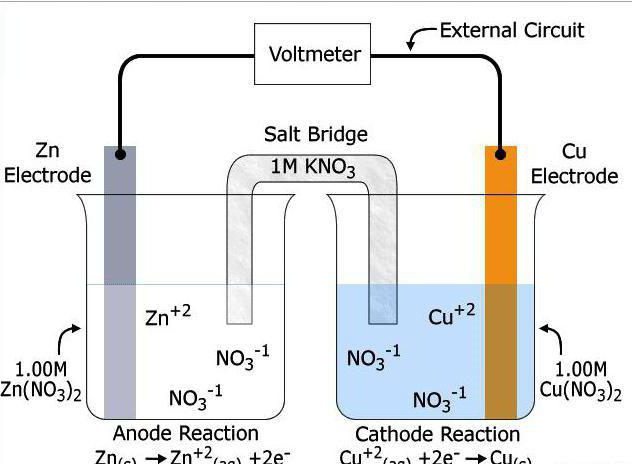
Устройство и принцип работы ХИТ
Устройство химических источников тока включает в себя два электрода (проводники первого рода) и находящийся между ними электролит (проводник второго рода, или ионный проводник). На границе между ними возникает электронный потенциал. Электрод, на котором происходит окисление восстановителя называют анодом, а тот, на котором происходит восстановление окислителя, — катодом. Вместе с электролитом они составляют электрохимическую систему.
Побочным результатом окислительно-восстановительной реакции между электродами является возникновение электрического тока. Во время такой реакции восстановитель окисляется и отдает электроны окислителю, который их принимает и за счет этого восстанавливается. Присутствие между катодом и анодом электролита является необходимым условием реакции. Если просто смешать между собой порошки из двух разных металлов, никакого выделения электроэнергии не произойдет, вся энергия выделится в виде тепла. Электролит нужен, чтобы упорядочить процесс перехода электронов. Чаще всего в его качестве выступает солевой раствор или расплав.
Электроды выглядят как металлические пластины или решетки. При их погружении в электролит возникает разность электрических потенциалов между ними — напряжение разомкнутой цепи. Анод имеет тенденцию к отдаче электронов, а катод - к их принятию. На их поверхности начинаются химические реакции. Они прекращаются при размыкании цепи, а также когда израсходован один из реагентов. Размыкание цепи происходит при удалении одного из электродов или электролита.

Состав электрохимических систем
Источники тока химические в качестве окислителей используют кислородсодержащие кислоты и соли, кислород, галоиды, высшие оксиды металлов, нитроорганические соединения и т. д. Восстановителями в них являются металлы и их низшие оксиды, водород и углеводородные соединения. Как электролиты используются:
- Водные растворы кислот, щелочей, солевые и т. д.
- Неводные растворы с ионной проводимостью, полученные при растворении солей в органических или неорганических растворителях.
- Расплавы солей.
- Твердые соединения с ионной решеткой, в которой один из ионов подвижен.
- Матричные электролиты. Это жидкие растворы или расплавы, находящиеся в порах твердого непроводящего тела — электроносителя.
- Ионообменные электролиты. Это твердые соединения с фиксированными ионогенными группами одного знака. Ионы другого знака при этом подвижны. Это свойство делает проводимость такого электролита униполярной.

Гальванические батареи
Источники тока химические состоят из гальванических элементов — ячеек. Напряжение в одной из таких ячеек невелико — от 0,5 до 4В. В зависимости от потребности, в ХИТ используют гальваническую батарею, состоящую из нескольких последовательно соединенных элементов. Иногда применяется параллельное или последовательно-параллельное соединение нескольких элементов. В последовательную цепь всегда включают исключительно одинаковые первичные ячейки или аккумуляторы. Они должны иметь одни и те же параметры: электрохимическую систему, конструкцию, технологический вариант и типоразмер. Для параллельного соединения допустимо использование элементов разного типоразмера.

Классификация ХИТ
Химические источники тока отличаются по:
- размеру;
- конструкции;
- реагентам;
- природе энергообразующей реакции.
Эти параметры определяют эксплуатационные свойства ХИТ, подходящие для конкретной области применения.
Классификация электрохимических элементов основана на различии в принципе работы устройства. В зависимости от этих характеристик, различают:
- Первичные химические источники тока — элементы одноразового действия. В них имеется определенный запас реагентов, который расходуется при реакции. После полного разряда такая ячейка теряет работоспособность. По-другому первичные ХИТ называют гальваническими элементами. Верным будет и называть их просто — элемент. Самые простые примеры первичного источника питания — "батарейка" А-А.
- Перезаряжаемые химические источники тока — аккумуляторы (их также называют вторичными, обратимыми ХИТ) являются многоразовыми элементами. Путем пропускания тока от внешней цепи в обратном направлении через аккумулятор после полного разряда израсходованные реагенты регенерируются, вновь накапливая химическую энергию (заряжаясь). Благодаря возможности подзарядки от внешнего постоянного источника тока это устройство используется в течение долгого времени, с перерывами на подзарядку. Процесс выработки электрической энергии называется разрядом аккумулятора. К таким ХИТ можно отнести элементы питания многих электронных устройств (ноутбуки, мобильные телефоны и т. п.).
- Тепловые химические источники тока — приборы непрерывного действия. В процессе их работы происходит непрерывное поступление новых порций реагентов и удаление продуктов реакции.
- В комбинированных (полутопливных) гальванических элементах имеется запас одного из реагентов. Второй подается в устройство извне. Срок работы устройства зависит от запаса первого реагента. Комбинированные химические источники электрического тока используются как аккумуляторы, если есть возможность восстановления их заряда путем пропускания тока от внешнего источника.
- ХИТ возобновляемые перезаряжаются механическим или химическим путем. Для них существует возможность замены после полного разряда израсходованных реагентов на новые порции. То есть они не являются устройствами непрерывного действия, а, подобно аккумуляторам, периодически подзаряжаются.

Характеристики ХИТ
К основным характеристикам химических источников тока относятся:
- Напряжение разомкнутой цепи (НРЦ или разрядное напряжение). Этот показатель, прежде всего, зависит от выбранной электрохимической системы (сочетание восстановителя, окислителя и электролита). Также на НРЦ влияют концентрация электролита, степень разряженности, температура и другое. НРЦ зависит от значения проходящего через ХИТ тока.
- Мощность.
- Ток разряда — зависит от сопротивления внешней цепи.
- Емкость — максимальной количество электричества, которое ХИТ отдает при полном его разряде.
- Энергозапас — максимальная энергия, получаемая при полном разряде устройства.
- Энергетические характеристики. Для аккумуляторов, это, прежде всего, гарантированное количество зарядно-разрядных циклов без снижения емкости или напряжения заряда (ресурс).
- Температурный диапазон работоспособности.
- Срок сохраняемости — максимально допустимый промежуток времени между изготовлением и первым разрядом устройства.
- Срок службы — максимально допустимый общий срок хранения и работы. Для топливных элементов значение имеют сроки службы при непрерывной и прерывистой работе.
- Общая энергия, отдаваемая за весь срок службы.
- Механическая прочность по отношению к вибрации, ударам и т. п.
- Возможность работы в любом положении.
- Надежность.
- Простота в обслуживании.
Требования к ХИТ
Конструкция электрохимических элементов должна обеспечивать условия, способствующие наиболее эффективному протеканию реакции. К этим условиям относятся:
- предотвращение утечек тока;
- равномерная работа;
- механическая прочность (в том числе герметичность);
- разделение реагентов;
- хороший контакт между электродами и электролитом;
- отвод тока от зоны реакции до внешнего вывода с минимальными потерями.
Источники тока химические должны отвечать следующим общим требованиям:
- самые высокие значения удельных параметров;
- максимальный температурный интервал работоспособности;
- самое большое напряжение;
- минимальная стоимость единицы энергии;
- стабильность напряжения;
- сохранность заряда;
- безопасность;
- простота обслуживания, а в идеале отсутствие необходимости в нем;
- длительный срок службы.
Эксплуатация ХИТ
Главное преимущество первичных гальванических элементов — отсутствие необходимости какого-либо обслуживания. Перед началом их использования достаточно провести проверку внешнего вида, срока годности. При подключении важно соблюсти полярность и проверить целостность контактов прибора. Более сложные химические источники тока — аккумуляторы, требуют уже более серьезного ухода. Цель их обслуживания — максимальное продление срока службы. Уход за аккумуляторной батареей заключается в:
- поддержании чистоты;
- контроле напряжения разомкнутой цепи;
- поддержании уровня электролита (для доливки можно использовать только дистиллированную воду);
- контроле концентрации электролита (с помощью ареометра — простого прибора для измерения плотности жидкостей).
При эксплуатации гальванических элементов необходимо соблюдать все требования, относящиеся к безопасному использованию электроприборов.
Классификация ХИТ по электрохимическим системам
Виды химических источников тока, в зависимости от системы:
- свинцовые (кислотные);
- никель-кадмиевые, никель-железные, никель-цинковые;
- марганцево-цинковые, медно-цинковые, ртутно-цинковые, хлорно-цинковые;
- серебряно-цинковые, серебряно-кадмиевые;
- воздушно-металлические;
- никель-водородные и серебряно-водородные;
- марганцево-магниевые;
- литиевые и т. д.
Современное применение ХИТ
Источники тока химические в настоящее время применяются в:
- транспортных средствах;
- переносных приборах;
- военной и космической технике;
- научном оборудовании;
- медицине (электрокардиостимуляторы).
Привычные примеры ХИТ в быту:
- батарейки (сухие батареи);
- аккумуляторные батареи переносных бытовых приборов и электроники;
- источники бесперебойного питания;
- автомобильные аккумуляторы.
Особенно широкое применение получили литиевые химические источники тока. Это связано с тем, что литий (Li) обладает самой высокой удельной энергией. Дело в том, что он отличается самым отрицательным электродным потенциалом среди всех прочих металлов. Литий-ионные аккумуляторы (ЛИА) опережают все прочие ХИТ по величинам удельной энергии и рабочего напряжения. Сейчас они постепенно осваивают новую сферу — автомобильный транспорт. В дальнейшем разработки ученых, связанные с усовершенствованием литиевых элементов питания, будут двигаться в направлении сверхтонких конструкций и крупных сверхмощных аккумуляторных батарей.




























