Массовая концентрация раствора является одним из распространенных понятий в современной химии. В статье мы выявим особенности растворов, их виды, применение. Отметим некоторые примеры расчета разных видов концентраций.
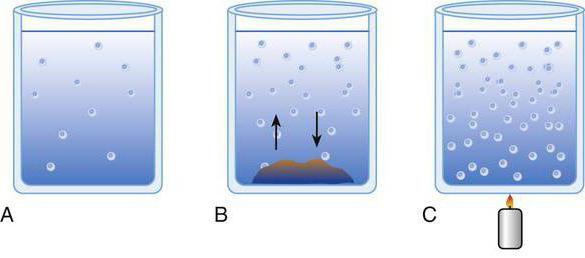
Особенности растворов
Раствор - это однородная система, имеющая переменный состав. Из двух компонентов раствора один всегда выступает в качестве среды. Именно в ней будут растворяться структурные фрагменты других веществ. Ее называют растворителем, внутри которого и располагаются молекулы растворенного вещества.
Если смешивается два газообразных вещества, то в таком случае не выделяют растворителя. Для каждой конкретной ситуации всегда проводятся специальные расчеты.
Получение однородных систем
Для получения однородных растворов необходимо дробление растворенных веществ до структурных единиц. Только в таком случае системы будут истинными. При раздроблении до небольших капелек, песчинок, которые будут распределяться в среде, получают коллоидные растворы, эмульсии, суспензии.
Применение растворов
Кстати, в строительстве смесь песка, цемента, воды тоже называют раствором, но с химической точки зрения он представляет собой суспензию. Практическое значение растворов можно объяснить по разным причинам.
Химические реакции в жидких растворах происходят в объеме растворителя. Это делает их доступными для реакции без любого дополнительного действия на систему. В смеси, содержащей твердые частицы, невозможно провести реакцию в полном объеме. Чтобы ускорить процесс, потребуется соприкосновение частиц в некоторых точках. Для повышения скорости реакции перетирают кристаллы в ступке, затем их прессуют. Но не сразу можно достигнуть полноты протекания процесса.
В растворе же протекает процесс иначе. Молекулы движутся свободно, при их столкновениях происходят химические превращения. Энергия, которая начинает выделяться в таком взаимодействии, аккумулируется растворителем, система практически не разогревается.

Физические свойства и концентрация растворов
Массовая доля вещества позволяет определять количественное соотношение растворенного вещества и растворителя, взятое для их приготовления. Металлические сплавы, кстати, тоже являются растворами, но твердыми, характеризующимися определенными физическими параметрами.
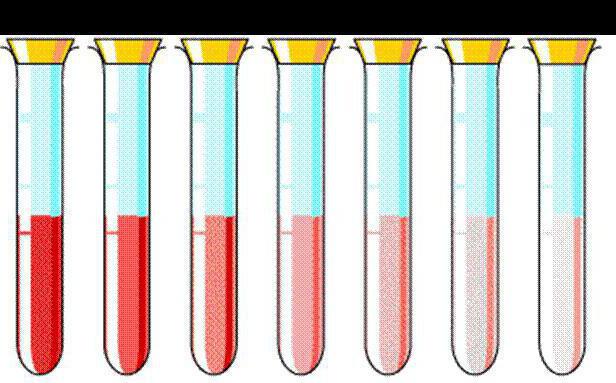
Растворы обладают способностью менять силы действия растворенного компонента. Это делает их востребованными в сельском хозяйстве, медицине. Например, раствор марганцовки (перманганата калия) используют для обработки ссадин и ран в средней концентрации. Но практическое значение имеет и его незначительная концентрация. Так, массовая доля вещества 2-3% придает раствору слабо-розовый цвет, востребованный для промывания желудка.
Темные фиолетовые кристаллы перманганата калия не применяют в медицинских целях, поскольку они обладают сильными окислительными свойствами. Вообще, интенсивность окраски напрямую связана с тем, какова его концентрация. Массовая доля вещества позволяет регулировать токсичность готового раствора.

Массовая доля
Как вычисляется подобная концентрация? Массовая доля вещества характеризуется отношением массы вещества к массе раствора, взятого в процентах. На их органолептические свойства оказывает влияние не только то, что будет растворяться, но и количественный показатель. Например, для слабого раствора поваренной соли почти не характерен привкус, а при больших концентрациях он проявляется в разной степени.
Как на практике определяется концентрация? Массовая доля вещества в растворе рассматривается в школьном курсе неорганической химии. Задачи на ее определение включены в тестовые задания для выпускников 9 класса.
Приведем пример задания, в котором используется концентрация.
Массовая доля поваренной соли 25%. Масса раствора 250 граммов. Определите массу воды, содержащейся в нем. Для проведения вычислений сначала нужно выяснить массу вещества. Исходя из пропорции, получаем, что вещества в растворе 62,5 грамма. Для определения массы воды нужно вычесть из 250 граммов массу самого вещества, в результате получаем 187,5 г.

Виды концентраций
Что такое концентрация? Массовых долей в растворе может содержаться не более ста процентов. В химии термин «концентрация» предполагает некое содержание растворенного вещества. Существует несколько ее вариантов: молярная, массовая концентрация.
Например, если необходимо приготовить раствор из 80 граммов воды и 20 граммов поваренной соли и определить массовые доли вещества в растворе, сначала нужно определить массу раствора. Она составит сто граммов. Процентное содержание вещества получается 20 процентов.
Мы проанализировали, что представляет собой массовая доля. Молярная концентрация предполагает отношение количества вещества к объему взятого раствора. Чтобы приготовить раствор с заданной молярной концентрацией, сначала определяют массу вещества. Затем взвешивают его нужное количество и растворяют в литре растворителя.
Расчет молярной концентрации
Так, для приготовления 2 литров раствора с концентрацией 0,15 моль/л сначала рассчитывают массу соли, которая содержится в растворе. Для этого нужно разделить 0,15 моль на 2 литра, получаем 0,075 моль. Теперь вычисляем массу: 0,075 моль умножаем на 58,5 г/моль. Результат - 4,39 г.
Задачи аналитической химии
В качестве прикладной химической задачи рассматривают анализ. С его помощью выявляют состав смеси, проводят диагностические пробы, анализируют горные породы. Для этого нужно определять качественный и количественный состав раствора.
Среди тех задач, которые чаще всего встречаются в неорганической химии, выделим определение концентрации одного вещества по заданной величине у другого вещества. С помощью опытов можно осуществить постепенное добавление к раствору, у которого известна молярная концентрация, искомого раствора. Данный процесс называется титрованием.
Растворимость и растворители
Самым распространенным растворителем является вода. В ней отлично растворяются основания, кислоты, соли, некоторые органические соединения. Именно водные растворы являются самыми распространенными в природе системами. Вода выполняет функцию биологического растворителя. Она считается основой для протекания многих сред: крови, цитозолей, межклеточных жидкостей. Многие типы животных и растений живут именно в водной среде.
Растворимостью называют свойство вещества растворяться в выбранном растворителе. Это сложное явление, которое требует учета определенных нюансов и особенностей строения растворителя.
В качестве хороших органических веществ можно отметить спирты. Они в свой состав включают гидрокисльные группы, поэтому имеют высокую растворимость.

Заключение
Любая жидкость может рассматриваться в качестве растворителя. Именно поэтому часто ведут речь о взаимной растворимости разных жидких веществ. К примеру, среди органических веществ можно упомянуть о растворимости в воде сложных эфиров.
Различные виды концентраций, используемые в неорганической и органической химии, помогают проводить качественные и количественные определения веществ. Теория растворов востребована в аналитической химии, фармацевтике и современной медицине.


























