У всех организмов (исключение составляют некоторые вирусы) реализация генетического материала происходит по системе ДНК-РНК-белок. На первом этапе информация переписывается (транскрибируется) с одной нуклеиновой кислоты на другую. Белки, которые регулируют этот процесс, называются факторами транскрипции.
Что такое транскрипция
Транскрипция представляет собой биосинтез молекулы РНК на основе ДНК-матрицы. Это возможно благодаря комплементарности определенных азотистых оснований, входящих в состав нуклеиновых кислот. Синтез осуществляется специализированными ферментами – РНК-полимеразами и контролируется множеством регуляторных белков.
Транскрибируется не сразу весь геном, а лишь определенный его участок, называемый транскриптоном. В состав последнего входят промотор (место присоединения РНК-полимеразы) и терминатор (последовательность, активирующая завершение синтеза).
Транскриптон прокариот представляет собой оперон, состоящий из нескольких структурных генов (цистронов). На его основе синтезируется полицистронная РНК, содержащая информацию об аминокислотной последовательности группы функционально родственных белков. В транскриптон эукариот входит только один ген.
Биологическая роль процесса транскрипции заключается в формировании матричных последовательностей РНК, на основании которой в рибосомах осуществляется белковый синтез (трансляция).
Синтез РНК у прокариотов и эукариотов
Схема синтеза РНК одинакова для всех организмов и включает 3 стадии:
- Инициация – присоединение полимеразы к промотору, активация процесса.
- Элонгация – наращивание нуклеотидной цепи в направлении от 3´к 5´ концу с замыканием фосфодиэфирных связей между азотистыми основаниями, которые подбираются комплементарно мономерам ДНК.
- Терминация – завершение процесса синтеза.
У прокариотов все виды РНК транскрибируются одной РНК-полимеразой, состоящей из пяти протомеров (β, β′, ω и двух субъединиц α), которые в совокупности образуют кор-фермент, способный наращивать цепь рибонуклеотидов. Есть еще дополнительная единица σ, без которой невозможно присоединение полимеразы к промотору. Комплекс из кора и сигма-фактора называется холоферментом.
Несмотря на то что субъединица σ не всегда ассоциирована с кором, она считается частью РНК-полимеразы. В диссоциированом состоянии сигма не способна связываться с промотором, – только в составе холофермента. После завершения инициации этот протомер отделяется от кора, заменяясь фактором элонгации.
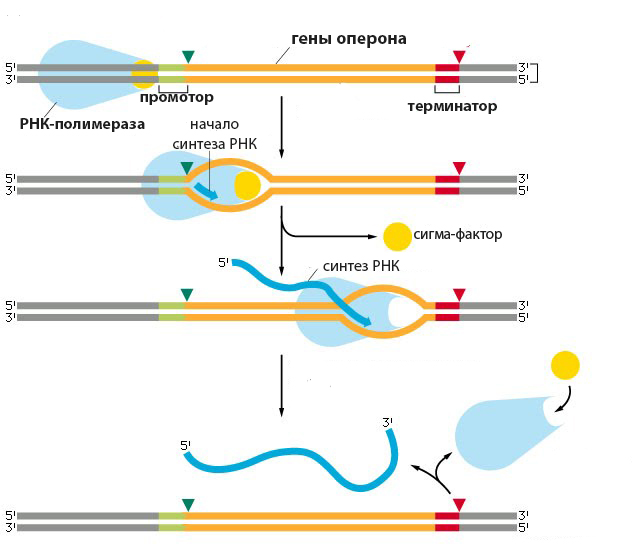
Особенностью прокариот является сочетание процессов трансляции и транскрипции. К начавшей синтезироваться РНК тут же присоединяются рибосомы и строят аминокислотную цепь. Остановка транскрипции происходит за счет образования шпилечной структуры в области терминатора. На этом этапе комплекс ДНК-полимераза-РНК распадается.
В клетках эукариот транскрипция осуществляется тремя ферментами:
- РНК-полимераза l – синтезирует 28S и 18S-рибосомальные РНК.
- РНК-полимераза ll – транскрибирует гены, кодирующие белки и малые ядерные РНК.
- РНК-полимераза lll – отвечает за синтез тРНК и 5S рРНК (малая субъединица рибосом).
Ни один из этих ферментов не способен инициировать транскрипцию без участия специфических белков, обеспечивающих взаимодействие с промотором. Суть процесса такая же, как и у прокариотов, но каждый этап протекает значительно сложнее с участием большего числа функциональных и регуляторных элементов, в том числе хроматин-модифицирующих. Только на стадии инициации задействовано около сотни белков, включая ряд транскрипционных факторов, тогда как у бактерий для связи с промотором достаточно одной субъединицы сигма и иногда нужна помощь активатора.
Важнейший вклад биологической роли транскрипции в процессах биосинтеза различных типов белков определяет необходимость существования строгой системы контроля считывания генов.
Регуляция транскрипции
Ни в одной клетке генетический материал не реализуется в полном объеме: транскрибируется только часть генов, а остальные неактивны. Это возможно благодаря сложным механизмам регуляции, определяющим, с каких участков ДНК и в каком количестве будут синтезироваться РНК-последовательности.
У одноклеточных организмов дифференциальная активность генов имеет адаптивное значение, тогда как у многоклеточных она еще и обуславливает процессы эмбриогенеза и онтогенеза, когда на основании одного генома формируются разные типы тканей.
Контроль экспрессии генов осуществляется на нескольких уровнях. Самым важным этапом является регуляция транскрипции. Биологический смысл этого механизма заключается в поддержании необходимого количества различных белков, требуемых клетке или организму в конкретный момент существования.
Существует корректировка биосинтеза и на других уровнях, таких как процессинг, трансляция и транспорт РНК из ядра в цитоплазму (последнее отсутствует у прокариотов). При позитивной регуляции эти системы отвечают за производство белка на основе активированного гена, в чем и заключается биологический смысл транскрипции. Однако на любом из этапов цепочка может быть приостановлена. Некоторые особенности регуляции у эукариотов (альтернативные промоторы, сплайсинг, модификация сайтов полиаденелирования) приводят к появлению различных вариантов белковых молекул на основании одной ДНК-последовательности.
Так как формирование РНК – это первый этап дешифровки генетической информации на пути к биосинтезу белка, биологическая роль процесса транскрипции в модификации клеточного фенотипа гораздо значительней, чем регуляция процессинга или трансляции.
Определение активности конкретных генов как у прокариотов, так и у эукариотов происходит на стадии инициации при помощи специфических переключателей, к которым относят регуляторные области ДНК и транскрипционные факторы (ТФ). Работа таких переключателей не автономна, а находится под строгим контролем других клеточных систем. Есть также механизмы неспецифической регуляции синтеза РНК, обеспечивающие нормальное прохождение инициации, элонгации и терминации.
Понятие о транскрипционных факторах
В отличие от регуляторных элементов генома, факторы транскрипции по химической природе являются белками. Связываясь с определенными участками ДНК, они могут активировать, ингибировать, ускорять или замедлять процесс транскрипции.
В зависимости от производимого эффекта факторы транскрипции прокариот и эукариот можно разделить на две группы: активаторы (инициируют или увеличивают интенсивность синтеза РНК) и репрессоры (подавляют или угнетают процесс). В настоящий момент у различных организмов в совокупности обнаружено более 2000 ТФ.
Регуляция транскрипции у прокариотов
У прокариотов контроль синтеза РНК происходит преимущественно на стадии инициации за счет взаимодействия ТФ со специфической областью транскриптона – оператором, который располагается рядом с промотором (иногда пересекаясь с ним) и, по сути, является посадочной площадкой для регуляторного белка (активатора или репрессора). Для бактерий характерен еще один способ дифференциального контроля генов – синтез альтернативных σ-субъединиц, предназначенных для разных групп промоторов.
Частично экспрессия оперона может регулироваться на стадиях элонгации и терминации, но уже не за счет связывающихся с ДНК ТФ, а благодаря белкам, взаимодействующим с РНК-полимеразой. К ним относят Gre-белки и антитерминаторные факторы Nus и RfaH.
На элонгацию и терминацию транскрипции у прокариотов определенным образом влияет происходящий параллельно синтез белка. У эукариотов как сами эти процессы, так и факторы транскрипции и трансляции пространственно разделены, а значит, функционально не связаны.
Активаторы и репрессоры
У прокариотов есть два механизма регуляции транскрипции на стадии инициации:
- позитивная – осуществляется белками-активаторами;
- негативная – контролируется репрессорами.
При позитивной регуляции присоединение фактора к оператору активирует ген, а при негативной, наоборот, выключает. Способность регуляторного белка связываться с ДНК зависит от присоединения лиганда. В роли последнего обычно выступают низкомолекулярные клеточные метаболиты, которые в таком случае выполняют роль коактиваторов и корепрессоров.
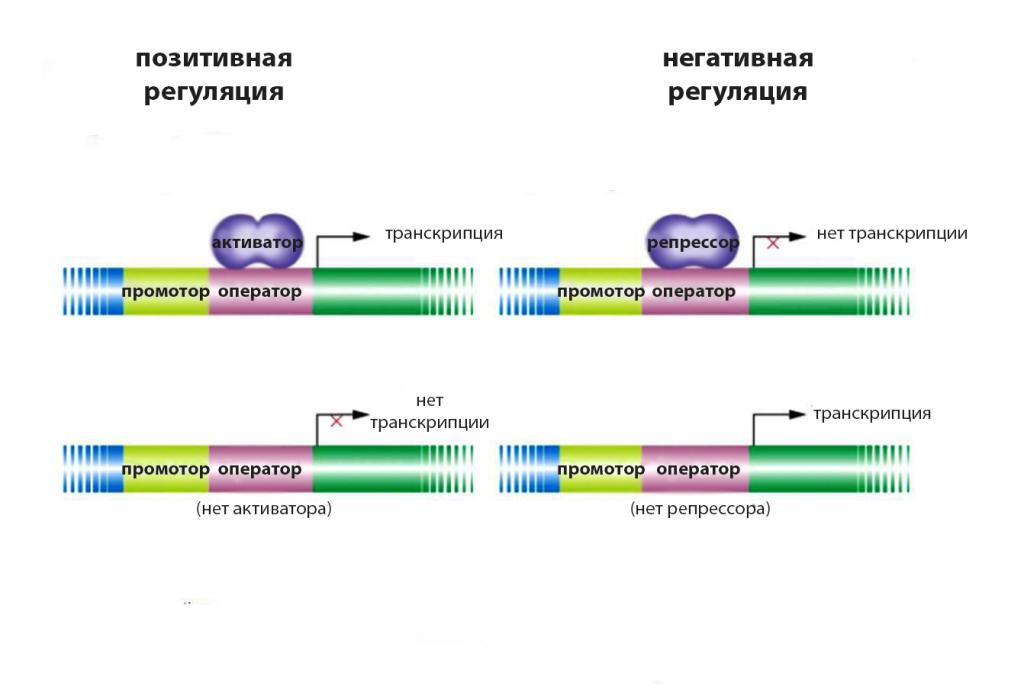
Механизм действия репрессора основан на перекрывании областей промотора и оператора. В оперонах с такой структурой присоединение белкового фактора к ДНК закрывает часть посадочной площадки для РНК-полимеразы, не давая последней инициировать транскрипцию.
Активаторы работают на слабых промоторах с низкой функциональностью, которые плохо распознаются РНК-полимеразами или с трудом поддаются плавлению (разделению цепей спирали ДНК, необходмому для начала транскрипции). Присоединясь к оператору, белковый фактор взаимодействует с полимеразой, значительно повышая вероятность инициации. Активаторы способны увеличивать интенсивность транскрипции в 1000 раз.
Некоторые ТФ прокариот могут действовать и как активаторы, и как репрессоры в зависимости от расположения оператора по отношению к промотору: если эти области перекрываются, фактор ингибирует транскрипцию, а в противном случае – запускает.
| Функция лиганда по отношению к фактору | Состояние лиганда | Негативная регуляция | Позитивная регуляция |
| Обеспечивает отделение от ДНК | Присоединение | Удаление белка-репрессора, активация гена | Удаление белка-активатора, выключение гена |
| Присоединяет фактор к ДНК | Удаление | Удаление репрессора, включение транскрипции | Удаление активатора, выключение транскрипции |
Негативную регуляцию можно рассмотреть на примере триптофанового оперона бактерии E. coli, для которого характерно расположение оператора внутри последовательности промотора. Белок-репрессор активируется присоединением двух молекул триптофана, которые изменяют угол наклона ДНК-связывающего домена таким образом, чтобы он мог войти в большую бороздку двойной спирали. При низкой концентрации триптофана репрессор теряет лиганд и вновь становится неактивны. Иными словами, частота инициации транскрипции обратно-пропорциональна количеству метаболита.
Некоторые опероны бактерий (например, лактозный) сочетают позитивный и негативный механизмы регуляции. Такая система необходима тогда, когда одного сигнала для рационального контроля экспрессии недостаточно. Так, лактозный оперон кодирует ферменты, траспортирующие внутрь клетки, а затем расщепляющие лактозу – альтернативный источник энергии, менее выгодный, чем глюкоза. Поэтому только при низкой концентрации последней белок CAP связывается с ДНК и запускает транскрипцию. Однако это целесообразно только при наличии лактозы, отсутствие которой приводит к активации Lac-репрессора, блокирующего доступ полимеразы к промотору даже при наличии функциональной формы белка-активатора.
Благодаря оперонной структуре у бактерий несколько генов контролируется одной регуляторной областью и 1-2 ТФ, тогда как у эукариотов на один-единственный ген приходится большое количество регуляторных элементов, каждый из которых зависим от множества других факторов. Такая сложность соответствует высокому уровню организации эукариот, и особенно – многоклеточных организмов.
Регуляция синтеза мРНК у эукариотов
Контроль экспрессии эукариотических генов определяется совокупным действием двух элементов: белковых фактов транскрипции (ТФ) и регуляторных последовательностей ДНК, которые могут находиться рядом с промотором, намного выше него, в интронах либо после гена (имеется в виду кодирующая область, а не ген в полном значении).
Некоторые участки выполняют функцию переключателей, а другие не взаимодействуют напрямую с ТФ, но придают молекуле ДНК гибкость, необходимую для формирования петлеобразной структуры, сопровождающей процесс транскрипционной активации. Такие участки называются спейсерами. Все регуляторные последовательности вместе с промотором составляют контролирующую область гена (gene conrol region).
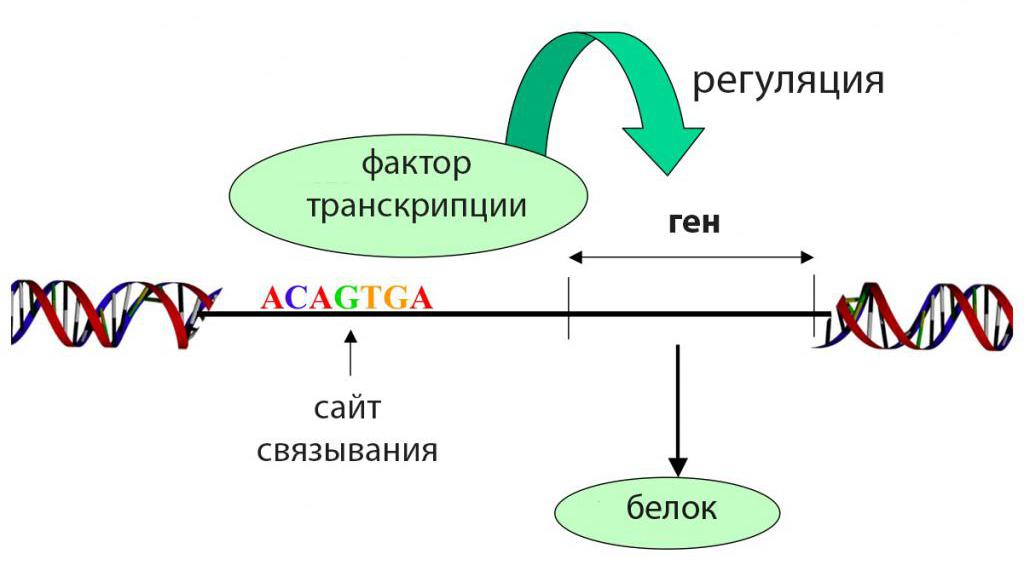
Стоит отметить, что действие самих транскрипционных факторов является лишь частью сложной многоуровневой регуляции генетической экспрессии, в которой огромное количество элементов складываются в результирующий вектор, определяющий, будет ли в итоге с конкретного участка генома синтезироваться РНК.
Дополнительным фактором контроля транскрипции в ядерной клетке служит изменение структуры хроматина. Здесь присутствует как тотальная регуляция (обеспечивается распределением участков гетерохроматина и эухроматина), так и локальная, связанная с конкретным геном. Для работы полимеразы должны быть устранены все уровни компактизации ДНК, включая нуклеосомный.
Разнообразие факторов транскрипции у эукариотов связано с большим количеством регуляторов, к которым относят усилители, глушители (энхансеры и сайленсоры), а также адаптерные элементы и инсуляторы. Эти участки могут находиться как вблизи, так и на значительном расстоянии от гена (до 50 тыс н. п.).
Энхансеры, сайленсоры и адаптерные элементы
Энхансеры – это короткие последовательные ДНК, способные при взаимодействии с регуляторным белком запускать транскрипцию. Приближение усилителя к промоторной области гена осуществляется за счет образования петлеобразной структуры ДНК. Связывание активатора с энхансером либо стимулирует сборку комплекса инициации, либо помогает полимеразе перейти к элонгации.
Энхансер имеет сложное строение и состоит из нескольких сайтов-модулей, каждому из которых соответствует свой регуляторный белок.
Сайленсоры – это участки ДНК, которые подавляют или полностью исключают возможность транскрипции. Механизм работы такого переключателя пока неизвестен. Одним из предположительных способов является окупирование больших областей ДНК особыми белками группы SIR, которые закрывают доступ факторам инициации. В таком случае выключаются все гены, расположенные в пределах нескольких тысяч нуклеотидных пар от сайленсора.
Адаптерные элементы в комплексе со связывающимися с ними ТФ составляют отдельный класс генетических переключателей, избирательно реагирующих на стероидные гормоны, циклическую АМФ и глюкокортикоиды. Этот регуляторный блок отвечает за реакцию клетки на тепловой шок, воздействие металлов и некоторых химических соединений.
В числе контролирующих участков ДНК выделяют еще один тип элементов – инсуляторы. Это специфические последовательности, которые препятствуют влиянию факторов транскрипции на отдаленные гены. Механизм действия инсуляторов до сих пор не выяснен.
Транскрипционные факторы эукариот
Если у бактерий транскрипционные факторы имеют только регуляторную функцию, то в ядерных клетках есть целая группа ТФ, обеспечивающих фоновую инициацию, но при этом напрямую зависящих от связывающихся с ДНК белков-регуляторов. Количество и разнообразие последних у эукариотов огромно. Так, в организме человека доля последовательностей, кодирующих белковые факторы транскрипции, составляет около 10 % генома.
На настоящий момент ТФ эукариот изучены недостаточно, как и механизмы работы генетических переключателей, устройство которых намного сложнее моделей позитивной и негативной регуляции у бактерий. В отличие от последних, на активность факторов транскрипции ядерной клетки влияет не один-два, а десятки и даже сотни сигналов, которые могут взаимно усиливать, ослаблять или исключать друг друга.
С одной стороны, для активации конкретного гена требуется целая группа транскрипционных факторов, но с другой - одного регуляторного белка может быть достаточно, чтобы запустить экспрессию нескольких генов по механизму каскада. Вся эта система представляет собой сложнейшую вычислительную машину, обрабатывающую сигналы от разных источников (как внешних, так и внутренних) и складывающую их эффекты в конечный результат со знаком "плюс" или "минус".
Регуляторные факторы транскрипции у эукариотов (активаторы и репрессоры) взаимодействуют не с оператором, как у бактерий, а с рассеянными по ДНК контролирующими участками и влияют на инициацию через посредников, в качестве которых могут выступать белки медиатора, факторы комплекса инициации и ферменты, изменяющие структуру хроматина.
За исключением некоторых ТФ, входящих в преинициаторный комплекс, все транскрипционные факторы имеют в своем составе ДНК-связывающий домен, который отличает их от других многочисленных белков, обеспечивающих нормальное прохождение транскрипции или выступающих в роли посредников при ее регуляции.
Последние исследования доказали, что ТФ эукариотов могут влиять не только на инициацию, но и на элонгацию транскрипции.
Разнообразие и классификация
У эукариотов выделяют 2 группы белковых факторов транскрипции: базальные (иначе называются общими или главными) и регуляторные. Первые отвечают за распознавание промоторов и создание преинициаторного комплекса. Необходимы для начала транскрипции. Эта группа насчитывает несколько десятков белков, которые всегда присутствуют в клетке и не влияют на дифференциальную экспрессию генов.
Комплекс из базальных факторов транскрипции представляет собой инструмент, по функции аналогичный сигма-субъединице у бактерий, только более сложный и подходящий для всех видов промоторов.
Факторы другого типа влияют на транскрипцию за счет взаимодействия с регуляторными последовательностями ДНК. Так как эти ферменты ген-специфичны, их насчитывается огромное количество. Связываясь с участками конкретных генов, они контролируют секрецию определенных белков.
Классификация факторов транскрипции у эукариотов основана на трех принципах:
- механизм действия;
- условия функционирования;
- структура ДНК-связывающего домена.
По первому признаку различают 2 класса факторов: базальные (взаимодействуют с промотором) и связывающиеся с upstream-участками (расположенными выше гена регуляторными областями). Этот вид классификации по сути соответствует функциональному делению ТФ на общие и специфические. Upstream-факторы делятся на 2 группы в зависимости от необходимости в дополнительной активации.
По особенностям функционирования различают конститутивные ТФ (всегда присутствуют в любой клетке) и индуцируемые (свойственны не всем типам клеток и могут требовать определенных механизмов активации). Факторы второй группы, в свою очередь, подразделяются на клетко-специфичные (участвуют в онтогенезе, характеризуются строгим контролем экспрессии, но не требуют активации) и сигнал-зависимые. Последние дифференцируются по типу и способу действия активирующего сигнала.
Структурная классификация белковых факторов транскрипции весьма обширна и включает 6 надклассов, в которые входят множество классов и семейств.
Принцип действия
Функционирование базальных факторов представляет собой каскадную сборку различных субъединиц с образованием комплекса инициации и активацией транскрипции. По сути, этот процесс является заключительным этапом воздействия белка-активатора.
Специфические факторы могут регулировать транскрипцию на двух этапах:
- сборка комплекса инициации;
- переход к продуктивной элонгации.
В первом случае работа специфических ТФ сводится к первичной перестройке хроматина, а также привлечению, ориентации и модификации медиатора, полимеразы и базальных факторов на промоторе, что приводит к активации транскрипции. Главным элементом передачи сигнала является медиатор - комплекс из 24 субъединиц, выступающий в качестве посредника между регуляторным белком и РНК-полимеразой. Последовательность взаимодействий индивидуальна для каждого гена и соответствующего ему фактора.
Регуляция элонгации осуществляется за счет взаимодействия фактора с белком P-Tef-b, который помогает РНК-полимеразе преодолеть ассоциированную с промотором паузу.
Функциональные структуры ТФ
Факторы транскрипции имеют модульную структуру и выполняют свою работу за счет трех функциональных доменов:
- ДНК-связывающего (DBD) – нужен для распознавания и взаимодействия с регуляторным участком гена.
- Транс-активирующего (TAD) – позволяет взаимодействовать с другими регуляторными белками, включая транскрипционные факторы.
- Сигнал-распознающего (SSD) – необходим для восприятия и передачи регуляторных сигналов.
В свою очередь ДНК-связывающий домен имеет множество типов. К основным мотивам в его структуре относятся:
- "цинковые пальцы";
- гомеодомен;
- "β"-слои;
- петли;
- "лейциновая молния";
- спираль-петля-спираль;
- спираль-поворот-спираль.
Благодаря этому домену транскрипционный фактор "прочитывает" нуклеотидную последовательность ДНК по форме рисунка на поверхности двойной спирали. Благодаря этому возможно специфическое узнавание определенных регуляторных элементов.
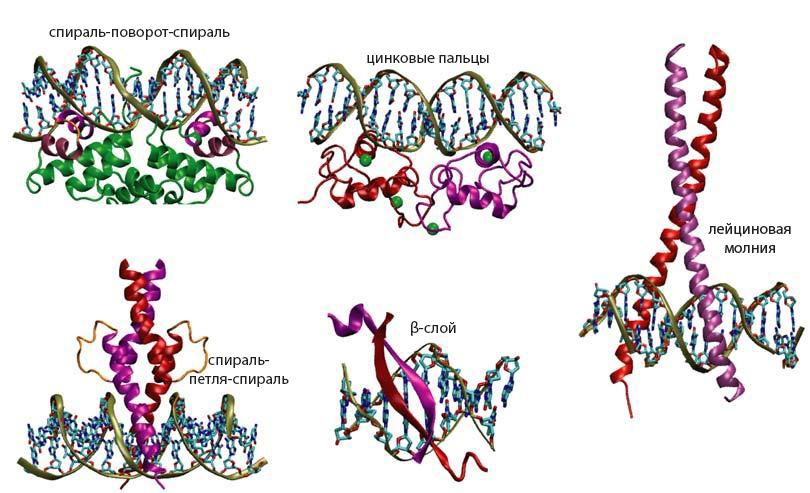
Взаимодействие мотивов со спиралью ДНК основывается на точном соответствии между поверхностями этих молекул.
Регуляция и синтез ТФ
Существует несколько путей регуляции влияния транскрипционных факторов на транскрипцию. К ним относятся:
- активация – изменение функциональности фактора по отношению к ДНК за счет фосфорилирования, присоединения лиганда или взаимодействия с другими регуляторными белками (в том числе ТФ);
- транслокация – транспортировка фактора из цитоплазмы в ядро;
- доступность сайта связывания – зависит от степени конденсации хроматина (в состоянии гетерохроматина ДНК недоступна для ТФ);
- комплекс механизмов, характерных и для других белков (регуляция всех процессов от транскрипции до пострансляционной модификации и внутриклеточной локализации).
Последний способ определяет количественный и качественный состав транскрипционных факторов в каждой клетке. Некоторые ТФ способны регулировать свой синтез по типу классической обратной связи, когда ингибитором реакции становится ее собственный продукт. В таком случае определенная концентрация фактора останавливает транскрипцию кодирующего его гена.
Общие факторы транскрипции
Эти факторы необходимы для начала транскрипции любых генов и в номенклатуре обозначаются как TFl, TFll и TFlll в зависимости от вида РНК-полимеразы, с которой они взаимодействуют. Каждый фактор состоит из нескольких субъединиц.
Базальные ТФ выполняют три основные функции:
- правильное расположение РНК-полимеразы на промоторе;
- расплетание цепей ДНК в области начала транскрипции;
- освобождение полимеразы от промотора в момент перехода к элонгации;
Определенные субъединицы базальных факторов транскрипции связываются с регуляторными элементами промотора. Самым важным является ТАТА-бокс (характерен не для всех генов), расположенный на расстоянии "-35" нуклеотидов от точки инициации. Другие сайты связывания включают последовательности INR, BRE и DPE. Некоторые ТФ напрямую с ДНК не контактируют.
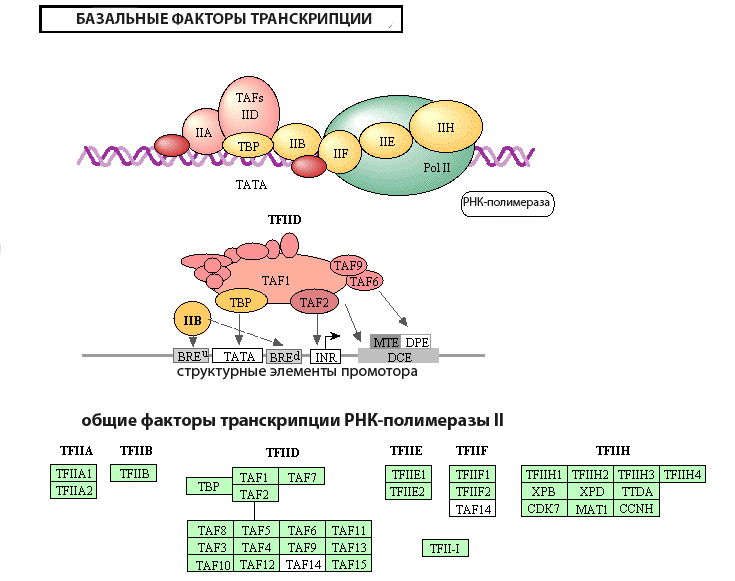
В группу главных факторов транскрипции РНК полимеразы ll входят TFllD, TFllB, TFllF, TFllE и TFllH. Латинская буква в конце обозначения указывает на очередность обнаружения этих белков. Так, первым был выделен фактор TFlllA, относящийся к РНК-полимеразе lll.
| Название | Число белковых субъединиц | Функция |
| TFllD | 16 (TBP +15 TAFs) | TBP связывается с ТАТА-боксом, а TAFs узнают другие последовательности промотора |
| TFllB | 1 | Распознает BRE-элемент, точно ориентирует полимеразу в сайте инициации |
| TFllF | 3 | Стабилизарует взаимодействие полимеразы с TBP и TFllB, облегчает присоединение TFllE и TFllH |
| TFllE | 2 | Присоединяет и регулирует TFllH |
| TFllH | 10 | Разъединяет цепи ДНК в точке инициации, освобождает синтезирующий РНК фермент от промотора и главных факторов транскрипции (биохимия процесса основывается на фосфолирировании Cer5-C-концевого домена РНК-полимеразы) |
Сборка базальных ТФ происходит только при содействии активатора, медиатора и хроматин-модифицирующих белков.
Специфические ТФ
Через контроль генетической экспресии эти факторы транскрипции регулируют биосинтетические процессы как отдельных клеток, так и целого организма начиная от эмбриогенеза заканчивая тонкой фенотипической адаптацией к изменяющимся условиям среды. Сфера влияния ТФ включает 3 основных блока:
- развитие (эмбрио- и онтогенез);
- клеточный цикл;
- ответ на внешние сигналы.
Особая группа факторов транскрипции регулирует морфологическую дифференцировку зародыша. Этот белковый набор кодируется особой консенсусной последовательностью длиной 180 пар нуклеотидов, названной гомеобоксом.
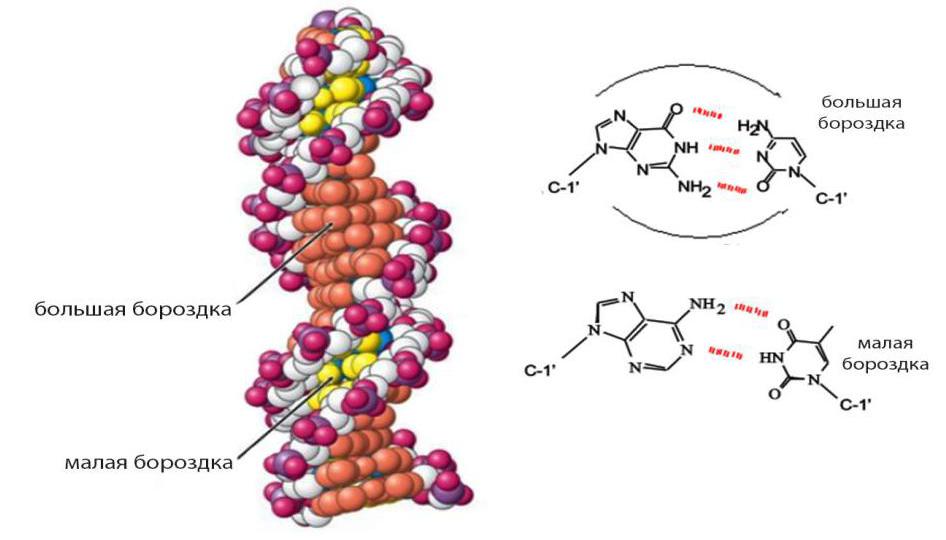
Для того чтобы определить, какой именно ген должен быть транскрибирован, регуляторный белок должен "отыскать" и связаться со специфическим участком ДНК, выполняющим роль генетического переключателя (энхансер, сайленсор и т. д.). Каждой такой последовательности соответствуют один или несколько родственных транскрипционных факторов, которые узнают нужный сайт за счет совпадения химических конформаций конкретного внешнего отрезка спирали и ДНК-связывающего домена (принцип ключ-замок). Для распознавания используется участок первичной структуры ДНК, называемый большой бороздкой.
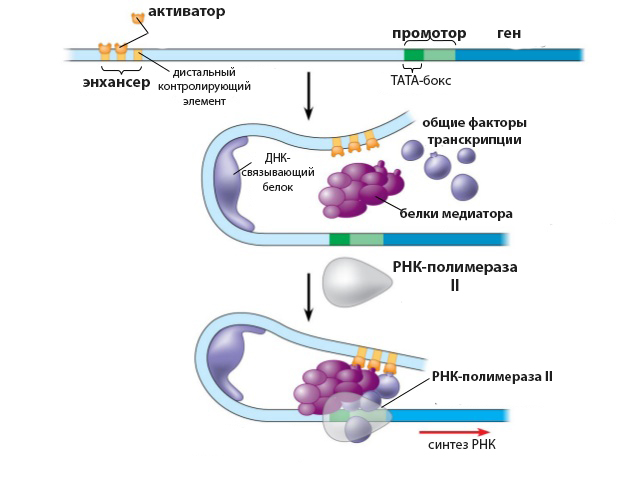
После связывания с ДНК действия белка-активатора запускают ряд последовательных этапов, приводящих к сборке преинициаторного комплекса. Обобщенная схема этого процесса выглядит следующим образом:
- Связывание активатора с хроматином в области промотора, привлечение АТФ-зависимых перестраивающих комплексов.
- Перестройка хроматина, активация гистон-модифицирующих белков.
- Ковалентная модификация гистонов, привлечение других белков-активаторов.
- Связывание дополнительных активирующих белков с регуляторной областью гена.
- Привлечение медиатора и общих ТФ.
- Сборка преинициаторного комплекса на промоторе.
- Воздействие других белков-активаторов, перестройка субъединиц преинициаторного комплекса.
- Начало транскрипции.
Порядок этих событий от гена к гену может изменяться.
Такому большому количеству механизмов активации соответствует столь же широкий набор способов репрессии. То есть ингибируя один из этапов на пути к инициации, регуляторный белок может снизить ее эффективность или полностью блокировать. Чаще всего репрессор задействует сразу несколько механизмов, гарантируя отсутствие транскрипции.
Координированный контроль генов
Несмотря на то что каждый транскриптон имеет свою систему регуляции, у эукариотов есть механизм, позволяющий подобно бактериям запускать или останавливать группы генов, направленных на выполнение конкретной задачи. Это достигается с помощью определяющего фактора транскрипции, который завершает комбинации других регуляторных элементов, необходимых для максимальной активации или подавления гена.
У транскриптонов, подверженных такой регуляции, взаимодействие разных компонентов ведет к одному и тому же белку, выполняющему роль результирующего вектора. Поэтому активация такого фактора оказывает влияние сразу на несколько генов. Система работает по принципу каскада.
Схему координированного контроля можно рассмотреть на примере онтогенетической дифференциации клеток скелетных мышц, предшественниками которых являются миобласты.
Транскрипция генов, кодирующих синтез характерных для зрелой мышечной клетки белков, запускается с помощью любого из четырех миогенных факторов: MyoD, Myf5, MyoG и Mrf4. Эти белки активируют синтез самих себя и друг друга, а также включают гены дополнительного фактора транскрипции Mef2 и структурных мышечных белков. Mef2 участвует в регуляции дальнейшей дифференциации миобластов, одновременно поддерживая концентрацию миогенных белков по механизму положительной обратной связи.



























