Вторым этапом реализации генетической информации является синтез белковой молекулы на основе матричной РНК (трансляция). Однако в отличие от транскрипции нуклеотидная последовательность не может быть переведена в аминокислотную напрямую, так как эти соединения имеют разную химическую природу. Поэтому для осуществления трансляции требуется посредник в виде транспортной РНК (тРНК), функция которого состоит в переводе генетического кода на "язык" аминокислот.
Общая характеристика транспортной РНК
Транспортные РНК или тРНК - это небольшие молекулы, которые доставляют аминокислоты к месту синтеза белка (в рибосомы). Количество этого вида рибонуклеиновой кислоты в клетке составляет примерно 10 % от общего пула РНК.
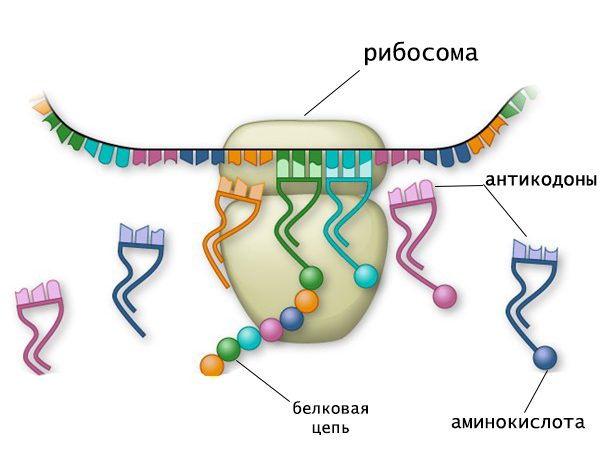
Как и другие разновидности рибонуклеиновых кислот, тРНК состоит из цепочки рибонуклеозидтрифосфатов. Длина нуклеотидной последовательности насчитывает 70-90 звеньев, и около 10 % состава молекулы приходится на минорные компоненты.
Из-за того, что каждой аминокислоте соответствует свой переносчик в виде тРНК, клетка синтезирует большое количество разновидностей этой молекулы. В зависимости от вида живого организма этот показатель варьирует от 80 до 100.
Функции тРНК
Транспортная РНК является поставщиком субстрата для белкового синтеза, который происходит в рибосомах. За счет уникальной способности связываться и с аминокислотами, и с матричной последовательностью тРНК выполняет функцию смыслового адаптера при переводе генетической информации из формы РНК в форму белка. Взаимодействие такого посредника с кодирующей матрицей, как в транскрипции, основано на принципе комплементарности азотистых оснований.
Главная функция тРНК заключается в акцептировании аминокислотных звеньев и их транспортировке в аппарат белкового синтеза. За этим техническим процессом стоит огромный биологический смысл - реализация генетического кода. Осуществление этого процесса основано на следующих особенностях:
- все аминокислоты кодируются триплетами нуклеотидов;
- для каждого триплета (или кодона) существует антикодон, входящий в состав тРНК;
- каждая тРНК может связаться только с определенной аминокислотой.
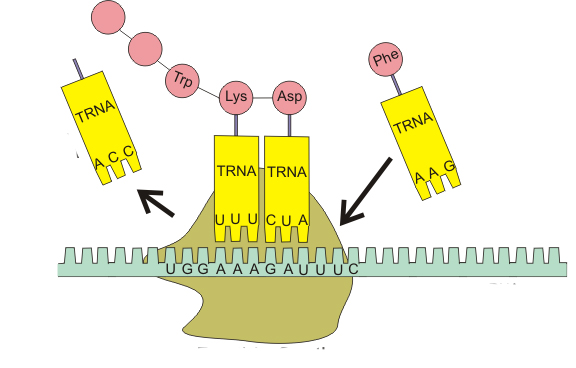
Таким образом, аминокислотная последовательность белка определяется тем, какие тРНК и в каком порядке будут комплементарно взаимодействовать с матричной РНК в процессе трансляции. Это возможно благодаря наличию в транспортной РНК функциональных центров, один из которых отвечает за избирательное присоединение аминокислоты, а другой - за связывание с кодоном. Поэтому функции и структура тРНК тесно взаимосвязаны.
Строение транспортной РНК
Уникальность тРНК заключается в том, что ее молекулярная структура не линейна. Она включает в себя спиральные двуцепочечные участки, которые называют стеблями, и 3 одноцепочечные петли. По форме такая конформация напоминает клеверный лист.
В структуре тРНК различают следующие стебли:
- акцепторный;
- антикодоновый;
- дигидроуридиловый;
- псевдоуридиловый;
- добавочный.
Двойные спирали стеблей содержат от 5 до 7 Уотсон-Криксоновских пар. На конце акцепторного стебля расположена небольшая цепочка неспаренных нуклеотидов, 3-гидроксил которой является местом прикрепления соответствующей молекулы аминокислоты.
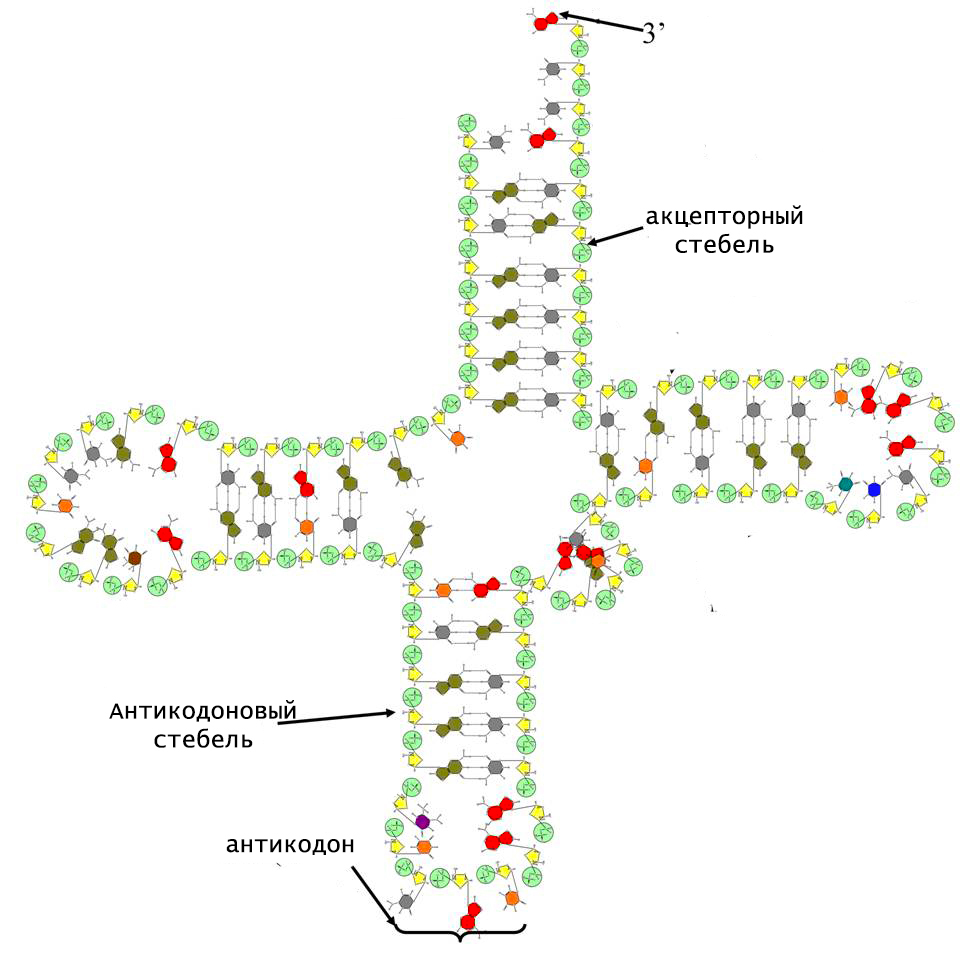
Структурной областью для соединения с мРНК служит одна из петель тРНК. Она содержит антикодон, комплементарный смысловому триплету в матричной РНК. Именно антикодон и акцептирующий конец обеспечивают адапторную функцию тРНК.
Третичная структура молекулы
"Клеверный лист" является вторичной структурой тРНК, однако за счет фолдинга молекула приобретает L-образную конформацию, которая скрепляется дополнительными водородными связями.
L-форма представляет собой третичную структуру тРНК и состоит из двух практически перпендикулярных А-РНК спиралей, имеющих длину 7 нм и толщину 2 нм. Такая форма молекулы имеет всего 2 конца, на одном из которых расположен антикодон, а на другом - акцепторный центр.
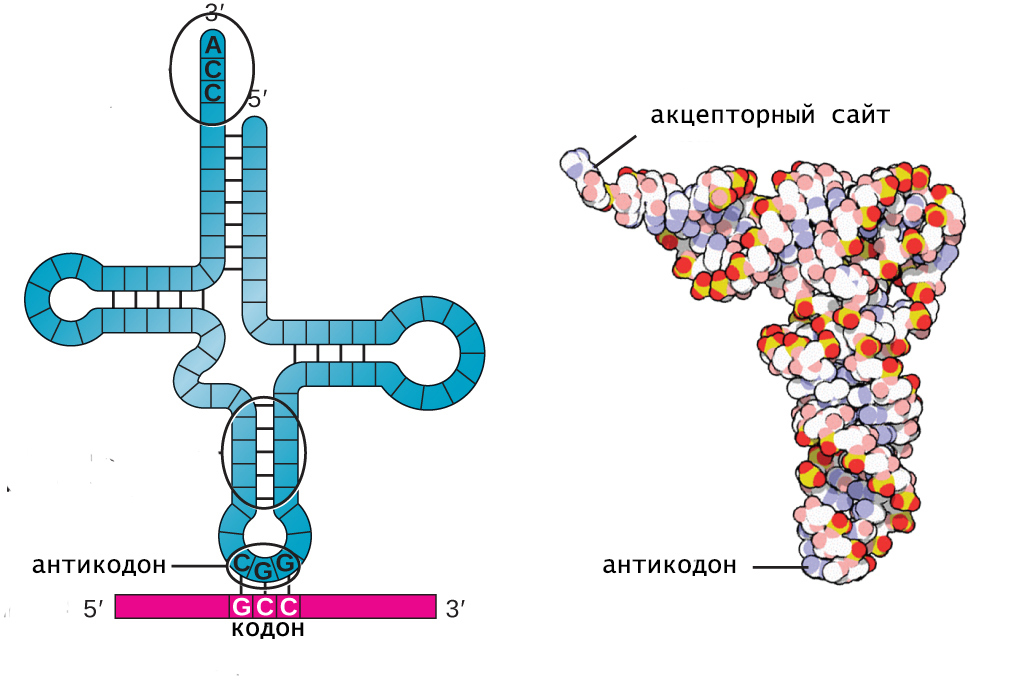
Особенности связывания тРНК с аминокислотой
Активацию аминокислот (их присоединение к транспортной РНК) осуществляет аминоацил-тРНК-синтетаза. Этот фермент одновременно выполняет 2 важных функции:
- катализирует образования ковалентной связи между 3`-гидроксильной группой акцепторного стебля и аминокислотой;
- обеспечивает принцип избирательного соответствия.
Для каждой из 20 аминокислот есть своя аминоацил-тРНК-синтетаза. Она может взаимодействовать только с соответствующим видом транспортной молекулы. Это означает, что антикодон последней должен быть комплементарен триплету, кодирующему именно эту аминокислоту. Например, синтетаза лейцина будет соединяться только с предназначеным для лейцина тРНК.
В молекуле аминоацил-тРНК-синтетазы есть три нуклеотид-связывающих кармана, конформация и заряд которых комплементарны нуклеотидам соответствующего антикодона в тРНК. Таким образом, фермент определяет нужную транспортную молекулу. Гораздо реже фрагментом опознавания служит нуклеотидная последовательность акцепторного стебля.


























