Малеиновая кислота была впервые получена почти 200 лет тому назад. Ее удалось синтезировать посредством перегонки яблочной кислоты. В дальнейшем она нашла свое применение в химической области, и об этом стоит рассказать в подробностях. Впрочем, сначала речь пойдет о ее свойствах и прочих особенностях.

Общие характеристики
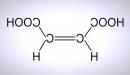
Формула малеиновой кислоты выглядит так: НООС-СН=СН-СООН (или H4C4O4). Данное вещество представляет собой органическое соединение с двумя основами. В соответствии с номенклатурой IUPAC, его правильно называть цис-бутендиовой кислотой.
Характеристики данного вещества можно выделить в следующий перечень:
· Молярная масса составляет 116,07 г/моль.
· Плотность равна 1,59 г/см³.
· Температура плавления и разложения достигает 135 °C. Вспышка происходит при 127 °C.
· Показатель растворимости в воде составляет 78,8 г/л. Лучше всего этот процесс осуществляется при 25°C.
У данного вещества есть транс-изомер, и он известен как фумаровая кислота. Ее молекулы более стабильны, чем у малеиновой. Отсюда и разница в показателях температуры сгорания, составляющая 22,7 кДж/моль.
А еще фумаровая кислота, в отличие от малеиновой, очень плохо растворяется в воде. Всего 6,3 г/л. Это объясняется тем, что в малеиновых молекулах образуется водородная связь.

Получение вещества
Получение малеиновой кислоты осуществляется посредством гидролиза ангидрида C4H2O3. Он представляет собой органическое соединение, имеющее в чистом состоянии твердую консистенцию. Это вещество, как правило, бесцветное или белое.
У ангидрида очень разнообразные химические свойства, ведь он имеет крайне высокую реакционную способность и две функциональные группы. Малеиновая кислота образуется вследствие его взаимодействия с водой. А вот если соединить его со спиртами, то получатся неполные эфиры.
Сам ангидрид раньше синтезировали посредством окисления бензола или иных ароматических соединений. Сейчас этот метод используют редко. Из-за выросших на бензол цен и влияния этого вещества на экологическую среду, его заменили н-бутаном – углеводородом класса алканов.
Вступление в реакции
Стоит отметить, что малеиновую кислоту реально превратить в яблочную. Это достигается посредством гидратации – присоединением молекул воды к ионам/частицам основного вещества. Яблочная кислота известна как пищевая добавка под обозначением Е296. У нее природное происхождение, так что она используется в кондитерском деле и в производстве фруктовых вод. Еще она применима в медицине.
Также малеиновое соединение можно превратить и в янтарную кислоту, которую используют для стимуляции роста растений и повышения урожая. Впервые ее получили в XVII столетии перегонкой янтаря. А сейчас данное вещество синтезируют гидрированием малеиновой кислоты. То есть путем присоединения к ней водорода. А посредством дегидратации (отщеплением воды от молекул) из нее можно получить ангидрид малеиновой кислоты.
Все перечисленные реакции теоретически могли бы использоваться в промышленности для производства указанных веществ. Вот только они экономически невыгодны, поэтому к ним не прибегают.

Применение
Сложно переоценить свойства малеиновой кислоты. Сама она используется лишь для получения фумарового соединения, но вот применение ее производных распространено широко:
· Ангидрид задействован в изготовлении полиэфирной продукции. Смол, в частности. Конечные продукты активно применяются в сфере строительства. Это ЛКМ, искусственный камень, стеклопластики и т. д.
· Реагенты используются для изготовления алкидных смол, которые отлично упрочняют покрытия на масляной основе. Они применяются и в качестве антикоррозийного покрытия.
· Также из ангидрида, поскольку он является сополимером малеиновой кислоты, делают синтетические ткани и искусственные волокна.
· Эфиры данного вещества используют в качестве растворителей. Самым распространенным является диэтилмалеат. Его используют химические лаборатории, оборонные предприятия, а также в сфере лакокрасочной продукции.
· Гидразит малеинового соединения используют как гербицид. Он отлично поражает сорные травы.
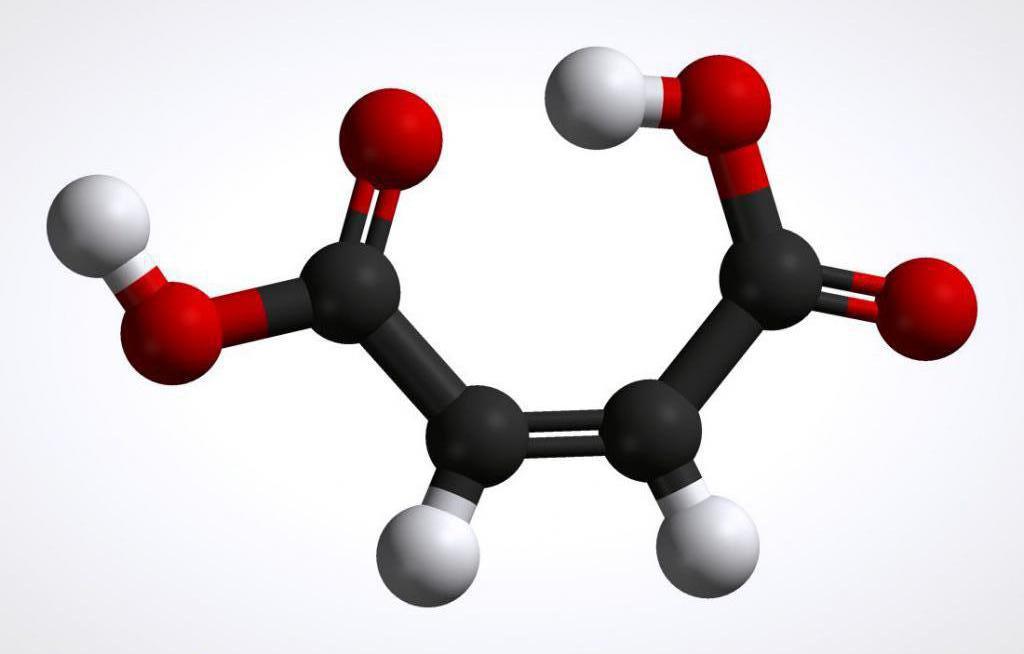
Получение фумаровой кислоты
О нем тоже необходимо сказать пару слов. Чтобы получить фумаровую кислоту, малеиновую каталитически изомеризуют. Данный процесс осуществляется с применением тиомочевины (тиокарбамид). Хотя нередко ее заменяют неорганическими кислотами.
Поскольку фумаровое соединение плохо растворяется, его легко выделить из малеинового вещества. Обе кислоты относятся к конформерам – имеют одинаковое количество атомов и молекул, а также схожую структуру. Но, несмотря на это, они не могут превращаться друг в друга самопроизвольно. Чтобы данный процесс произошел, надо разорвать углеродную двойную связь, но это невыгодно с энергетической точки зрения.
Так что в промышленности используется способ, уже упомянутый ранее – каталитическая изомеризация малеинового соединения в воде.

Применение фумарового соединения
Об этом стоит рассказать напоследок. Дольше всего фумаровая кислота используется в пищевой промышленности. Впервые ее применили в 1946 году. Это соединение имеет фруктовый вкус, поэтому его часто используют в качестве подсластителя. Обозначается Е297.
Еще фумаровой кислотой нередко заменяют винную и лимонную. Это экономически выгодно. Если добавлять цитрат, то для достижения нужного вкусового эффекта понадобится 1.36 г. Фумарата нужно меньше – всего 0.91 г.
Также эфиры данного вещества применяются в процессе лечения такого кожного заболевания, как псориаз. Для взрослого человека установлена дневная норма в 60-105 миллиграмм (точная доза зависит от индивидуального случая). Может быть увеличена со временем до 1300 мг в день.
А соль данного вещества является ключевым компонентом таких препаратов, как "Конфумин" и "Мафусол". Первый помогает организму адаптироваться к недостатку кислорода и регулирует метаболизм. А второй улучшает реологические свойства крови и ее вязкость.
Интересно, что даже человеческий организм способен синтезировать фумарат. Он образуется кожей, когда на нее оказывается воздействие солнечного света. К тому же фумарат – это побочный продукт цикла мочевины.