Гидроксид натрия, или едкий натр – неорганическое соединение, которое относится к классу оснований, или гидроксидов. Также в технике и за рубежом данное вещество называют каустической содой. Тривиальное название – едкий натр – оно получило из-за своего сильного разъедающего действия.

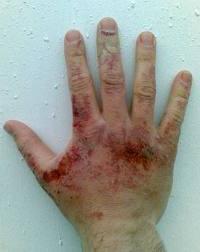
При растворении в воде образует активное вещество – щелочь, – мыльное на ощупь. Данная реакция протекает очень бурно – с разбрызгиванием и выделением тепла. Именно попадание щелочи на кожу и слизистые вызывает сильнейшие химические ожоги, поэтому при работе необходимо быть осторожным и защитить руки и глаза. При попадании данного вещества на эпителий или в глаза, рот, необходимо пораженные места как можно быстрее промыть водой и слабым раствором уксусной (2%) или борной (3%) кислоты, а затем снова водой. После оказания неотложной помощи пострадавшего необходимо показать врачу.
Гидроксид натрия (формула химического соединения - NaOH, струтурная - Na-O-H) - это химически активное вещество, которое может вступать в реакции как с неорганическими, так и с органическими веществами. Обнаружить его в водных растворах поможет качественная реакция на гидроксид–ион с различными индикаторами. Так, лакмусовый индикатор становится темно-синим, метилоранжевый – желтым, а фенолфталеин – малиновым, при этом интенсивность окраски будет зависеть от концентрации щелочи.
Гидрксид натрия вступает в такие реакции:
1. нейтрализации с кислотами, кислотными оксидами и амфотерными соединениями. Результатом данной реакции является образование воды и соли или гидроксокомплека - в случае взаимодействия с амфотерными основаниями и оксидами;
2. обмена с солями;
3. с металлами, которые находятся до водорода в ряду Бекетова и имеют низкий электорхимический потенциал;
4. с неметаллами и галогенами;
4. гидролиза с эфирами;
5. омыления с жирами (образуются мыло и глицерин);
6. взаимодействия со спиртами (образуются вещества алкоголяты).
Также в расплавленном виде едкий натр способен разрушать фарфор и стекло, а при доступе кислорода - благородный металл (платину).
Гидроксид натрия можно получить такими способами:
- электролиз водного раствора NaCl (диафрагменный и мембранный метод),
- химический (известковый и ферритный метод).
В последние годы чаще всего применяются методы на основе электролиза, т.к. они выгоднее.
Каустическая сода пользуется большой популярностью и применяется во многих отраслях промышленности - косметической, целлюлозно-бумажной, химической, текстильной, пищевой. Ее используют в качестве добавки Е-524, для дегазации помещений и при получении биодизельного топлива.
Таким образом, гидроксид натрия – это щелочь, которая нашла широкое применение в различных отраслях хозяйственной деятельности человека за счет своей химически активной природы.





















