С точки зрения химии, пропан - это предельный углеводород, обладающий типичными свойствами алканов. Однако в некоторых областях производства под пропаном понимают смесь двух веществ - пропана и бутана. Далее мы постараемся разобраться, что такое пропан, и зачем его смешивают с бутаном.
Строение молекулы
Каждая молекула пропана состоит из трех атомов углерода, связанных друг с другом простыми одинарными связями, и восьми атомов водорода. Он имеет молекулярную формулу С3Н8. Связи С-С в пропане являются ковалентными неполярными, а вот в паре С-Н углерод немного более электроотрицателен и слегка оттягивает на себя общую электронную пару, а значит, связь ковалентная полярная. Молекула имеет зигзагообразное строение из-за того, что атомы углерода находятся в состоянии sp3-гибридизации. Но, как правило, говорят, что молекула линейная.
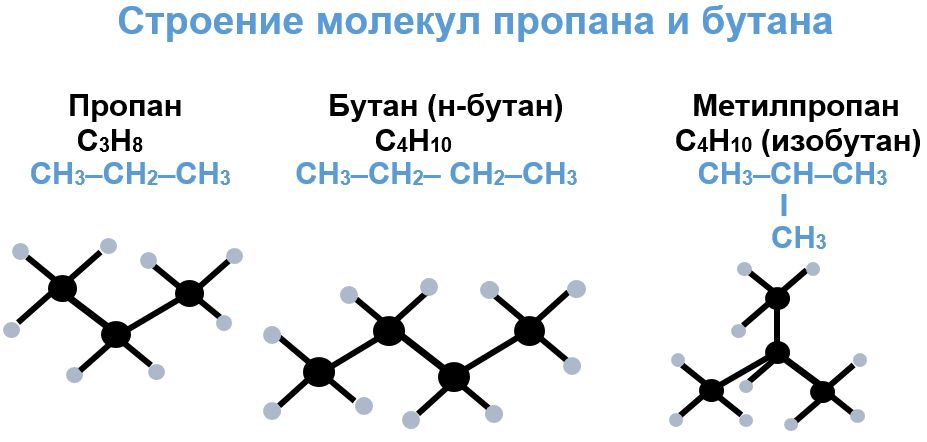
В составе молекулы бутана четыре атома углерода С4Н10, и он имеет два изомера: н-бутан (имеет линейное строение) и изобутан (имеет разветвленное строение). Зачастую, они не разделяются после получения, а существуют в виде смеси.
Физические свойства
Пропан - это газ без цвета и какого-либо запаха. В воде растворяется очень плохо, зато хорошо в хлороформе и простом диэтиловом эфире. Плавится при температуре tпл = -188 °С, а закипает при tкип = -42 °С. Взрывоопасным становится при достижении его концентрации в воздухе выше 2%.
Физические свойства пропана и бутана очень близки. Оба бутана также имеют газообразное состояние при нормальных условиях и не имеют запаха. Практически не растворяются в воде, но хорошо взаимодействуют с органическими растворителями.
В промышленности также имеют важное значение следующие характеристики этих углеводородов:
- Плотность (отношение массы к объему тела). Плотность жидких пропан-бутановых смесей во многом определяется составом углеводородов и температурой. С ростом температуры происходит объемное расширение, и плотность жидкости уменьшается. С ростом давления объем жидкости пропана и бутана сжимается.
- Вязкость (способность веществ в газообразном или жидком состоянии сопротивляться сдвигающим усилиям). Определяется силами сцепления молекул в веществах. Вязкость жидкой смеси пропана с бутаном зависит от температуры (с ее ростом вязкость уменьшается), а вот изменение давления на эту характеристику влияет незначительно. Газы же с ростом температуры увеличивают свою вязкость.
Нахождение в природе и методы получения
Основные природные источники пропана - это нефтяные и газовые месторождения. Он содержится в природном газе (от 0,1 до 11,0%) и в попутных нефтяных газах. Довольно много бутана получают в процессе ректификации нефти - разделении ее на фракции, основываясь на температурах кипения ее компонентов. Из химических способов переработки нефти наибольшее значение имеет каталитический крекинг, в процессе которого происходит разрыв цепи высокомолекулярных алканов. При этом пропана образуется порядка 16-20% от всех газообразных продуктов этого процесса:
СΗ3-СΗ2-СΗ2-СΗ2-СΗ2-СΗ2-СΗ2-СΗ3 ―> СΗ3-СΗ2-СΗ3 + СΗ2=СΗ-СΗ2-СΗ2-СΗ3
Большие количества пропана образуются при гидрогенизации разных видов угля и каменноугольной смолы, они достигают 80% от объема всех образующихся газов.

Также широко распространено получение пропана по методу Фишера-Тропша, который основан на взаимодействии СО и Н2 в присутствии различных катализаторов при повышенных температуре и давлении:
nCO + (2n + 1)Η2 ―> CnΗ2n+2 + nΗ2O
3CO + 7Η2 ―> C3Η8 + 3Η2O
Промышленные объемы бутана также выделяют при нефтегазовой переработке физическими и химическими методами.
Химические свойства
От особенностей строения молекул зависят физические и химические свойства пропана и бутана. Поскольку они являются насыщенными соединениями, для них не характерны реакции присоединения.
1. Реакции замещения. Под действием ультрафиолета легко происходит замещение водорода на атомы хлора:
СН3-СН2-СН3 + Cl2 ―> СН3-СН (Cl)-СН3 + HCl
При нагревании с раствором азотной кислоты, происходит замена атома Н на группу NO2:
СΗ3-СΗ2-СΗ3 + ΗNO3 ―> СΗ3-СΗ (NO2)-СΗ3 + H2О
2. Реакции отщепления. При нагревании в присутствии никеля или палладия происходит отщепление двух атомов водорода с образованием в молекуле кратной связи:
СΗ3-СΗ2-СΗ3 ―> СΗ3-СΗ=СΗ2 + Η2
3. Реакции разложения. При нагревании вещества до температуры порядка 1000 °С происходит процесс пиролиза, который сопровождается разрывом всех имеющихся в молекуле химических связей:
С3Н8 ―> 3С + 4H2

4. Реакции горения. Эти углеводороды горят не коптящим пламенем с выделением большого количества теплоты. Что такое пропан знают многие хозяйки, которые пользуются газовыми плитами. В ходе реакции образуются углекислый газ и парообразная вода:
С3Н8 + 5O2―> 3СО2 + 4H2О
Сгорание пропана в условиях недостатка кислорода приводит к появлению сажи и образованию молекул угарного газа:
2С3Н8 + 7O2―> 6СО + 8H2О
С3Н8 + 2O2―> 3С + 4H2О
Применение
Пропан активно применяется как топливо, поскольку при его горении выделяется 2202 кДж/моль теплоты, это очень высокий показатель. В процессе окисления из пропана получают многие вещества, необходимые для химического синтеза, например, спирты, ацетон, карбоновые кислоты. Он необходим для получения нитропропанов, используемых, как растворители.

В качестве пропеллента применяется в пищевой сфере, имеет код E944. В смеси с изобутаном используется в качестве современного хладагента, не наносящего вред окружающей среде.
Пропан-бутановая смесь
Она имеет много преимуществ перед другими видами топлива, в том числе природным газом:
- высокий КПД;
- легкий возврат к газообразному состоянию;
- хорошие испарение и сжигание при окружающей температуре.

Пропан в полной мере отвечает этим качествам, а вот бутаны несколько хуже испаряются при понижении температуры до -40°С. Исправить этот недостаток помогают добавки, лучшая из которых - это пропан.
Пропан-бутановую смесь применяют для отопления и приготовления пищи, при газовой сварке металлов и их резке, как топливо для транспортных средств и для химического синтеза.



























