Фраза «озоновый слой», ставшая известной в 70-е гг. прошлого века, давно уже набила оскомину. При этом мало кто действительно понимает, что означает это понятие и чем опасно разрушение озонового слоя. Еще большей загадкой для многих является строение молекулы озона, а ведь она напрямую связана с проблемами озонового слоя. Давайте узнаем больше об озоне, его строении и применении этого вещества в промышленности.
Что такое озон
Озон, или, как его еще называют, активный кислород, – это газ лазурного цвета с резким металлическим запахом.
Данное вещество может существовать во всех трех агрегатных состояниях: газообразном, твердом и жидком.
При этом в природе озон встречается только в виде газа, образуя так называемый озоновый слой. Именно из-за его лазурного цвета небо кажется голубым.
Как выглядит молекула озона
Свое прозвище «активный кислород» озон получил из-за своего сходства с кислородом. Так главным действующим химическим элементом в этих веществах является оксиген (О). Однако если в молекуле кислорода содержится 2 его атома, то молекула озона (формула - О3) состоит из 3 атомов этого элемента.
Благодаря такому строению, свойства озона подобны кислородным, однако более выражены. В частности, как и О2, О3 является сильнейшим окислителем.
Самое главное отличие между этими «родственными» веществами, которое помнить жизненно важно для каждого, следующее: озоном нельзя дышать, он токсичен и при вдыхании способен повредить легкие или даже убить человека. При этом О3 прекрасно подходит для очистки воздуха от токсичных примесей. Кстати, именно из-за этого после дождя так легко дышится: озон окисляет вредные вещества, содержащиеся в воздухе, и он очищается.
Модель молекулы озона (состоящая из 3 атомов оксигена) немного напоминает изображение угла, причем его размер - 117°. Эта молекула не имеет неспаренных электронов, поэтому является диамагнитной. Помимо этого, она обладает полярностью, хотя и состоит из атомов одного элемента.
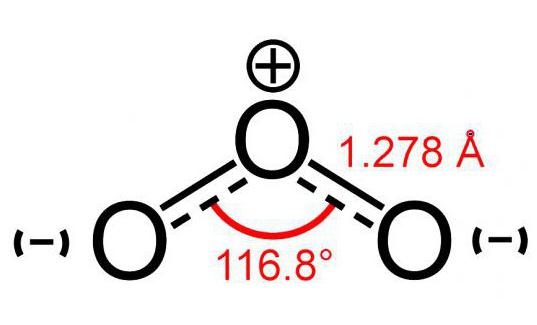
Два атома данной молекулы прочно скреплены между собой. А вот связь с третьим менее надежна. По этой причине молекула озона (фото модели можно увидеть ниже) весьма непрочна и вскоре после образования распадается. Как правило, при любой реакции распада О3 выделяется кислород.
Из-за нестабильности озона его не получается заготавливать и хранить, а также перевозить, как другие вещества. По этой причине его производство более затратно, чем других веществ.
При этом высокая активность молекул О3 позволяет этому веществу быть сильнейшим окислителем, более мощным, чем кислород, и более безопасным, чем хлор.
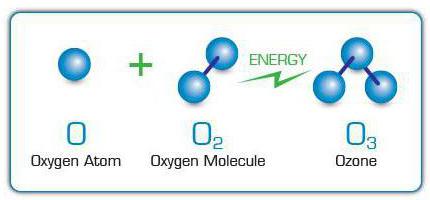
Если молекула озона разрушается и выделяется О2, данная реакция всегда сопровождается выделением энергии. В то же время, чтобы произошел обратный процесс (образование О3 из О2), необходимо затратить ее не меньше.
В газообразном состоянии молекула озона распадается при температуре 70° С . Если ее повысить до 100 градусов и более, реакция значительно ускорится. Также ускоряет период распада молекул озона наличие примесей.
Свойства О3
В каком бы из трех состояний ни пребывал озон, он сохраняет синий цвет. Чем тверже вещество, тем насыщеннее и темнее этот оттенок.
Каждая молекула озона весит 48 г/моль. Она является более тяжелой, чем воздух, что помогает разделять эти вещества между собою.
О3 способен окислять практически все металлы и неметаллы (кроме золота, иридия и платины).
Также это вещество может участвовать в реакции горения, однако для этого нужна более высокая температура, чем для О2.
Озон способен растворяться в Н2О и фреонах. В жидком состоянии он может смешиваться с жидким кислородом, азотом, метаном, аргоном, тетрахлоруглеродом и углекислотой.
Как образуется молекула озона
Молекулы О3 образуются с помощью прикрепления к молекулам кислорода свободных атомов оксигена. Они, в свою очередь, появляются благодаря расщеплению других молекул О2 из-за воздействия на них электрических разрядов, ультрафиолетовых лучей, быстрых электронов и других частиц высокой энергии. По этой причине специфический запах озона можно почувствовать возле искрящих электрических приборов или ламп, излучающих ультрафиолет.
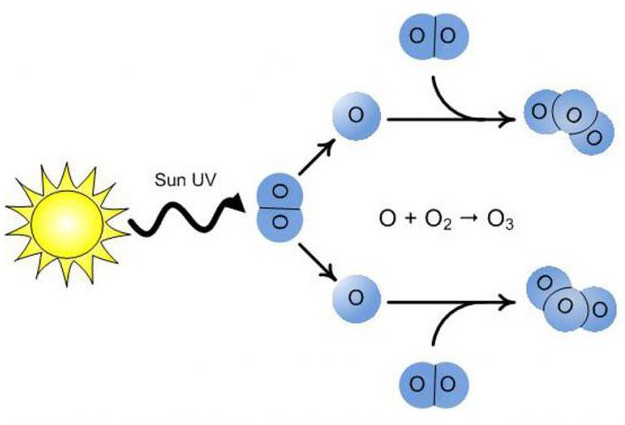
В промышленных масштабах О3 выделяют с помощью электрических генераторов озона или озонаторов. В этих приборах электрический ток высокого напряжения пропускается через газовый поток, в котором находится О2, атомы которого и служат «строительным материалом» для озона.
Иногда в эти аппараты запускают чистый кислород или обычный воздух. От чистоты исходного продукта зависит качество получаемого озона. Так, медицинский О3, предназначенный для обработки ран, добывают только из химически чистого О2.
История открытия озона
Разобравшись с тем, как выглядит молекула озона и как она образуется, стоит познакомиться с историей этого вещества.
Впервые оно было синтезировано нидерландским исследователем Мартином Ван Марумом во второй половине XVIII в. Ученый заметил, что после пропускания электрических искр через емкость с воздухом газ в ней менял свои свойства. При этом Ван Марум так и не понял, что выделил молекулы нового вещества.
А вот его немецкий коллега по фамилии Шейнбейн, пытаясь с помощью электричества разложить Н2О на Н и О2, обратил внимание на выделение нового газа с едким запахом. Проведя массу исследований, ученый описал открытое им вещество и дал ему имя «озон» в честь греческого слова «пахнуть».
Способность убивать грибки и бактерии, а также понижать токсичность вредных соединений, которой обладало открытое вещество, заинтересовала многих ученых. Через 17 лет после официального открытия О3 Вернером фон Сименсом был сконструирован первый аппарат, позволяющий синтезировать озон в любом количестве. А еще через 39 лет гениальный Никола Тесла изобрел и запатентовал первый в мире генератор озона.
Именно этот аппарат уже через 2 года впервые был использован во Франции на очистительных сооружениях для питьевой воды. С началом XX в. Европа начинает переходить на озонирование питьевой воды для ее очистки.
Российская империя впервые использовала эту методику в 1911 г., а через 5 лет в стране было оборудовано почти 4 десятка установок для очистки питьевой воды с помощью озона.
Сегодня озонирование воды постепенно вытесняет хлорирование. Так, 95% всей питьевой воды в Европе очищается с помощью О3. Также весьма популярна данная методика и в США. В СНГ она пока еще на стадии изучения, поскольку, хотя данная процедура и более безопасна и удобна, обходится она дороже, чем хлорирование.
Сферы применения озона
Помимо очистки воды, О3 имеет ряд других сфер применения.
- Озон используется в качестве отбеливателя при производстве бумаги и ткани.
- Активный кислород применяется для дезинфекции вин, а также для ускорения процесса «старения» коньяков.
- С помощью О3 рафинируются различные растительные масла.
- Очень часто это вещество применяют для обработки скоропортящихся продуктов, вроде мяса, яиц, фруктов и овощей. При этой процедуре не остается химических следов, как при использовании хлора или формальдегидов, а продукты могут храниться значительно дольше.
- Озоном стерилизуют медицинское оборудование и одежду.
- Также очищенный О3 применяют для различных медицинских и косметических процедур. В частности, с его помощью в стоматологии дезинфицируют ротовую полость и десны, а также лечат различные заболевания (стоматит, герпес, оральный кандидоз). В европейских странах О3 весьма популярен для дезинфекции ран.
- В последние годы огромную популярность приобретают портативные домашние приборы для фильтрации воздуха и воды с помощью озона.
Озоновый слой - что это?
На расстоянии 15-35 км над поверхностью Земли находится озоновый слой, или, как его еще называют, озоносфера. В этом месте концентрированный О3 служит своеобразным фильтром для вредного солнечного излучения.
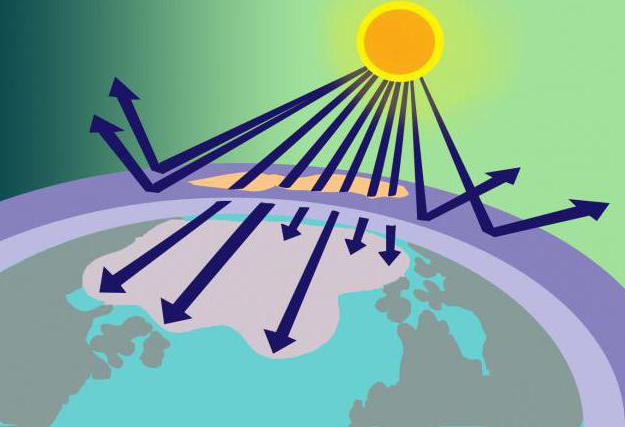
Откуда берется такое количество вещества, если его молекулы нестабильны? Ответить на этот вопрос не сложно, если вспомнить модель молекулы озона и способ ее образования. Итак, кислород, состоящий из 2 молекул оксигена, попадая в стратосферу, нагревается там солнечными лучами. Этой энергии оказывается достаточно, чтобы расщепить О2 на атомы, из которых образуется О3. При этом озоновый слой не только использует часть солнечной энергии, но и фильтрует ее, поглощает опасный ультрафиолет.
Выше было сказано, что озон растворяется фреонами. Эти газообразные вещества (применяются при изготовлении дезодорантов, огнетушителей и холодильников), попав в атмосферу, влияют на озон и способствуют его разложению. Вследствие этого в озоносфере возникают дыры, сквозь которые на планету попадают нефильтрированые солнечные лучи, которые разрушительно действуют на живые организмы.
Рассмотрев особенности и строение молекул озона, можно прийти к выводу, что это вещество, хотя и опасно, но весьма полезно для человечества, если его правильно использовать.


























